- •Физические свойства бензола.
- •Способы получения бензола
- •Химические свойства бензола.
- •Реакции электрофильного замещения в бензоле
- •Влияние заместителей на скорость и направление реакций электрофильного и нуклеофильного замещения в бензольном ряду
- •Электроноакцепторные заместители
- •Нуклеофильное замещение атомов галогенов в бензольном ядре
- •Реакции активированного нуклеофильного замещения с аммиаком и аминами
- •Электронодонорные заместители
- •Пространственное влияние на направление химической реакции
- •Согласованное и несогласованное влияние заместителей
- •Особая группа заместителей
- •Наиболее важные производные ароматических углеводородов
- •Способы получения фенола и его аналогов
- •Электронное и пространственное строение фенола.
- •Химические свойства фенолов
- •Ароматические амины
- •Алкилирование натрового производного ацетанилида галогенпроизводными алканов:
- •Гидролиз n-алкильного производного ацетанилида
- •Содержание
Влияние заместителей на скорость и направление реакций электрофильного и нуклеофильного замещения в бензольном ряду
Любой атом или группа атомов, которую удалось ввести в бензольное ядро вместо одного из атомов водорода, называется заместителем. По отношению к заместителю «Х» различают три различных положения: орто (о), мета (м) и пара (п).
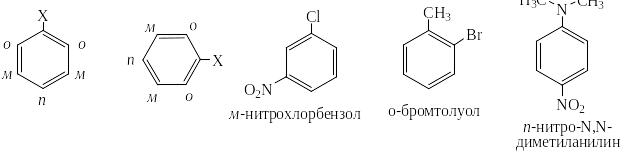
Все заместители, которые могут быть введены в бензольное ядро, делят на три группы:
Электроноакцепторные (ЭА)
Электронодонорные (ЭД)
Особая группа заместителей (ОГ)
Электроноакцепторные заместители
Общим признаком большинства электроноакцепторных заместителей является наличие кратной (двойной или тройной) связи у атома, контактирующего с атомом углерода бензольного ядра. Причём, как правило, эта связь с более электроотрицательным атомом, чем атом связанный с ароматическим циклом. Ниже приведены наиболее часто встречающиеся ЭА-заместители:
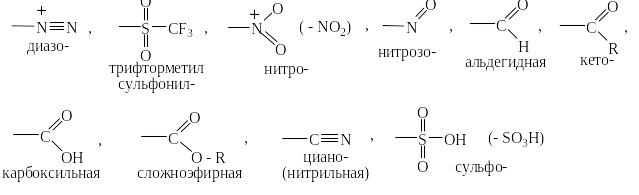
Для предсказания химических свойств заместителей могут быть использованы приёмы очень простой и наглядной теории, предложенной ещё в 1928 году известным американским физико-химиком, лауреатом Нобелевской премии Лайнусом Полингом. Согласно этой теории изображается обычная структурная формула соединения и ещё несколько формул, отличающихся от исходной переносом электрона с одного атома на другой с сохранением обычной валентности атомов и ионов (положительно и отрицательно заряженных). Например, для такого типичного ЭА и часто применяемого заместителя, как нитрогруппа:
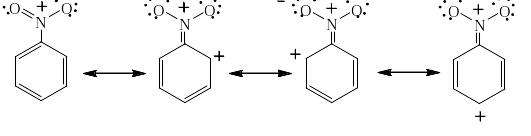
Как видно в первой резонансной структуре в бензольном ядре нет зарядов, но в остальных он присутствует либо в одном из о-положений, либо в п-положении. Легко увидеть также, что валентность незаряженного углерода равна 4, положительно заряженного 3 (третья связь с водородом – её не изображают в бензоле почти всегда), положительно заряженного азота 4, нейтрального кислорода 2 и, наконец, отрицательно заряженного кислорода 1. Ни одна из резонансных форм не является реальностью, но каждая из них объясняет какое-либо свойство реальной молекулы. Например, если молекулу нитробензола атакует положительно заряженная частица, то очевидно, что в о- или п-положение ей попасть будет очень трудно, так как одноименные заряды отталкиваются, и пробиться она сможет лишь в м-положение, где положительного заряда нет.
Мысленно наложив друг на друга резонансные структуры, получим «суперпозицию» или резонансный (мезомерный по Малликену) гибрид, который отталкивает большинство атакующих его частиц, как это показано ниже:

Следует отметить также, что не все частицы А+, даже летящие в м-положение (как прямая «a») достигают цели, так как положительные заряды, находящиеся с двух сторон в о- и п-положении, оттолкнут их большинство, не обладающее достаточно высокой энергией (как прямая «b»).
Таким образом ЭА-заместители затрудняют (резко замедляют) реакции электрофильного замещения и ориентируют вступающий элетрофильный реагент м-положение по отношению к себе. Кроме того, ЭА-заместители облегчают (очень резко ускоряют) реакции нуклеофильного замещения атомов галогенов в бензольном ядре, но только тогда, когда эти атомы стоят к ним в о- и п- положении.
Оценим каково же соотношение констант скоростей одной и той же реакции электрофильного замещения у бензола и нитробензола. Известно, что бензол бромируется меньше, чем за один час при температуре кипения бензола в присутствии катализатора – бромида железа (III):
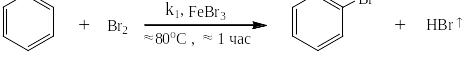
Нитробензол удаётся пробромировать только за 6 – 7 часов и это при температуре его кипения равной 211ОС:
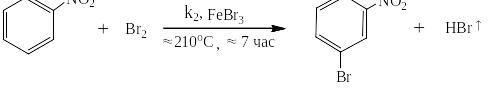
Согласно правилу Вант-Гоффа при увеличении температуры на каждые 10ОС скорость реакции возрастает в 2 – 4 раза. Возьмём среднее значение – 3. Тогда:
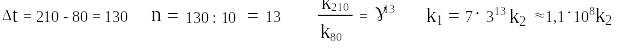
То есть константа скорости бромирования для незамещенного бензола в 10 миллиардов раз выше, чем для бензола с ЭА-заместителем.
Аналогичные закономерности наблюдаются и в других реакциях электрофильного замещения, например, реакция нитрования нитробензола идёт при тех же условиях примерно в 6,5 миллионов раз медленнее, чем нитрование незамещённого бензола:
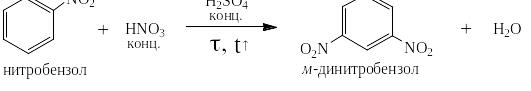
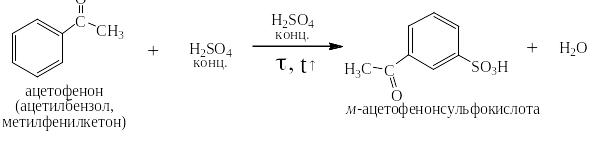
Так же намного медленнее, чем в незамещённом бензоле протекает сульфирование ацетофенона: