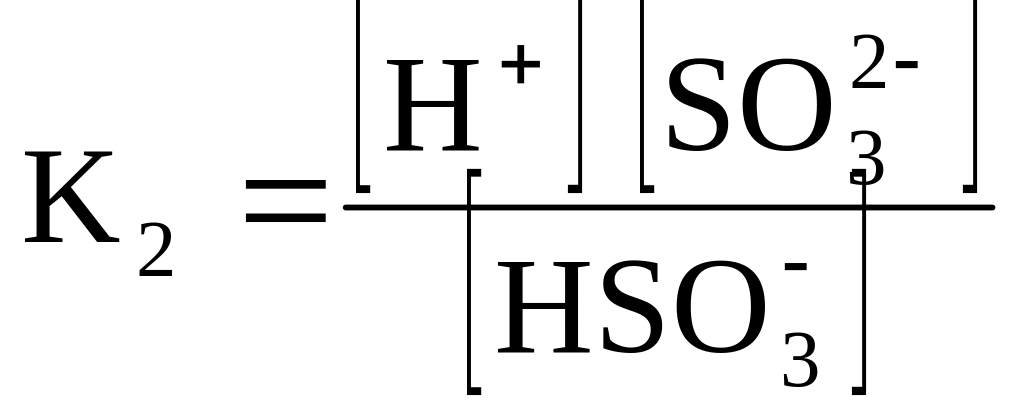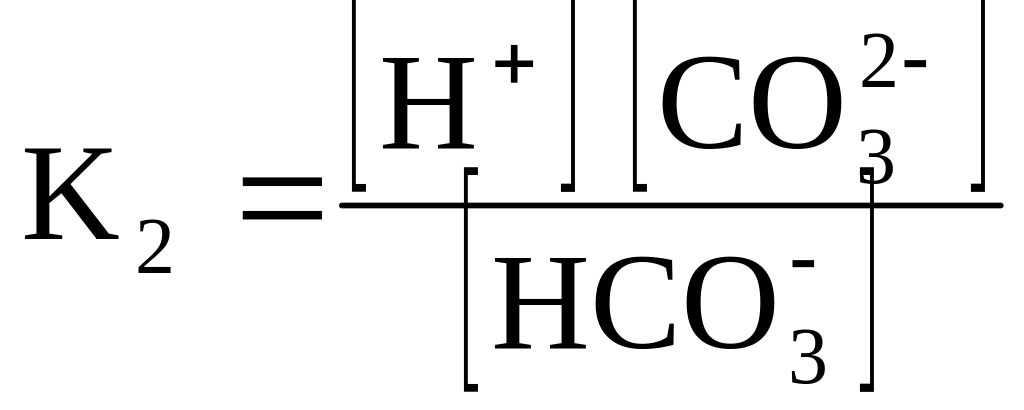- •Модуль I. Основні положення неорганічної та біонеорганічної хімії.
- •1.1. Основні поняття і закони хімії
- •1.2. Будова атома. Періодичний закон та періодична система елементів д.І. Менделєєва. Хімічний зв'язок і будова молекул.
- •1.3. Особливості номенклатури й класифікації неорганічних сполук та генетичний зв'язок між ними.
- •Модуль II. Основні закони хімічних перетворень.
- •2.1. Хімічна кінетика і рівновага.
- •2.2. Поняття про розчини (газоподібні, тверді, рідкі).
- •2.3. Особливості електролітичної дисоціації кислот, основ і солей та реакції у розчинах електролітів.
- •2.4. Гідроліз солей.
- •Модуль III. Основні закони хімічних перетворень із зміною ступенів окиснення елементів або їх валентності.
- •3.1. Роль окисно-відновних процесів у хімії й біології.
- •3.2. Окисно-відновні реакції на електродах. Стандартні електродні потенціали. Гальванічний елемент.
- •3.3. Рівняння Нернста. Принцип розрахунку напрямку окисно-відновних реакцій.
- •3.4. Окисно-відновні реакції:
- •3.5. Координаційні комплексні сполуки, їх роль у живій природі. Просторова інтерпретація координаційних чисел, ізомерія координаційних сполук.
- •3.6. Приклади реакцій утворення найпоширеніших типів координаційних сполук, їх дисоціація, константи нестійкості й стійкості.
- •Модуль IV. Хімія елементів головних та побічних підгруп на прикладі найважливіших біогенних елементів.
- •4.1. Хімія сполук елементів головних підгруп VII, VI, V, IV, III груп (хлор, бром, йод, оксиген, сульфур, нітроген, фосфор, карбон, бор, алюміній). Гідроген і його сполуки. Біологічна роль елементів.
- •4.2. Хімія сполук найважливіших біогенних металів. Метал – макро- і мікроелементи.
- •Зразок екзаменаційного тесту
- •Підписи нпп, які проводили атестації ______________________
- •5. Додатки
- •Константи дисоціації деяких кислот та основ при 250 с
- •Додаток 3 Густина водних розчинів кислот при 18 0с у г/см3
- •Додаток 4
- •Додаток 6 Добуток розчинності малорозчинних речовин
Підписи нпп, які проводили атестації ______________________
______________________
Дата атестації “___”__________________ 2006 р.
КРИТЕРІЇ ОЦІНКИ ЗНАНЬ СТУДЕНТІВ
НА ІСПИТАХ ТА ЗАЛІКАХ
Згідно до “Положення про модульно-рейтингову систему навчання студентів та оцінювання їх знань”, введеного в НАУ з 1 червня 2004 р., рейтинг з дисципліни Rдис визначається в балах відповідно до загальної кількості годин. Для допуску до іспиту або заліку студенту необхідно набрати мінімальну кількість балів для засвоєння матеріалу, що складає 50% (35 балів) від сумарної рейтингової оцінки змістових модулів - RОМ. Шкала оцінки визначається наступним чином:
Оцінка національна |
Оцінка ECTS |
Визначення ECTS |
Рейтинг з дисципліни, бали |
Рейтинг з дисципліни «Загальна та неорганічна хімія», бали |
Відмінно |
А |
Відмінно - відмінне виконання лише з незначною кількістю помилок |
(0,90-1,00)Rдис |
90-100 |
Добре |
B |
Дуже добре - вище середнього рівня з кількома помилками |
(0,82-0,89)Rдис |
82-89 |
C |
Добре - в загальному правильна робота з певною кількістю грубих помилок |
(0,75-0,81)Rдис |
75-81 |
|
Задовільно |
D |
Задовільно - непогано, але зі значною кількістю недоліків |
(0,66-0,74)Rдис |
66-74 |
E |
Достатньо - виконання задовольняє мінімальні критерії |
(0,60-0,65)Rдис |
60-65 |
|
Незадовільно |
FX |
Незадовільно - потрібно працювати перед тим, як отримати позитивну оцінку іспиту (залік) |
(0,35-0,59)Rдис |
35-59 |
F |
Незадовільно - необхідна серйозна подальша робота |
(0,01-0,34)Rдис |
10-34 |
При порушенні студентом дисципліни під час іспиту, користування недозволеними матеріалами викладач має право припинити для цього студента іспит та відмітити у відомості “Іспит припинено”.
5. Додатки
ДОДАТОК 1
Константи дисоціації деяких кислот та основ при 250 с
Сполука
|
Вираз для константи дисоціації |
Кдис |
рК = - lg Кдис |
1 |
2 |
3 |
4 |
HF |
|
6,810-4 |
3,20 |
HCl |
|
1,0107 |
-7,00 |
HBr |
|
1,0109 |
-9,00 |
HI |
|
1,01011 |
-11,00 |
HClO |
|
3,010-8 |
7,53 |
HClO2 |
|
1,110-2 |
1,97 |
HBrO |
|
2,510-9 |
8,66 |
HIO |
|
2,310-11 |
10,64 |
HIO3 |
|
1,610-11 |
10,80 |
H2S |
|
1,010-7
2,510-18 |
6,99
12,60
|
H2SO3 |
|
1,410-2
6,210-8 |
1,85
7,20 |
H2SO4 |
|
1,0103
|
-3,00
|
1 |
2 |
3 |
4 |
|
|
1,210-2 |
1,94 |
HNO2 |
|
6,910-4 |
3,16 |
H3PO4 |
|
7,110-3
6,210-8
5,010-13 |
2,15
7,21
12,00 |
H4P2O7 |
|
1,210-1
7,910-3
2,010-7
4,810-10 |
0,91
2,10
6,70
9,32
|
H3AsO4 |
|
5,610-3
1,710-7
3,010-12 |
2,25
6,77
11,53
|
HAsO2 |
|
610-10 |
9,22 |
HCOOH |
|
1,610-12 |
11,80
|
CH3COOH |
|
1,7510-5 |
4,75 |
HCN |
|
5,010-10 |
9,30
|
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
H2CO3 (“удавана” константа) |
|
4,4510-7
4,6910-11 |
6,35
10,33
|
H2C2O4 |
|
5,610-2
5,4·10-5
|
1,25
4,27
|
H2SiO3 |
|
2,210-10
1,610-12 |
9,66
11,80
|
H2SnO2 |
|
10-15 |
15,00 |
H2SnO3 |
|
10-10 |
10,00 |
H2PbO2 |
|
10-11 |
11,00 |
H3BO3 |
|
5,810-10
1,8·10-13
1,6·10-14 |
9,22
12,74
13,80 |
H2B4O7 |
|
1,010-4
1,010-9 |
4,00
9,00
|
HAlO2 |
|
6,010-15 |
14,22 |
H2MnO4 |
|
~10-1
7,110-11 |
1
10,15 |
1 |
2 |
3 |
4 |
HMnO4 |
|
2,0102 |
- 2,3 |
H2CrO4 |
|
1,610-1
3,210-7 |
0,80
6,50 |
H2MoO4 |
|
2,910-3
1,410-4 |
2,54
3,86
|
H2PbO2 |
|
110-12 |
12,00 |
AgOH |
|
1,1·10-4 |
3,96 |
Al(OH)3 |
|
1,38·10-9 |
8,86 |
Ba(OH)2 |
|
2,310-1 |
0,64 |
Ca(OH)2 |
|
4,010-3 |
1,40 |
Cd(OH)2 |
|
5,010-3 |
2,80 |
Co(OH)2 |
|
4,010-5 |
4,4 |
Cr(OH)3 |
|
1,0210-10 |
9,99 |
Cu(OH)2 |
|
3,410-7 |
6,47 |
|
|
|
|
1 |
2 |
3 |
4 |
Fe(OH)2 |
|
1,310-4 |
3,89 |
Fe(OH)3 |
|
1,810-11
1,410-12 |
10,74
11,87 |
|
|
|
|
Hg(OH)2 |
|
710-12
210-23
|
11,15
22,70 |
LiOH |
|
6,810-1 |
0,17 |
Mn(OH)2 |
|
5,010-4 |
3,30 |
Mg(OH)2 |
|
2,510-3 |
2,60 |
NaOH |
|
5,9 |
- 0,77 |
Ni(OH)2 |
|
2,510-5 |
4,60 |
NH4OH (“удавана” константа) |
|
1,7610-5 |
4,755 |
Pb(OH)2 |
|
9,610-4
3·10-8 |
3,02
7,52
|
Sr(OH)2 |
|
1,510-1 |
0,82 |
Zn(OH)2 |
|
4,010-5
|
4,40
|
ДОДАТОК 2
Густина водних розчинів основ при 18 0С у г/см3
% |
KOH |
NaOH |
NH3 |
% |
KOH |
NaOH |
NH3 |
4 |
1,033 |
1,046 |
0,983 |
34 |
1,334 |
1,374 |
0,889 |
6 |
1,048 |
1,069 |
0,973 |
36 |
1,358 |
1,395 |
0,884 |
8 |
1,065 |
1,092 |
0,967 |
38 |
1,384 |
1,416 |
- |
10 |
1,082 |
1,115 |
0.960 |
40 |
1,411 |
1,437 |
- |
12 |
1,100 |
1,137 |
0,958 |
42 |
1,437 |
1,458 |
- |
14 |
1,118 |
1,159 |
0,946 |
44 |
1,460 |
1,478 |
- |
16 |
1,137 |
1,181 |
0,939 |
46 |
1,485 |
1,499 |
- |
18 |
1,156 |
1,203 |
0,932 |
48 |
1,511 |
1,519 |
- |
20 |
1,176 |
1,225 |
0,926 |
50 |
1,538 |
1,540 |
- |
22 |
1,196 |
1,247 |
0,919 |
52 |
1,564 |
1,560 |
- |
24 |
1,217 |
1,268 |
0,913 |
54 |
1,590 |
1,580 |
- |
26 |
1,240 |
1,289 |
0,908 |
56 |
1,616 |
1,601 |
- |
28 |
1,263 |
1,310 |
0,903 |
58 |
- |
1,622 |
- |
30 |
1,286 |
1,332 |
0,898 |
60 |
- |
1,643 |
- |
32 |
1,310 |
1,352 |
0,893 |
|
|
|
|