
7. Классификация неорганических веществ.
Примеры решения типовых задач
Пример 1. Назовите и напишите графические формулы молекул следующих оксидов: CaO, SeO2, Sb2O3.
Решение:
CaO – оксид кальция;
Графическая формула CaO, Ca=O;
SeO2 – оксид селена (IV);
Графическая формула SeO2 ,О= Se=O
Sb2O3 – оксид сурьмы (III);
Графическая формула Sb2O3, О= Sb-O- Sb=O.
Пример 2.Напишите уравнения реакций получения солей из оксидов хрома.
Решение:
Хром в соединениях имеет степень окисления +6, +3, +2. Его оксиды CrO3, Cr2O3 и CrO соответственно кислотный, амфотерный и основной. Уравнения реакций, характеризующие их способность образовывать соли, следующие:
CrO3 + 2NaOH = Na2CrO4 + H2O
Cr2O3 + 6HCl = 2CrCl3 + 3H2O
Cr2O3 + 2NaOH = 2NaCrO2 + H2O
CrO + 2HCl = CrCl2 + H2O/
Пример 3.С каким из перечисленных веществ вступит в реакцию серная кислота: KOH, CuO, Ba(OH)2,Fe2O3, Al2O3, CO2, SiO2, H3PO4, O2, H2O? Составьте уравнения возможных реакций.
Решение:
Серная кислота не взаимодействует с веществами, имеющими кислотные свойства (H3PO4, CO2 и SiO2), и с кислородом, т.к. она не способна окисляться.
Уравнения возможных реакций:
H2SO4 + 2KOH = K2SO4 + 2H2O
основание
H2SO4 + CuO = CuSO4 +H2O
основной
оксид
H2SO4 + Ba(OH)2 = BaSO4 + 2H2O
основание
3H2SO4 + Fe2O3 = Fe2(SO4)3 + 3H2O
амфотерный
оксид
3H2SO4 + Al2O3 = Al2(SO4)3 + 3H2O
амфотреный
оксид
H2SO4 + KOH = KHSO4 + H2O
2H2SO4 + CuO = Cu(HSO4)2 + H2O
H2SO4(конц.) + nH2O = H2SO4 * nH2O
олеум
Пример 4. Написать реакции, с помощью которых можно осуществить следующие превращения:
Al2O3 KAlO2 Al(OH)3 AlOHSO4 Al2(SO)4 Al Al(NO3)3
Решение:
а) Al2O3 + 2KOH = 2KAlO2 + H2O
метаалюминат
калия
б) 2KAlO2 + H2SO4 + 2H2O 2Al(OH)3 + K2SO4
в) Al(OH)3 +H2SO4 = AlOHSO4 + 2H2O
недост. сульфат
гидроксоаллюминия
г) 2AlOHSO4 + H2SO4 = Al2(SO4)3 + H2O
сульфат алюминия
д) Al2(SO4)3 + 3Mg = 2Al + 3MgSO4
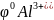 Al
= -1,68 B
Al
= -1,68 B
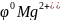 Mg
= -2,37 B
Mg
= -2,37 B
Следовательно, магний активнее алюминия и может вытеснить алюминий из его соли:
е) Al + 4HNO3 = Al(NO3)3 + NO + 2H2O
Al – 3e = Al3+ 1
NO3 + 4H+ + 3e = NO + 2H2O 1
Задания для выполнения контрольной работы
369. Напишите уравнения реакций, свидетельствующих об основных свойствах
FeO, Al2O3 ,CaO , CrO.
370. Напишите уравнения реакций, доказывающих кислотный характер SO2, Mn2O7 , P2O5 , CrO3.
371. Какие из веществ, формулы которых приведены ниже, будут реагировать с оксидом бария:CO2, NaOH , P2O5 ,AlCl3 ,K2O , CuO , H2O? Дайте обоснованный ответ. Напишите уравнения возможных реакций, укажите условия их осуществления и назовите вещества.
372. Какие вещества, формулы которых указаны ниже, будут реагировать с оксидом цинка :NaOH ,Fe2O3 ,Ca(OH)2 SO3 , HNO3?Дайте обоснованный ответ. Запишите уравнения возможных реакций, укажите условия их осуществления и назовите вещества.
373. Напишите уравнения реакций образования Mg2P2O7 ,Ca3(PO4)2 , Mg(ClO4)2,Ba(NO3)2 в результате взаимодействия:
а) основного и кислотного оксидов;
б) основания и кислотного оксида;
в) основного оксида и кислоты.
374. Укажите,какой характер имеют гидраты указанных оксидов:CaO ,N2O5, Mn2O7 ,MnO , SnO ,FeO ,SiO2 ,Fe2O5.Напишите формулы гидратов, назовите их.
375. Назовите и напишите графические формулы оксидов:P2O5 ,CO2 , Mn2O7 , ZnO .Составьте уравнения реакций взаимодействия их с водой.
376. Напишите реакции солеобразования оксидов следующих элементов:
а) лития, бериллия , бора, углерода, азота;
б) натрия, магния, алюминия, фосфора, серы;
в) стронция, серебра, цинка, сурьмы, мышьяка.
377. Напишите уравнения реакций образования кислых солей (назовите эти соли):
а) KOH + H2SO3 г) KOH + H3PO3
б)Ca(OH)2 + H3PO4 д)NaOH + H2S
в) KOH + CO2 е)Ba(OH)2 + H2SO4
378. Напишите уравнения реакций образования основных солей (назовите их):
а) Al(OH)3 + HNO3; б)Mg(OH)2 + HCl; в)Cu(OH)2+HNO3; г)Bi(OH)3+HNO3;
д)Fe(OH)3 + H2SO4; е)Al(OH)3 + H2SO4.
379.Составьте уравнения реакций между кислотами и основаниями, приводящих к образованию солей K2S, KHS, (MgOH)2SO4, Mg(HSiO3)2.
380. Напишите уравнения реакций в молекулярной и ионной формах, при помощи которых можно осуществить следующие превращения:
Ca(NO3)2 NaHCO3 Mg(NO3)2
Ca(OH)2 CO2 MgCl2
а) CaCO3 б) Na2CO3 в) MgCO3
381. Напишите уравнения реакций в молекулярной и ионной формах, при помощи которых можно осуществить следующие превращения:
Fe(OH)2 NaOH Cu(OH)2
FeSO4 FeCl2 Na2CO3 NaNO3 CuCl2 Cu(NO3)2
а) Fe(NO3)2 б) Na2SO4 в) CuCO3
382. Допишите уравнения реакций взаимодействие веществ в молекулярной и ионной формах:
а) Al2(SO4)3 + Ba(NO3)2 …
б) FeCl3 + KOH …
в)Na2CO3 + Ca(OH)2 …
г) Na2SiO3 + HCl …
383. Допишите уравнения следующих реакций в молекулярной и ионной формах:
а)CuSO4 + NaOH …
б)CuCl2 + K2CO3 …
в)CuO + HNO3 …
г)Cu(OH)2 + HCl …
384. Допишите уравнения реакций образования основных солей в молекулярной и ионной формах:
а)Al(OH)3 + HNO3 …
б)Fe2(SO4)3 + NaOH …
в)Zn(OH)2 + H3AsO4 …
г)Mg(OH)2 + HCl …
385. Допишите уравнения реакций образования кислых солей в молекулярной и ионной формах:
а)NaOH + H2CO3 …
б)KOH + H3PO4 …
в)KOH + H2SO4 …
г)Ba(OH)2 + H3PO4 …
386. Напишите уравнения реакций в молекулярной и ионной формах между следующими веществами: а) хлоридом железа (III) и фосфатом натрия; б) сульфатом меди (II) и фосфатом натрия; в) сероводородом и нитратом меди (II);
г) сульфидом калия и сульфатом цинка; д) сульфидом натрия и нитратом магния.
387. Напишите уравнения реакций в молекулярной и ионной формах между следующими веществами; а) хлоридом железа (III) и фосфатом натрия; б) сульфатом меди (II) и фосфатом натрия; в) сероводородом и нитратом меди (II); г) сульфидом калия и сульфатом цинка; д) сульфидом натрия и нитратом магния.
388. Напишите уравнения реакций в молекулярной и ионной формах между следующими веществами; а) гидроксохлоридом магния и гидроксидом натрия; б)гидроксосульфатом железа (III) и серной кислотой; в) гидрофосфатом кальция и гидроксидом кальция; г) гидросульфидом кальция и гидроксидом калия; д) дигидрофосфатом бария и гидроксидом бария.
389. Закончите уравнения следующих реакций получения солей в молекулярной и ионной формах:
а)ZnO + KOH … в)Sn(OH)2 + NaOH …
б)Al2O3 + NaOH … г)Zn + KOH …
390. Закончите уравнения реакций получения солей в молекулярной и ионной формах:
а)Ca + H3PO4 … в)Al(OH)3 + HClO4 …
б)CaO + HNO3 … г)Ba(OH)2 + H3AsO4 …
391. Напишите уравнения реакций образования средних солей между следующими веществами: а) силикатом натрия и азотной кислотой; б) гидрокарбонатом калия и бромводородной кислотой; в) гидросульфатом калия и гидроксидом калия; г) гидроксосульфатом алюминия и серной кислотой; д) гидроксоацетатом алюминия и уксусной кислотой.
392. Составить уравнения реакций получения всеми возможными способами следующих солей: сульфат меди (II), нитрат натрия, карбонат кальция.
393. Какие соли можно получить, имея в своем распоряжении CaSO4, AgNO3, K3PO4, BaCl2? Написать уравнения реакций и назвать полученные соединения.
394 .Составить уравнения, с помощью которых можно осуществить следующие превращения:
а) Fe(OH)3 Fe2O3 Fe FeCl3 FeOHCl2 Fe2(SO4)3 Fe(NO3)3;
б) P P2O5 H3PO4 Ca3(PO4)2 Ca(H2PO4)2 Ca3(PO4)2;
в)Сu (OH)2 CuO Cu CuSO4 Cu2(OH)2SO4 Cu(NO3)2;
395.
а)Al2O3 KAlO2 Al(OH)3 AlOHSO4 Al Al(NO3)3;
б)Zn ZnSO4 Zn(OH)2 Na2ZnO2 ZnCl2 ZnCO3 ZnO;
в)CO2 Ca(HCO3)2 CaCO3 CaCl2 Ca(OH)2 CaCO3 CO2;
396.
а)SiO2 Si Mg2Si SiH4 SiO2 Na2SiO3 H2SiO3 SiO2;
б)Al NaAlO2 HAlO2 K[Al(OH)4] Al2O3 Al AlCl3 AlOHCl2;
в)Fe FeO Fe(NO3)3 FeSO4 Fe(HSO4)2 Fe2(SO4)3 FeOHSO4;
397.
а)Cu Cu(NO3)2 Cu(OH)2 CuOHCl CuCl2 [Cu(NH3)4]Cl2;
б)(NH4)2Cr2O7 Cr2O3 Cr(OH)3 NaCrO2 Na2CrO4 NaHCrO4;
в)NaHCO3 Na2CO3 Na2O Na2SO4 NaOH Cr(OH)3 CrOHSO4;
398.
а)KMnO4 MnO2 MnCl2 Mn(OH)4 MnCl4;
б)ZnO Al2(ZnO2)3 Zn(OH)2 ZnCl2 ZnOHCl ZnCl2.
в)
Fe(OH)2
FeSO4 FeCl2
Fe(NO3)2
Варианты контрольных заданий
Каждый студент выполняет свой вариант контрольных заданий.
Номер варианта указывает преподаватель.
Номер варианта |
Номера задач, относящихся к данному заданию |
01 |
1 11 41 101 161 201 241 281 321 369 |
02 |
2 12 42 102 162 202 242 282 322 370 |
03 |
3 13 43 103 163 203 243 283 323 371 |
04 |
4 14 44 104 164 204 244 284 324 372 |
05 |
5 15 45 105 165 205 245 285 325 373 |
06 |
6 16 46 106 166 206 246 286 326 374 |
07 |
7 17 47 107 167 207 247 287 327 375 |
08 |
8 18 48 108 168 208 248 288 328 376 |
09 |
9 19 49 109 169 209 249 289 329 377 (а, б) |
10 |
10 50 81 110 170 210 250 290 330 377 (в, г) |
11 |
11 51 82 111 171 211 251 291 331 378 (а, б) |
12 |
12 52 83 112 172 212 252 292 332 379 |
13 |
13 53 84 113 173 213 253 293 333 380 (а) |
14 |
14 54 85 114 174 214 254 294 334 380 (б) |
15 |
15 55 86 115 175 215 255 295 335 380 (в) |
16 |
16 56 87 116 176 216 256 296 336 381 (а) |
17 |
17 57 88 117 177 217 257 297 337 381 (б) |
18 |
18 58 89 118 178 218 258 298 338 381 (в) |
19 |
19 59 90 119 179 219 259 299 339 386 |
20 |
20 60 91 120 180 220 260 300 340 387 |
21 |
21 61 92 121 18 1 221 261 301 341 388 |
22 |
22 62 93 122 182 222 262 302 342 389 |
23 |
23 63 94 123 183 223 263 303 343 390 |
24 |
24 64 95 124 184 224 264 304 344 391 |
25 |
25 65 96 125 185 225 265 305 345 392 |
26 |
26 66 97 126 186 226 266 306 346 393 |
27 |
27 67 98 127 187 227 267 307 347 394 (а) |
28 |
28 68 99 128 188 228 268 308 348 394 (б) |
29 |
29 69 100 129 189 229 269 309 349 394 (в) |
30 |
30 70 130 141 190 230 270 310 350 395 (а) |
31 |
31 71 131 142 191 231 271 311 351 395 (б) |
32 |
32 72 132 143 192 232 272 312 352 395 (в) |
33 |
33 73 133 144 193 233 273 313 353 396 (а) |
34 |
34 74 134 145 194 234 274 314 356 396 (б) |
35 |
35 75 135 146 195 235 275 315 357 396 (в) |
36 |
36 76 136 147 196 236 276 316 358 397 (а) |
37 |
37 77 137 148 197 237 277 317 359 397 (б) |
38 |
38 78 138 149 198 237 278 318 360 397 (в) |
39 |
39 79 139 150 199 238 279 319 361 398 (а) |
40 |
40 80 140 151 200 239 280 320 362 398 (б) |
Список литературы
1. Глинка Н. Л. Общая химия: Учебное пособие / Н. Л. Глинка. М.: КНОРУС, 2009. – 752с.
2. Лидин Р. А. Задачи по общей и неорганической химии: учеб. пособие / Р. А. Лидин, В.А. Молочко, Л. Л. Андреева. М.: Владос, 2004. – 384с.
3. Иванов В. Г. Сборник задач и упражнений: Учебное пособие / В. Г. Иванов, О. Н. Гева, Ю. Г. Гаверова. М.: Академия, 2007. – 320с.
4. Ахметов Н. С. Общая и неорганическая химия: Учебник / Н. С. Ахметов. – 5-е изд., исправл. – М.: Высш. шк., 2003. – 743с
