
- •Подготовка к коллоквиуму
- •1.3. Определение точки эквивалентности в титриметрических методах
- •Основные расчетные формулы в титриметрии
- •Приемы титрования
- •Методы титриметрического анализа
- •Титрование сильной кислоты сильной щелочью и наоборот:
- •Титрование слабой кислоты сильной щелочью:
- •Титрование слабого основания сильной кислотой:
Титрование сильной кислоты сильной щелочью и наоборот:
НСl + NaOH = NaCl + H2O; H+ + OH- = H2O
Точка эквивалентности находится в нейтральной среде (рН=7), т.к. образующаяся соль не подвергается гидролизу.
Титрование слабой кислоты сильной щелочью:
СН3СООН + NaOH = CH 3COONa + H2O
В ионном виде:
СН3COOH + OH- = CH3COO- + H2O
В точке эквивалентности образуется соль слабой кислоты и сильного основания, которая вступает в реакцию гидролиза:
СH3COONa + HOH ↔ CH3COOH + NaOH
В ионном виде:
СН3СОО- + НОН ↔ СН3СООН + ОН-
В растворе накапливаются ионы ОН- и точка эквивалентности будет находиться в щелочной среде (рН > 7 ), не совпадая с точкой нейтральности.
Титрование слабого основания сильной кислотой:
NH4OH + HCl = NH4Cl + H2O
В ионном виде:
NH4OH + H+ = NH4+ + H2O
Образующаяся соль слабого основания и сильной кислоты (NH4Cl) подвергается гидролизу, и в растворе накапливаются ионы Н+, что вызывает смещение точки эквивалентности в кислую среду. Следовательно, и в третьем случае точка эквивалентности не совпадает с точкой нейтральности.
Поскольку кислотно-основное титрование не сопровождается внешним эффектом, например, изменением окраски, для фиксирования точки эквивалентности применяют индикаторы
Согласно протолитической теории к кислотам относятся химические соединения, способные в растворах отдавать протоны, а к основаниям вещества, способные присоединять протоны. Для того чтобы кислота могла отдать протон, необходимо присутствие основания, принимающего этот протон. Отдавая протон, кислота образует сопряженное с ней основание, а основание, принимая протон, образует сопряженную с ним кислоту.
В водных растворах кислот имеет место следующее равновесие:
![]()
В воде, которая является кислотой и основанием одновременно и представляет собой слабый электролит устанавливается равновесие
![]()
в сокращенном виде
![]()
Константа равновесия этой реакции при температуре 25° С равна
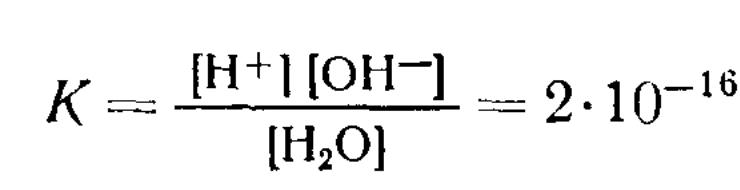
В водных растворах масса воды в большинстве случаев очень велика по сравнению с массой растворенного вещества, количество ее в 1 л раствора можно считать постоянным. Тогда выражение для константы равновесия запишется следующим образом:
![]()
Из уравнения следует, что ионное произведение является величиной постоянной при постоянной температуре. Эту константу называют ионным произведением воды, которое при температуре 25° С равно
![]()
![]()
В чистой воде
![]()
При избытке [ОН-]
![]()
При избытке [Н + ]
Концентрацию водородных ионов обычно используют для характеристики среды. В большинстве расчетов, относящихся к кислотно-основному равновесию, концентрации (и другие величины) удобно выражать в виде отрицательных логарифмов этих величин, обозначаемых знаком „р". Тогда
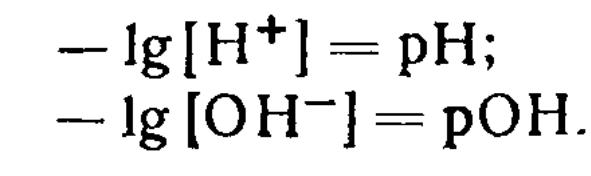
Ионное произведение воды тоже можно выразить в логарифмическом виде
![]()
Сильные кислоты (НХ) и сильные основания (МОН) в водных растворах практически полностью диссоциированы
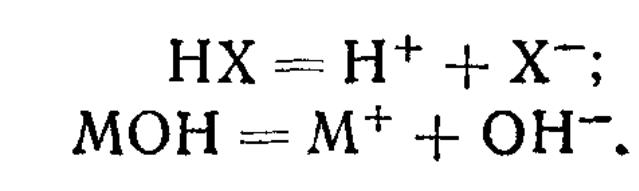
Концентрации Н+ и ОН- в этих растворах в первом приближении можно считать равными общей концентрации СА кислоты (НХ) и соответственно основания (МОН). Следовательно
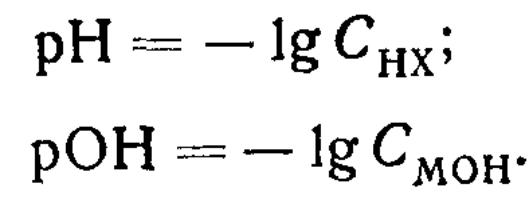
Эти выражения являются приближенными. В более строгих расчетах концентрацию электролитов следует заменять активностью ионов. Между концентрацией иона и активностью его существует следующая зависимость:
![]()
где ɤА — коэффициент активности. Коэффициент активности зависит от ионной силы раствора (μ)
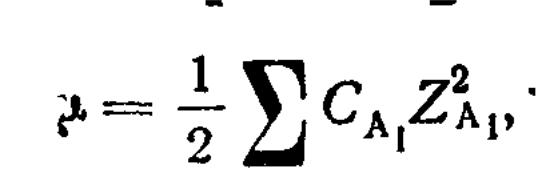
где С концентрации ионов - катионов и анионов
(М), Z. - заряды ионов.
В случае слабых кислот константа равновесия реакции может быть выражена следующим уравнением:
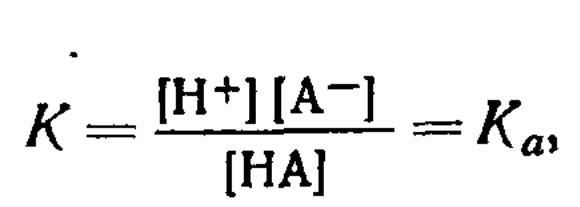
где Ка — константа диссоциации кислоты НА.
Если общую концентрацию кислоты обозначить СНА, а равновесную [НА], то
![]()
Из уравнения следует, что [Н+] = [А-]. Тогда выражение константы диссоциации слабой кислоты можно записать следующим образом:
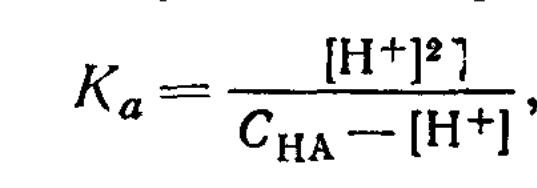
отсюда легко найти концентрацию [Н+]
![]()
Е![]() сли
кислота диссоциирована в незначительной
степени
сли
кислота диссоциирована в незначительной
степени
то приближенно можно считать, что
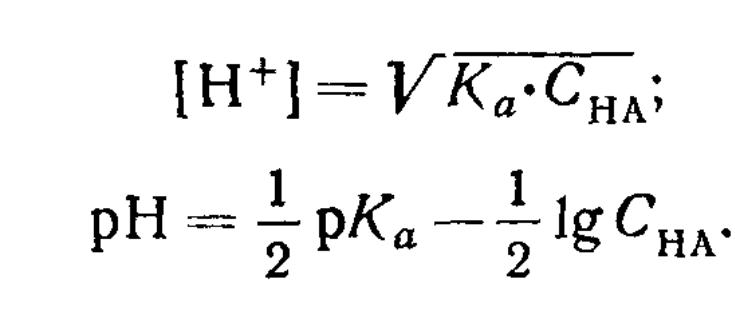
Слабое основание, как и слабая кислота, в водных растворах диссоциирует не полностью
![]()
как и для слабой кислоты
![]()
Поскольку [В+] = [ОН-], уравнение для константы диссоциации слабого основания будет иметь вид
![]()
![]()
Когда [ОН-] < Свон (102 [ОН-] < Свон), можно принять
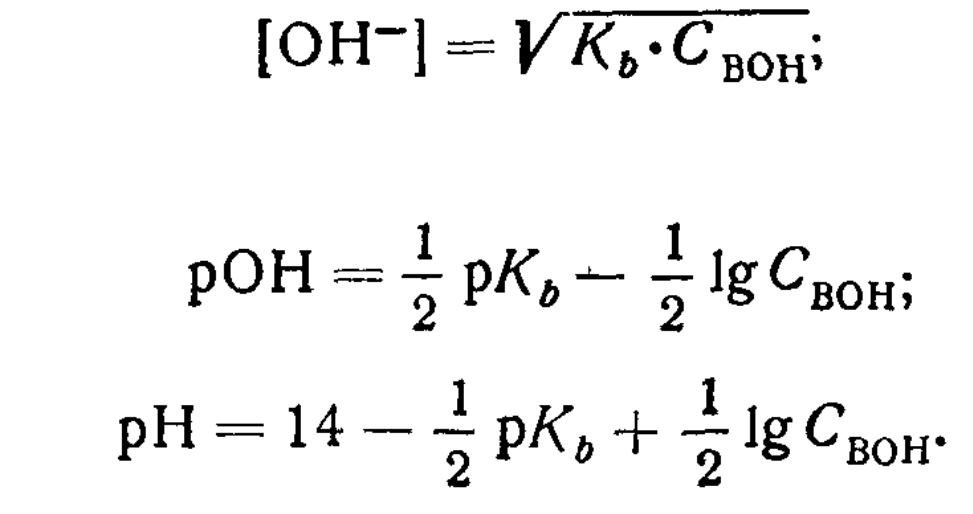
Многоосновные кислоты (H2S04, H2S03, H2C03, Н2С204, Н3Р04 и др.) в водных растворах диссоциируют ступенчато
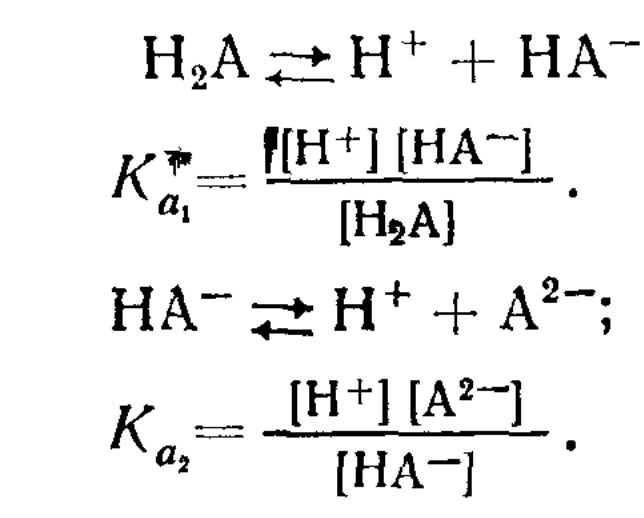
Константы диссоциации по первой ступени всегда больше, чем по второй ступени: Ка1>Ка2. Если Ка1 во много раз больше Ка2 (Ка1 ≥ 104 Ка2), то концентрация ионов водорода определяется главным образом диссоциацией кислоты по первой ступени.
Обозначим через х концентрацию диссоциированной части кислоты. Тогда, при начальной концентрации кислоты С1 равновесные концентрации будут равны
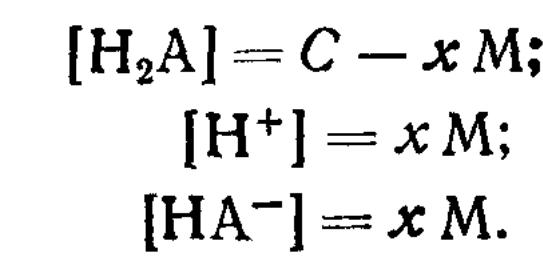
Подставив эти значения в уравнение получим
![]()
отсюда

Если Ка мала, то приближенно можно считать, что
![]()
Поскольку [Н+]~[НА-], то из уравнения находим
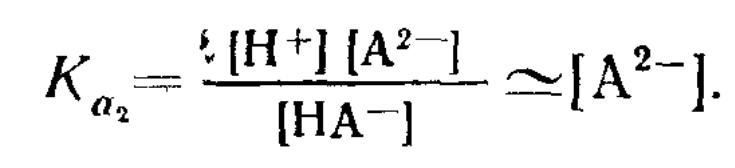
БУФЕРНЫЙ РАСТВОР, поддерживает при изменении состава среды постоянство значения к.-л. характеристики, напр. рН (кислотно-основной буферный раствор) или окислит.-восстановит. потенциала (окислит.-восстановит. буферный раствор).
Значение рН кислотно-основного буферного раствора зависит от концентраций компонентов буферной смеси, находящихся в хим.равновесии, и мало меняется при концентрировании и разбавлении р-ра, введении относительно небольших кол-в в-в, взаимодействующих с одним из компонентов буферного раствора.
Наиб. распространены
водные кислотно-основные буферные растворы.
Они содержат слабую к-ту НА и сопряженное
с ней основание А
-, напр. СН3СООН и СН3СОО-,
NH4+ и NH3. В таких
системах осуществляется равновесие:
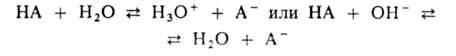
По данным
о константе диссоциации к-ты
Ка = — [Н3О+] [А- ]
/[НА] определяют значение рН р-ра:
![]()
где [НА] и [А-] -равновесные концентрации соотв. к-ты и основания, рКа= —lgКа. Это значение рН остается практически постоянным, т.к. при добавлении небольших кол-в сильных к-т или оснований ионы Н3О+ или ОН-связываются основанием (к-той) с образованием сопряженной к-ты (основания).
Количественно
буферный раствор характеризуется
буферной емкостью- производной![]() ,
где X - характеристика среды, с
-концентрация одного
из компонентов буферной смеси или
добавленного в-ва, количественно
реагирующего с одним из компонентов с
образованием другого.
,
где X - характеристика среды, с
-концентрация одного
из компонентов буферной смеси или
добавленного в-ва, количественно
реагирующего с одним из компонентов с
образованием другого.
Емкость кислотно-основного буферного раствора соответствует числу эквивалентов сильной к-ты или сильного основания, к-рое необходимо добавить к 1 л р-ра, чтобы изменить его рН на единицу. Буферная емкость возрастает при увеличении начальных концентраций его компонентов и максимальна при их равенстве. Буферные свойства проявляются очень слабо, если концентрация одного компонента в 10 раз и более отличается от концентрации другого. Поэтому буферный раствор часто готовят смешением р-ров равной концентрации обоих компонентов либо прибавлением к р-ру одного компонента соответствующего кол-ва реагента, приводящего к образованию равной концентрации сопряженной формы.
Интервал рН (равный обычно рКа± 1), в к-ром данная буферная система может поддерживать постоянное значение рН, называется областью буферирования. В справочной литературе имеются подробные рецепты приготовления кислотно-основных буферных растворов для различных значений рН.
