
- •Основы химической кинетики
- •Основы химической кинетики
- •Введение
- •1. Основные понятия химической кинетики
- •2. Скорость химических реакций
- •2.1. Гомогенные химические реакции
- •2.2. Зависимость скорости гомогенной химической реакции от концентрации реагирующих веществ
- •2.3. Графический метод определения констант дифференциального кинетического уравнения
- •2.4. Зависимость концентрации реагирующих веществ от времени для реакции первого порядка. Интегральное кинетическое уравнение
- •2.5. Скорость гетерогенной химической реакции
- •2.6. Зависимость скорости химической реакции от температуры
- •2.6.1. Уравнение Аррениуса
- •2.6.2. Энергия активации
- •Распределение молекул по энергиям
- •2.6.4. Энтропия активации. Стерический фактор
- •2.6.5. Применение уравнения Аррениуса
- •3. Каталитические реакции
- •3.1. Основные понятия
- •3.2. Сущность каталитического действия
- •3.3. Гомогенный катализ
- •3.4. Гетерогенный катализ
- •4. Химическое равновесие
- •4.1. Состояние равновесия
- •4.2. Константа равновесия
- •4.3. Расчет равновесного состава продуктов химической реакции
- •4.4. Смещение химического равновесия. Принцип Ле Шателье
- •4.4.1. Изменение концентраций
- •4.4.2. Изменение давления
- •4.4.3. Влияние температуры
- •5. Цепные реакции
- •5.1. Неразветвленные цепные реакции
- •5.2. Разветвленные цепные реакции
- •6. Индивидуальные задания для самостоятельной подготовки студентов
- •6.1. Примеры решения типовых задач
- •6.2. Задачи для домашнего задания
- •6.3. Варианты домашних заданий
- •6.4. Варианты дополнительных домашних заданий
- •7. Экспериментальная часть Лабораторная работа «Определение дифференциального кинетического уравнения»
- •Выполнение работы
- •Вопросы для самоконтроля
- •Литература
- •Редактор н.П. Лапина
6.2. Задачи для домашнего задания
Как изменится начальная скорость простой реакции, если:
-
№
задачи
Условие
2А(г) + В(г) А2В(г) реакция для №1.1-1.8
1.1
концентрацию вещества А увеличить в 2 раза
1.2
концентрацию вещества В увеличить в 2 раза
1.3
увеличить давление в системе в 3 раза
1.4
уменьшить объем системы в 2 раза
1.5
уменьшить концентрацию веществ А и В в 3 раза
1.6
снизить давление в системе в 4 раза
1.7
увеличить объем системы в 2 раза
1.8
уменьшить концентрацию вещества А в 2 раза
А(г) + В(г) АВ(г) реакция для №1.9-1.16
1.9
концентрацию вещества А увеличить в 2 раза
1.10
концентрацию вещества В увеличить в 2 раза
1.11
увеличить давление в системе в 3 раза
1.12
уменьшить объем системы в 2 раза
1.13
уменьшить концентрацию веществ А и В в 3 раза
1.14
снизить давление в системе в 4 раза
1.15
увеличить объем системы в 2 раза
1.16
уменьшить концентрацию вещества А в 2 раза
Скорость разложения вещества А описывается кинетическим уравнением первого порядка. Определить начальную концентрацию вещества [А]0, концентрацию вещества через t секунд после начала реакции [A]t, константу скорости реакции k, время реакции t.
-
№
задачи
[A]t,
моль/л
[А]0,
моль/л
k,
с-1
t,
с
Конверсия,
%
Определить
2.1
0,2
0,003
90
[A]t
2.2
0,026
80
t
2.3
0,2
0,045
20
[А]0
2.4
0,045
65
t
2.5
0,1
0,026
30
[A]t
2.6
0,4
0,8
50
k
2.7
0,4
0,013
40
[А]0
2.8
10
30
k
2.9
40
50
k
2.10
0,1
0,3
0,017
t
2.11
0,5
0,005
90
[A]t
2.12
0,1
0,025
20
[А]0
2.13
0,2
0,4
60
k
2.14
0,012
45
t
2.15
0,4
0,012
80
[A]t
2.16
0,3
0,026
30
[А]0
Как изменится скорость реакции A(г) + B(г) C(г) + D(г) при:
а) повышении (понижении) температуры, если энергия
активации реакции равна Еа (№ 3.1-3.10);
б) уменьшении Еа и температуре, равной Т оС
(№ 3.11 – 3.16).
-
№
задачи
Условие задачи
Еа,
кДж/моль
T,
C
3.1
повышении температуры от 27 до 37C
50
3.2
понижении температуры от 45 до 30C
50
3.3
повышении температуры от 20 до 40C
50
3.4
понижении температуры от 60 до 25C
50
3.5
повышении температуры от 10 до 27C
50
3.6
повышении температуры от 27 до 37C
75
3.7
понижении температуры от 45 до 30C
75
3.8
повышении температуры от 20 до 40C
75
3.9
понижении температуры от 60 до 25C
75
3.10
повышении температуры от 10 до 27C
75
3.11
уменьшении энергии активации на 4 кДж
25
3.12
уменьшении энергии активации на 10 кДж
35
3.13
уменьшении энергии активации на 20 кДж
21
3.14
уменьшении энергии активации на 25 кДж
15
3.15
уменьшении энергии активации на 7 кДж
22
3.16
уменьшении энергии активации на 12 кДж
18
Для реакции с заданной константой равновесия Kс и начальными концентрациями газообразных исходных веществ C0 рассчитайте равновесные концентрации исходных веществ и продуктов:
-
№
задачи
Реакция
Kс
C0,
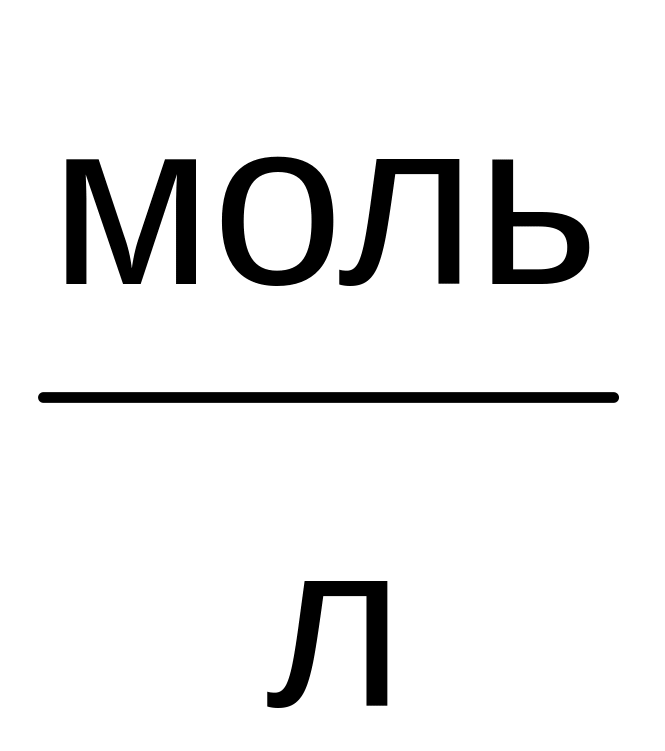
4.1
CO(г) + H2O(г) CO2(г) + H2(г)
2,2
0,02
4.2
FeO(тв) + CO(г) Fe(тв) + CO2(г)
13,6
0,04
4.3
2H(г) H2(г) + 2(г)
0,5
0,02
4.4
SO2 (г) + CO 2 (г) SO3 (г) + CO (г)
0,5
0,01
4.5
H 2(г) + SO3 (г) H 2O (г) + SO2 (г)
1,3
0,01
4.6
2CuO (тв) + CO (г) Cu 2O (тв) + CO 2 (г)
15,8
0,03
4.7
2HBr (г) H 2(г) + Br 2(г)
0,4
0,04
4.8
H 2 (г) + Cl2 (г) 2HCl (г)
3,7
0,01
4.9
N 2 (г) + O 2 (г) 2NO (г)
3,4
0,02
4.10
SO3 (г) + CO (г) SO2(г) + CO 2(г)
1,9
0,02
4.11
H 2(г) + Br 2(г) 2HBr (г)
2,8
0,01
4.12
2HCl (г) H 2 (г) + Cl2 (г)
0,3
0,03
4.13
Fe 2O 3(тв) + CO(г) 2FeO(тв) + CO2 (г)
11,3
0,04
4.14
H 2 (г) + CO 2 (г) H 2O (г) + CO (г)
2,6
0,01
4.15
2NO (г) O 2 (г) + N 2 (г)
0,3
0,04
4.16
NiO (тв) + H 2 (г) Ni (тв) + H 2O (г)
5,6
0,03
Определите константу равновесия Kс и начальные концентрации исходных веществ для гомогенной газообразной реакции, если равновесие в системе установилось при следующих концентрациях: Aравн = 0,04 моль/л; Bравн = 0,05 моль/л; Cравн = 0,08 моль/л.
-
№ задачи
Реакция
5.1
A + B C + D
5.2
2A + B C + D
5.3
A + B 2C + D
5.4
A + B 2С
5.5
A + 2B C + D
5.6
2A C + D
5.7
2A 2C + D
5.8
2B C + 2D
5.9
A + B 2C
5.10
A + B C + 2D
5.11
2B C + D
5.12
A + B C
5.13
2A C + 2D
5.14
A + B С
5.15
A C + D
5.16
2B 2C + D
На основании принципа Ле Шателье, определите в каком направлении сместится равновесие в системе при повышении: а) давления (T = const); б) температуры.
-
№ задачи
Реакция
6.1
COCl2(г) CO(г) + Cl2(г); H 0
6.2
H2(г) + 2(г) 2H(г); H 0
6.3
2CO (г)+ O 2 (г) 2CO2 (г); D H° < 0
6.4
N 2 (г) +O 2 (г) 2NO (г); D H° > 0
6.5
2H 2 (г) + O 2 (г) 2H 2O (г); D H° < 0
6.6
4HCl (г) + O 2 (г) 2H 2O (г) + 2 Cl2 (г); D H° < 0
6.7
2NO (г) +O 2 (г) 2NO 2 (г); D H° < 0
6.8
2SO3 (г) 2SO2 (г) + O 2 (г); D H° > 0
6.9
2O3 (г) 3O2 (г); D H° < 0
6.10
CO (г)+ 2H 2 (г) CH3OH (г); D H° < 0
6.11
N 2O 4 (г) 2NO 2 (г); D H° > 0
6.12
2H 2O (г) 2H 2 (г) + O 2 (г); D H° > 0
6.13
SO3 (г) + NO (г) SO2 (г) + NO 2 (г); D H° > 0
6.14
N 2 (г) +3H 2 (г) 2NH3 (г); D H° < 0
6.15
CH4 (г) + 2H 2O(г) CO2(г) +4H2(г); D H°> 0
6.16
PCl5(г) PCl3(г) + Cl2(г); D H° > 0
7. Определить вид дифференциального кинетического уравнения и константу скорости реакции
n А + m В ® продукты,
если в трех опытах при начальных концентрациях вещества В = 0,2; 0,4; 0,6 моль/л и фиксированной концентрации вещества А, равной [A]0 моль/л, скорости реакции имели значения 1, 2, 3. В трех последующих опытах при различных начальных концентрациях [А] = 0,1; 0,3; 0,5 моль/л и постоянной концентрации В, равной [B]0 моль/л, скорости реакции имели значения 4, 5, 6.
Значения 1 - 6, [A]0 и [B]0 приведены в табл. 4.
8. Приведенные ниже данные соответствуют температурной зависимости константы скорости реакции А продукты, имеющей первый порядок
Температура, К |
Т1 |
Т2 |
Т3 |
Константа k, с-1 |
0,0012 |
0,0027 |
0,0061 |
Определите энергию активации и значение предэкспоненциального множителя. Рассчитайте константу скорости при температуре T4 и определите концентрацию вещества А через 100 с после начала реакции, если известно, что начальная концентрация вещества А равна 2 моль/л. Значения Т1, Т2, Т3, T4 приведены в табл. 5.
9. Химическое равновесие гомогенной реакции, протекающей при T = const, установилось при следующих концентрациях реагирующих веществ (моль/л): А, B, C, D. Затем концентрацию вещества А увеличили до m моль/л.
Рассчитайте новые равновесные концентрации реагирующих веществ. Реакция и значения А, B, C, D, m приведены в табл. 6.
Таблица 4
-
№
задачи
Концентрация, моль/л
Скорость реакции, моль/л·с
[A]0
[B]0
1
2
3
4
5
6
7.1
1,1
1,3
0,1320
0,2640
0,3960
0,0780
0,2340
0,3920
7.2
1,4
2,25
0,3140
0,6270
0,9400
0,0180
0,1620
0,4510
7.3
1,4
1,6
0,1680
0,3360
0,5040
0,0960
0,2880
0,4800
7.4
1,2
1,4
0,2300
0,4600
0,6900
0,0112
0,1010
0,2850
7.5
1,3
1,5
0,1560
0,3130
0,4680
0,0900
0,2700
0,4500
7.6
1,1
1,3
0,1940
0,3880
0,5820
0,0104
0,0940
0,2600
7.7
1,1
1,4
0,1320
0,2640
0,3690
0,0840
0,2530
0,4210
7.8
1,3
1,2
0,0208
0,0832
0,1870
0,0576
0,1730
0,2880
7.9
1,2
1,5
0,1440
0,2880
0,4320
0,0900
0,2700
0,4500
7.10
1,4
1,1
0,0224
0,0900
0,2020
0,0484
0,1450
0,2420
7.11
1,1
1,6
0,1320
0,2640
0,3960
0,0960
0,2880
0,4800
7.12
1,3
1,3
0,0208
0,0832
0,1870
0,0675
0,2030
0,3380
7.13
1,2
1,3
0,1440
0,2880
0,4320
0,0780
0,2340
0,3920
7.14
1,4
1,2
0,0224
0,9000
0,2020
0,0576
0,1730
0,2880
7.15
1,3
1,4
0,1560
0,3130
0,4680
0,0840
0,2530
0,4210
7.16
1,3
1,1
0,0208
0,0832
0,1870
0,0484
0,1450
0,2420
Таблица 5
-
№
задачи
Температура, К
Т1
Т2
Т3
T4
8.1
295
306
316
320
8.2
309
320
333
343
8.3
341
355
370
382
8.4
324
336
350
357
8.5
367
384
401
410
8.6
331
344
359
370
8.7
299
312
324
338
8.8
380
398
417
425
8.9
294
306
319
325
8.10
309
325
341
332
8.11
384
407
433
440
8.12
282
293
306
320
8.13
339
355
374
385
8.14
308
321
338
348
8.15
283
296
311
326
8.16
341
358
376
364
Таблица 6
-
№
задачи
Реакция
Концентрация, моль/л
А
[В]
C
D
m
9.1
A + B C + D
0,2
0,3
0,2
0,3
0,4
9.2
A + B 2C
0,1
0,2
0,3
0
0,2
9.3
A + B C + D
0,3
0,2
0,3
0,3
0,4
9.4
2A B + C
0,1
0
0,2
0,2
0,2
9.5
A + B C + D
0,2
0,4
0,2
0,2
0,3
9.6
A + B 2C
0,2
0,3
0,2
0
0,3
9.7
A + B C + D
0,2
0,3
0,2
0,3
0,3
9.8
A + B C + D
0,1
0,4
0,2
0,2
0,3
9.9
2A B + C
0,3
0
0,3
0,3
0,4
9.10
A + B C + D
0,3
0,3
0,2
0,3
0,4
9.11
A + B 2C
0,1
0,1
0,2
0
0,2
9.12
A + B C + D
0,2
0,2
0,2
0,3
0,3
9.13
2A B + C
0,1
0
0,1
0,1
0,2
9.14
A + B 2C
0,1
0,2
0,1
0
0,2
9.15
A + B C + D
0,1
0,1
0,1
0,1
0,2
9.16
2A B + C
0,1
0
0,1
0,2
0,2
