
Работа 4
ИЗУЧЕНИЕ КИНЕТИКИ ИСПАРЕНИЯ ЖИДКОСТИ И ДИФФУЗИИ ЕЕ ПАРОВ В ВОЗДУХЕ
Теоретическое введение
Всякий гетерогенный процесс включает в себя несколько стадий. Как правило, основные из них – транспорт реагирующих веществ к реакционной поверхности, собственно химическая реакция, отвод продуктов реакции в объем. В зависимости от условий проведения процесса и его особенностей наиболее медленной может быть любая из трех стадий. Если лимитирующими являются первая и третья стадии, то скорость процесса зависит от скорости переноса вещества посредством диффузии. Такой процесс называют диффузионным.
Большое значение имеют диффузионные влияния в процессах испарения жидкостей и сублимации твердых тел. Они играют ведущую роль при сушке, перегонке и т.д. – везде, где скорость процесса лимитируется отводом пара от поверхности конденсированной фазы.
Процесс диффузии подчиняется первому закону Фика
Y = -D (dC/dx), (1)
где Y = 1/S* dm/dτ-количество m вещества, проходящее за время dτ через сечение S (диффузионный поток, г/см2*с); D – коэффициент диффузии; dC/dx – градиент концентрации.
Знак «-» показывает, что диффузия идет в направлении убывания концентрации. Величина D представляет собой удельную скорость диффузии, т.е. количество вещества, проходящего в единицу времени через единицу поверхности при единичном градиенте концентрации. Как следует из выражения (1), коэффициент D имеет размерность D = (длина)2 / время, а выражается его обычно в см2/с.
Кинетическая сторона диффузии ясно из следующих рассуждений. Если на границе раздела фаз концентрация испаряющегося вещества равна CS, а на расстоянии δ-С и равна концентрации в глубине объема V, то можно приближенно заменить
-dC/dx = (CS-C)/δ (2)
и I=D*(CS – C)/δ. (3)
разделив обе части уравнения (3) на объем и переходя к концентрации, получим
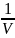 =
=
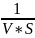 *
*
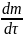 =
=
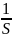 *
*
 =
=
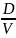 *
*
 .
(4)
.
(4)
Отсюда скорость диффузии запишется
=
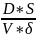 (CS-C).
(5)
(CS-C).
(5)
Таким образом, скорость диффузии кинетически подчиняется уравнению первого порядка относительно концентрации в объеме. Интегрирование (5) дает обычное выражения для константы массопереноса β=DS/Vδ, которая является аналогом константы скорости
β
=
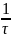 Ln
Ln
 ,
(6)
,
(6)
где С0 – начальная концентрация диффундирующего вещества в объеме.
Диффузия- процесс относительно медленный. Это объясняется тем, что каждая молекула диффундирующего вещества испытывает огромное число соударений и перемещается по сложной траектории, длина которой несоизмеримо велика по сравнению с расстоянием, проходимым молекулой в направлении диффузии.
Вследствие этого лишь небольшая часть молекул, вырвавшихся из жидкости, успевает удалиться от ее поверхности на значительное расстояние. В тонком слое газа над самой поверхностью накапливаются молекулы испаряющегося вещества, и парциальное давление паров растет до тех пор, пока не станет почти равным давлению насыщенного пара. В общем случае говорят: если процесс лимитируется диффузией, то около поверхности раздела фаз устанавливается состояние, близкое к равновесному.
Для экспериментального определения коэффициентов диффузии чаще всего создают такие условия, в которых процесс испарения и диффузии паров протекает стационарно. В стационарном процессе скорость его, а также концентрация вещества в любой точке системы не меняются со временем. Такой процесс диффузии легко роасчитать.
Например, для описания скорости стационарного испарения жидкости в вертикальной цилиндрической трубе, у верхнего среза которой поддерживается постоянное парциальное давление паров Р0 ,Стефан получил уравнение
I=
 Ln
Ln
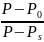 ,
(7)
,
(7)
которое позволяет выразить коэффициент диффузии через измеряемые в опыте величины
D
=
 ,
(8)
,
(8)
где C=MP/PT – концентрация диффундирующего вещества (г/см3), соответствующая его парциальному давлению, которое равно общему атмосферному давлению Р; М – молекулярный вес жидкости; Рs- давление насыщенных паров жидкости при температуре Т; d – плотность жидкости; h – расстояние от поверхности жидкости до верхнего среза трубы; Δh – измерение высоты уровня жидкости в результате испарения за время Δτ; R-универсальная газовая постоянная.
С повышением температуры коэффициент диффузии возрастает экспоненциально в жидкостях и твердых телах
D=D0exp (-E/RT) (9)
И по степенной зависимости в газах
D2/D1 = (T2/T1)n. (10)
Значение показателя степени в последнем уравнении лежит обычно в пределах 1,6-2,0.
Анализ нестационарного процесса испарения жидкости из вертикальной цилиндрической трубы показывает, что данный процесс должен подчиняться уравнению
x2
=
2D*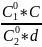 * τ,
(11)
* τ,
(11)
где
х – расстояние, на которое переместилась
в трубке граница жидкость – пар за время
τ;
 - концентрация воздуха на межфазной
границе (кг/м3);
- концентрация воздуха на межфазной
границе (кг/м3);
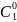 – концентрация насыщенного пара жидкости
на границе (кг/м3);
С =
+
.
– концентрация насыщенного пара жидкости
на границе (кг/м3);
С =
+
.
Экспериментальная часть
В держатели штатива зажимают две тонкие (4-6 мм диаметром) стеклянные пробирки. Одна из них служит для определения коэффициентов диффузии пара жидкости при стационарном процессе испарения по уравнению Стефана (8) (метод 1), другая – для расчета скорости нестационарного испарения по уравнению (11) (метод 2).
Метод 1. Исследуемую жидкость наливают в пробирку на 50-80 мм ниже ее верхнего среза. Через 30 мин, в течение которых происходит установление стационарного состояния, начинают измерения при помощи катетометра. Измерять Δh нужно с большой точностью, так как испарение идет медленно и Δh выражается десятыми долями миллиметра. Отсчеты снимают через 20-40 мин. За время опыта снимают 6-7 отсчетов и строят график Δh, τ, позволяющий судить о стационарности процесса испарения (dh/dτ=const). по уравнению (8) рассчитывают коэффициент диффузии пара жидкости в воздухе. За высоту h принимают среднее ее значение за время опыта (высота диффузионного пространства).
Измерения заносят в таблицу и представляют в виде графиков:
h=f(τ);
Δh/Δτ = t(τ).
Метод 2. Пробирку заполняют исследуемой жидкостью полностью до верхнего среза. Измерения перемещения межфазной границы во времени производят микрометром, постепенно увеличивая время между измерениями от 15-20 до 40-45 мин. Всего снимают 6-7 отсчетов.
Измерения заносят в таблицу и представляют в виде графиков:
x= f(τ);
x2=f(τ);
зависимость скорости испарения I = id от τ и τ-1, i - скорость перемещения, i = dx/dτ. По тангенсу угла наклона графика с учетом давления насыщенного пара исследуемой жидкости при температуре опыта рассчитывают D и сравнивают с полученным значением по методу 1 и литературным данным.
Расчет поверхностных концентраций для метода 2 описан в работе 5.
Контрольные вопросы
как зависит скорость испарения жидкости от температуры?
Каковы признаки диффузионного торможения гетерогенного химического процесса?
Каков порядок реакции, которая лимитируется диффузией?
Назовите примеры химико-технологических процессов, где важно знать закономерности массопереноса.
