
- •Термохімія
- •Молекулярність і порядок реакції
- •Кінетика необоротних реакцій
- •Необоротна реакція першого порядку
- •Необоротна реакція другого поряду
- •3.1 Електрохімічні процеси та їхнє медико-біологїчне значення. Розчини електролітів.
- •3.3 Кондуктометричне визначення ступеня та константи йонізації слабкого електроліту. Закон розведення Оствальда.
- •3.4 Кондуктометричне титрування. Застосування кондуктометрії в медицині.
- •4.1 Електродні потенціали та механізм їх виникнення. Рівняння
- •4.3 Електрохімічні (гальванічні) елементи та електрорушійні сили.
- •4.4. Дифузійні та мембранний потенціали, їхнє біологічне значення. Рівняння Нернста.
- •4 .5 Потенціометрія: потенціометричне визначення рН за допомогою воднево-хлорсрібного та хлорсрібного скляного елемента. Потенціометричне титрування.
- •Ізотерма адсорбції Ленгмюра
- •5.2 Адсорбція на межі поділу рідина - газ та рідина - рідина. Рівняння Гіббса. Орієнтація молекул поверхнево-активних речовин у поверхневому шарі.
- •5.3 Уявлення про структуру біологічних мембран. Адсорбція на межі поділу тверде тіло - газ.
- •5.4 Адсорбція із розчину на поверхні твердого тіла. Фізична та хімічна адсорбція. Закономірності адсорбції розчинених речовин, парів та газів. Рівняння Фрейндліха.
- •6.1 Адсорбція електролітів: специфічна (вибірна) та йонообмінна. Правило Панета- Фаянса.
- •6.2. Йонообмінники природні та синтетичні. Роль адсорбції та йонного обміну в процесах життєдіяльності рослин і організмів.
- •6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
- •6.4. Застосування хроматографії в біології та медицині. (спрс)
- •7.1 Загальна характеристика дисперсних систем: основні визначення та класифікація.
- •7.3 Електричні властивості колоїдно-дисперсних систем: механізм утворення подвійного електричного шару. Рівняння Гельмгольца-Смолуховського. Електрофоретична рухливість.
- •7.4 Електрокінетичні явища: електроосмос, електрофорез, потенціали перебігу та седиментації. Застосування електрофорезу в дослідницькій та клініко-лабораторній практиці.(спрс)
- •8.1 Стійкість та коагуляція дисперсних систем. Коагуляція гідрофобних золів під дією електролітів. Поріг коагуляції. Правило Шульце—Гарді.
- •9.1 Високомолекулярні сполуки - основа живих організмів. Глобулярна та фібрилярна структура білків. Порівняльна характеристика розчинів високомолекулярних сполук, істинних та колоїдних розчинів.
- •9.3 Аномальна в'язкість розчинів вмс. В'язкість крові. Мембранна рівновага Доннана.
- •9.4 Ізоелекгричний стан білка. Ізоелєктрична точка та методи її визначення. Йонний стан біополімерів в водних розчинах.
- •9.5 Значення високомолекулярних сполук (вмс) у медицині та фармації. (спрс).
6.3. Хроматографія. Класифікація хроматографічних методів аналізу за ознакою агрегатного стану фаз, техніки виконання та механізму розподілу. Адсорбційна, йонообмінна та розподільча хроматографія.
У 1903 р. російський ботанік М. С. Цвет виявив, що при пропусканні через шар адсорбенту суміші речовин, що володіють різною адсорбційною здатністю, останні маються в своєму розпорядженні в нім шарами, в порядку своєї адсорбованості (мал. 63). Якщо ці речовини забарвлені, то в адсорбенті видні, шари адсорбованих речовин; звідси цей метод розділення сумішей речовин був названий хроматографічним (хромос - по-грецьки колір). Ця ж назва була збережена і для випадків аналогічного розділення безбарвних речовин. Розрізняють декілька видів хроматографії.
Адсорбционная хроматография основана на избирательности адсорбции веществ тем или иным адсорбентом.
Сущность ее можно пояснить следующим
примером: через адсорбционную колонку,
аналогичную предложенной М. С. Цветом
(рис. 63) и заполненную 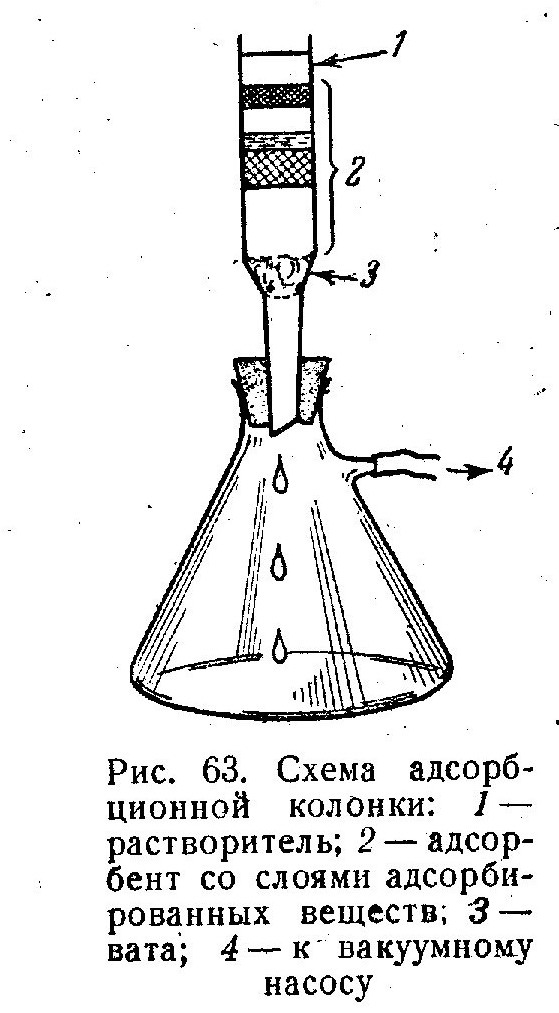 окисью
алюминия, пропускают раствор, содержащий
ионы меди и кобальта. Вначале в верхней
части колонки адсорбируются оба иона,
затем ток растворителя, который
продолжают пропускать, будет вымывать
хуже адсорбируемые окисью алюминия
ионы кобальта и уносить их ниже, на
свободный от ионов меди участок
адсорбента. Таким образом, происходит
постепенное разделение смеси ионов.
окисью
алюминия, пропускают раствор, содержащий
ионы меди и кобальта. Вначале в верхней
части колонки адсорбируются оба иона,
затем ток растворителя, который
продолжают пропускать, будет вымывать
хуже адсорбируемые окисью алюминия
ионы кобальта и уносить их ниже, на
свободный от ионов меди участок
адсорбента. Таким образом, происходит
постепенное разделение смеси ионов.
Ионообменная хроматография. В ее основе лежит обмен ионами между раствором и адсорбентом.
Как и при адсорбционной хроматографии, здесь через адсорбент .пропускают раствор, причем адсорбентом служит какой-либо ионообменник. В верхней части обмениваются наиболее интенсивно адсорбируемые ионы, затем менее интенсивно адсорбируемые и т. д., в результате происходит .послойное выделение ионов из раствора. Таким образом, в этом случае обмен ионами сочетается с избирательностью адсорбции.
Распределительная хроматография. При этом методе используются различия в распределении веществ между несмешивающимися жидкостями. Эти различия определяются законом Нернста: при постоянной температуре соотношение концентраций вещества, распределившегося между двумя несмешивающимися жидкостями (фазами), является величиной постоянной:
c1
----------- = k
c2
В этой форме закон применим для веществ, при растворении не диссоциирующих и не ассоциирующих. Распределительную хроматографию можно пояснить на следующем примере: предположим, что имеется смесь равных количеств веществ A и В ,и две практически несмешивающиеся жидкости — вода и бензол. Допустим, что в этой системе коэффициенты распределения вещества А и В равны 10, т. е. они распределяются в соответствии со своей растворимостью так, что в воде вещества А оказывается в 10
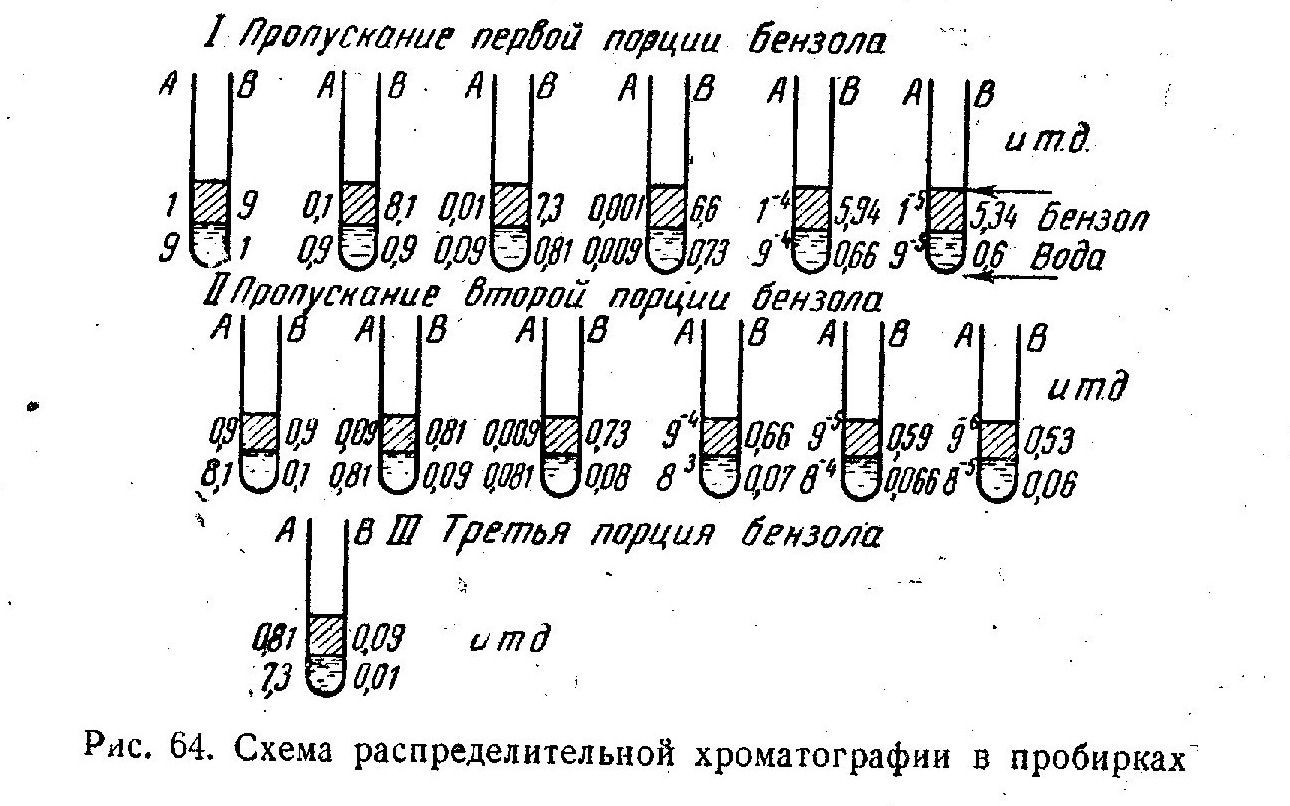
раз больше, чем в бензоле, а вещества В — наоборот, в 10 раз меньше. Приготовим ряд пробирок с водой (так называемая неподвижная фаза хроматографической системы), прильем в первую из них равный объем бензола, а затем добавим разделяемую смесь веществ. После встряхивания пробирки и расслоения жидкостей окажется, что в воде содержится 9 частей А и 1 часть В (рис. 64), а в слое бензола 1 часть А и 9 частей В.
Перенесем этот слой бензола во вторую пробирку, взболтаем, дадим отстояться. В слое бензола теперь останется 0,1 часть А и 8,1 частей В, При перенесении бензола из второй в третью пробирку после перераспределения в нем останется всего 0,01 части А и 7,3 частей В и т. д. В конце ряда слой бензола будет содержать практически только вещество В.
Если же вслед за первой порцией бензола в первую пробирку добавить вторую его порцию, то из слоя воды в бензол перейдет 0,9 содержащегося там вещества В, в третью порцию бензола, которую можно добавить после второй, — еще 0,9 от оставшегося в воде количества В и т. д. Таким образом, последовательным пропусканием порций бензола (подвижный растворитель хроматографической системы) можно добиться накопления в водных слоях первых пробирок ряда чистого вещества А.
Чем меньше отличаются коэффициенты распределения веществ или чем больше количество компонентов смеси, тем длиннее нужен ряд пробирок и тем больше повторных порций подвижного растворителя.
Очень удобным оказалось фиксировать неподвижную фазу (обычно полярный растворитель — воду, спирт) на полярных же веществах, например на хроматографической бумаге (специальный сорт фильтровальной). В этом случае каждое волокно бумаги может рассматриваться как отдельная пробирка, а смена порций подвижного растворителя осуществляется непрерывным его током. Эта разновидность метода называется бумажной хроматографией;
Чаще применяют нисходящую бумажную хроматографию (рис. 65), при которой лист хроматографической бумаги свисает в сосуде из укрепленной в верху его специальной стеклянной «лодочки» со смесью растворителей. Ток этой смеси перемещает разделяемые вещества, нанесенные у верхнего края бумаги, на разное расстояние. Отношение скорости движения растворителя к скорости движения какого-либо вещества называется коэффициентом распределения (Rf) и в стандартных условиях является величиной постоянной.
Восходящая бумажная хроматография отличается от нисходящей лишь тем, что лодочка с растворителем стоит на дне сосуда и ток растворителя движется по вертикальному листу бумаги снизу вверх. Нередко применяют двухмерную бумажную хроматографию: проведя разделение способом, например, нисходящей хроматографии, лист бумаги поворачивают на 90° и повторяют разделение, но с другими растворителями (в этом случае разделяемые вещества будут характеризоваться уже другими Rf). В результате после фиксации и окраски специфическими красителями получают хроматограммы (рис.66),
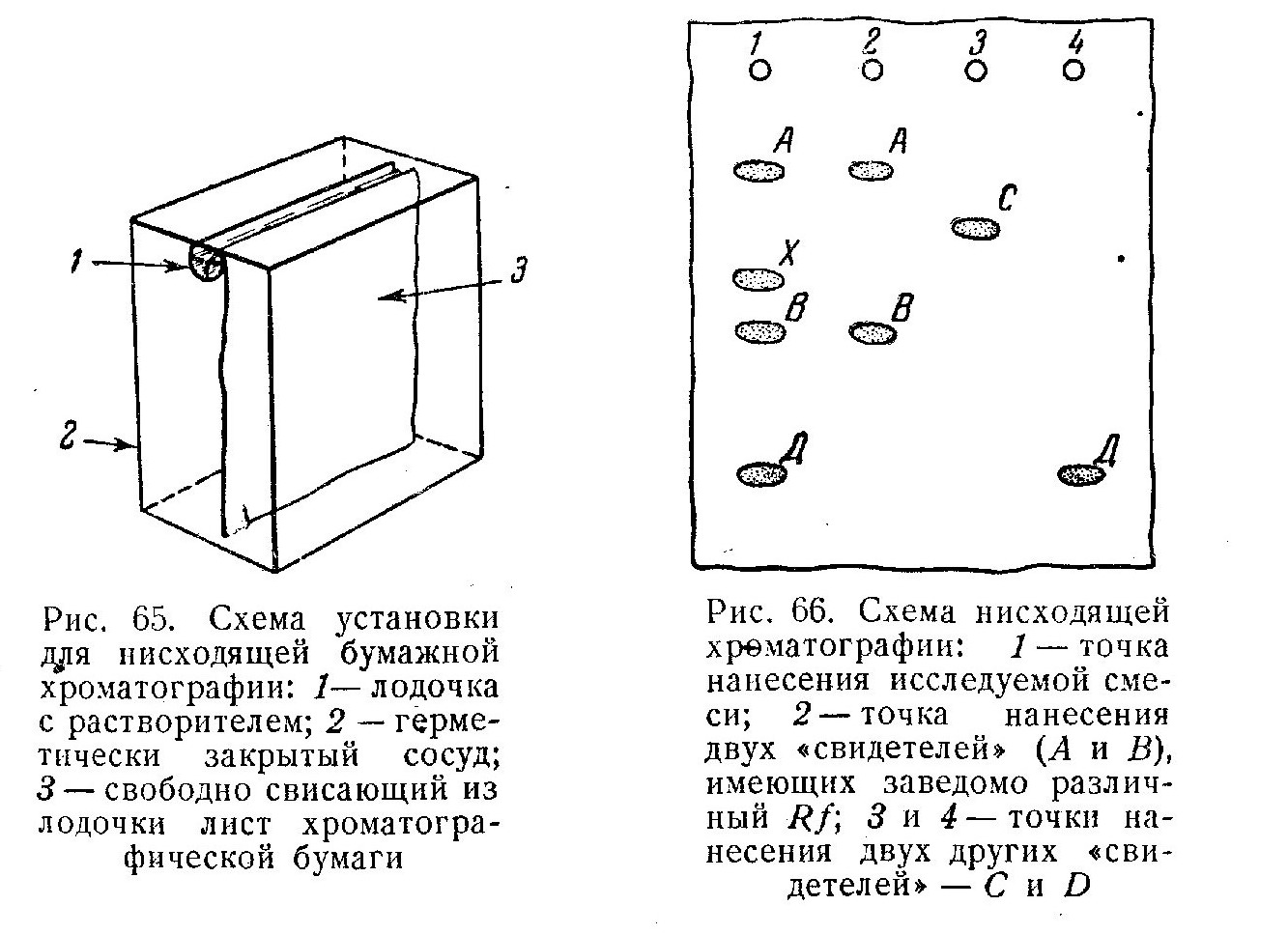
на которых пятна соответствуют каждому из разделяемых веществ. Для идентифицирования пятен обычно рядом со смесью разделяемых веществ наносят отдельно капельки чистых компонентов смеси (так называемые «свидетели»); при сравнении их расположения на хроматограмме с расположением пятен разделяемых веществ делают заключение об их тождестве. Изображенная хроматограмма показывает, что смесь состоит из веществ А, В, Д, какого-то неустановленного вещества X и не содержит вещества С.
Существует целый ряд других вариантов бумажной и распределительной хроматографии.
Менее разработаны и реже применяются другие виды хроматографического анализа:
осадочная хроматография, основанная на неодинаковой растворимости образующихся в результате химического взаимодействия осадков; при этом смесь веществ пропускают через носитель, пропитанный осадителем, т. е. веществом, реагирующим с компонентами разделяемой смеси, и термохроматография, при которой разделение веществ основано на изменении их адсорбируемости при изменении температуры.
