
- •Министерство образования и науки рф Иркутский государственный технический университет химия
- •Иркутск 2005
- •Оглавление
- •Лабораторная работа 1 основные классы неорганических соединений
- •Выполнение работы
- •Опыт 3. Взаимодействие амфотерных оксидов с кислотами и щелочами
- •Опыт 4. Получение и свойства оснований
- •Опыт 5. Получение основных солей
- •Лабораторная работа 2 определение молярной массы эквивалентов цинка
- •Выполнение работы
- •Данные опыта и результаты расчетов
- •Вычисления
- •Давление насыщенного водяного пара при различных температурах
- •Лабораторная работа 3 определение теплоты реакции нейтрализации
- •Выполнение работы
- •Вычисления
- •Лабораторная работа 4 скорость химической реакции
- •Выполнение работы
- •Опыт 1. Зависимость скорости реакции от концентрации реагирующих веществ
- •Опыт 2. Зависимость скорости реакции от температуры
- •Лабораторная работа 5 химическое равновесие и его смещение
- •Выполнение работы
- •Опыт 1. Влияние концентрации реагирующих веществ
- •На химическое равновесие
- •Для опыта удобно воспользоваться реакцией
- •Опыт 2. Влияние температуры на химическое равновесие
- •Лабораторная работа 6 реакции в растворах электролитов
- •Выполнение работы Опыт 1. Сравнение химической активности кислот
- •Лабораторная работа 7 гидролиз солей
- •Выполнение работы Опыт 1. Реакция среды в растворах различных солей
- •Опыт 2. Смещение равновесия гидролиза при разбавлении раствора
- •Опыт 3. Смещение равновесия гидролиза при изменении температуры
- •Опыт 4. Реакции обмена, сопровождаемые гидролизом
- •Лабораторная работа 8 окислительно-восстановительные реакции
- •П роцесс окисления
- •Выполнение работы
- •Опыт 1. Влияние среды на окислительно-восстановительные реакции
- •Опыт 2. Окислительно-восстановительная двойственность нитрита калия
- •Опыт 3. Реакция диспропорционирования
- •Опыт 4. Внутримолекулярная реакция
- •Лабораторная работа 9 химические свойства металлов
- •Выполнение работы Опыт 1. Взаимодействие металлов с водой
- •Опыт 2. Действие разбавленной и концентрированной серной кислоты на металлы
- •Опыт 3. Действие разбавленной и концентрированной азотной кислоты на металлы
- •Опыт 4. Действие щелочи на металлы
- •Лабораторная работа 10 электролиз
- •Выполнение работы
- •Лабораторная работа 11
- •Выполнение работы Опыт 1. Влияние образования гальванической пары на процесс растворения металла в кислоте
- •Опыт 2. Роль защитной пленки в ослаблении коррозии
- •Опыт 3. Защитные свойства металлических покрытий
- •Список литературы
Выполнение работы
Один из методов определения молярной массы эквивалентов металла основан на реакции растворения металла в избытке кислоты и измерении объема выделившегося водорода. По объему водорода вычисляют его массу, а затем молярную массу эквивалентов металла.
Определение молярной массы эквивалентов металла производится в приборе, изображенном на рисунке. Прибор состоит из трех частей: колбы А, двугорлой склянки Вульфа Б и приемника В. Отверстия двугорлой склянки закрываются резиновыми пробками, через которые проходят стеклянные трубки: короткая, оканчивающаяся сразу под пробкой, и длинная, доходящая почти до дна склянки. Короткая стеклянная трубка соединяется резиновой трубкой с колбой А, а длинная - со стеклянной трубкой Г, опущенной в приемник В.
Р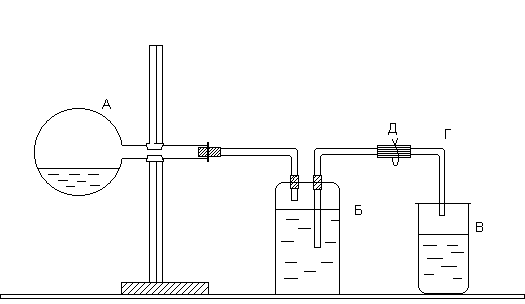 аботу
следует выполнять в следующем порядке.
Наполните водой двугорлую склянку. В
колбу налейте 10-15 мл соляной кислоты.
Закрепите колбу в горизонтальном
положении. Получите у преподавателя
навеску цинка и поместите ее в сухое
горло колбы. Закройте колбу резиновой
пробкой и проверьте герметичность
прибора. Для этого откройте зажим Д и
вдуйте воздух в прибор через стеклянную
трубку Г. В приборе создается избыточное
давление, вследствие чего вода из трубки
Г вытекает. Когда давление внутри прибора
станет равным атмосферному, вода из
трубки перестанет течь. Закройте зажим
Д. Если вода из трубки Г не уходит, прибор
герметичен. Воду из приемника вылейте
и поставьте его под трубку Г.
аботу
следует выполнять в следующем порядке.
Наполните водой двугорлую склянку. В
колбу налейте 10-15 мл соляной кислоты.
Закрепите колбу в горизонтальном
положении. Получите у преподавателя
навеску цинка и поместите ее в сухое
горло колбы. Закройте колбу резиновой
пробкой и проверьте герметичность
прибора. Для этого откройте зажим Д и
вдуйте воздух в прибор через стеклянную
трубку Г. В приборе создается избыточное
давление, вследствие чего вода из трубки
Г вытекает. Когда давление внутри прибора
станет равным атмосферному, вода из
трубки перестанет течь. Закройте зажим
Д. Если вода из трубки Г не уходит, прибор
герметичен. Воду из приемника вылейте
и поставьте его под трубку Г.
Наклоните колбу так, чтобы навеска цинка упала в кислоту, и откройте зажим. Водород, выделившийся при взаимодействии металла с кислотой, вытесняет воду из склянки Б в приемник В. Когда весь металл растворится, дайте прибору остыть, не закрывая зажима. Осторожно выньте из приемника трубку Г (следите, чтобы из нее не вылилась вода), измерьте мерным цилиндром объем воды в приемнике. Этот объем равен объему водорода, выделившегося при взаимодействии металла с кислотой. Запишите показания барометра и термометра. Исходные данные и результаты расчетов занесите в табл. 1.
Таблица 1
Данные опыта и результаты расчетов
Масса цинка m(Zn), г. |
Объем выделившегося водорода V , л |
Условия опыта |
Масса водорода m (H2), г. |
Молярная масса эквивалентов цинка |
|||
Температура Т, К |
давление атмосф. Р1, кПа |
давление водяного пара Р2, кПа |
практи- ческая МЭ,пр.(Zn), г/моль |
теорети- ческая МЭ,т. (Zn), г/моль |
|||
|
|
|
|
|
|
|
|
Вычисления
1![]() .
Вычислите массу выделившегося объема
водорода, пользуясь уравнением
Менделеева-Клапейрона:
.
Вычислите массу выделившегося объема
водорода, пользуясь уравнением
Менделеева-Клапейрона:
где P - парциальное давление водорода; V - объем выделившегося водорода; m - масса водорода; M - молярная масса водорода; Т - температура опыта; R - универсальная газовая постоянная, равная 8,314 Дж/моль·К.
В нашем опыте водород собирается над водой и потому содержит водяной пар. Общее давление газа в приборе равно атмосферному, а складывается оно из парциальных давлений водорода и водяного пара. Для вычисления парциального давления водорода нужно из величины атмосферного давления вычесть величину давления насыщенного водяного пара при температуре опыта (табл.2). Р = Р1 - Р2.
2. Зная массу металла и массу водорода, по закону эквивалентов рассчитайте молярную массу эквивалентов цинка Мэ,пр. (Zn).
3 Рассчитайте теоретическую молярную массу эквивалентов цинка Мэ,т.(Zn).
4. Вычислите относительную ошибку опыта Е:
E = (Mэ,т. - Mэ,пр.)/Mэ,т.) ∙ 100 %.
Таблица 2
