
- •Методы исследования в нейрофизиологии.
- •Структурно – функциональные особенности клеточной мембраны. Роль белков, липидов и углеводов.
- •Биохимические особенности нервной ткани.
- •Ионный состав внутриклеточной среды и среды межклеточного вещества. Мембранный потенциал.
- •Природа и значение потенциала покоя у клеток. Уравнение Нернста.
Функции нейроглии и гематоэнцефалический барьер. Нейроглия — сложный комплекс вспомогательных клеток нервной ткани: 1. Астроциты - основной элемент ГЭБ, регулирует водно-солевой обмен нервной ткани. 2. Олигодендроциты - формирует миелиновую оболочку аксонов. Отличаются высоким уровнем белкового и нуклеинового обмена; ответственны за транспорт веществ в нейроны. 3. Радиальные глиальные кл. - натянуты вдоль всей толщины спинного мозга, сетчатки, мозжечка к их поверхности, образуя продолговатые стяжи, вдоль которых развивающиеся нейроны мигрируют к своему месту назначения. 4. Эпендима - отвечает за образование и циркуляцию ликвора, а также выполняет роль барьера между кровью и ликвором. 5. Микроглия – мелкие округлые кл. в ЦНС. Выполняют роль фагоцитов, убирая омертвевшие участки нерв. ткани. 6. Шванновские кл. - аналог глиальных кл. в переф. нервах и ганглиях. Они формируют миелиновую оболочку вокруг быстро проводящих толстых аксонов, а также плотно облегают тонкие аксоны, не формируя при этом миелинового слоя. Оболочки выполняют защитную функцию. ГЭБ. 1. Проникновение веществ в мозг осуществляется главным образом не через ликворные пути, а через кровеносную систему на уровне капилляр — нервная клетка. 2. ГЭБ является в большей степени не анатомическим образованием, а функциональным понятием, характеризующим определенный физиологический механизм. Как любой существующий в организме физиологический механизм, ГЭБ находится под регулирующим влиянием нервной и гуморальной систем. 3. Среди управляющих ГЭБ факторов ведущим является уровень деятельности и метаболизма нервной ткани. ГЭБ регулирует проникновение из крови в мозг биологически активных веществ, метаболитов, химических веществ, воздействующих на чувствительные структуры мозга, препятствует поступлению в мозг чужеродных веществ, микроорганизмов, токсинов. Основная функция - проницаемость клеточной стенки. Существуют два механизма проникновения вещества в клетки мозга: через ликвор, который служит промежуточным звеном между кровью и нервной или глиальной клеткой, которая выполняет питательную функцию (ликворный путь), и через стенку капилляра. У взрослого организма основным путем движения вещества в нервные клетки является гематогенный (через стенки капилляров); ликворный путь становится вспомогательным, дополнительным. Проницаемость ГЭБ зависит от функционального состояния организма, содержания в крови медиаторов, гормонов, ионов. Повышение их концентрации в крови приводит к снижению проницаемости ГЭБ для этих веществ. Регуляция функций ГЭБ осуществляется высшими отделами ЦНС и гуморальными факторами. Значительная роль в регуляции отводится гипоталамо-гипофизарной адреналовой системе.
Ионный состав внутриклеточной среды и среды межклеточного вещества. Мембранный потенциал.
Внутренняя среда - много калия, кальция, аминокислот; мало натрия, хлора. Внешняя среда - много натрия, хлора; мало калия и аминокислот. Ионы перемещаются по градиенту концентрации оттуда, где их много, туда, где мало, т.е. ионы распределены не равномерно! Мембранный потенциал – разность зарядов между внутренними и внешними сторонами клетки.
Природа и значение потенциала покоя у клеток. Уравнение Нернста.
ПП
– мембранный потенциал возбудимой
клетки в состоянии покоя. Сущность ПП
- преобладание на внутренней стороне
мембраны отрицательных электрических
зарядов в виде анионов и недостаток
положительных электрических зарядов
в виде катионов, которые сосредотачиваются
на её наружной стороне. Внутри клетки
- "отрицательность", а снаружи -
"положительность". Первопричина
ПП – разность концентраций ионов калия
и натрия внутри и снаружи нейрона. Эту
разность создает работа особого
белка-насоса Na+-K+-АТФазы (натри-калиевый
насос). Уровень ПП (измеряется в
мВ-милиВольтах) зависит от 3-х главных
факторов: 1. Диффузии K+ из клетки. 2.
Диффузии Na+ в клетку. 3. Работы Na+/K+-АТФазы.
Уравнение
Нернста.
Выражает
зависимость электродного потенциала
от концентраций веществ, участвующих
в электродных процессах.
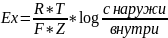 Ex – равновесный
потенциал. R - газовая постоянная.
F - число Фарадея.
T -абсолютная
температура.
Z - электровалентность
иона.
Ex – равновесный
потенциал. R - газовая постоянная.
F - число Фарадея.
T -абсолютная
температура.
Z - электровалентность
иона.
Условия возникновения ПД. Закон «все или ничего». ПД – резкий скачок мембранного потенциала возбудимой клетки в положительную сторону. Согласно закону «всё или ничего» мембрана клетки возбудимой ткани либо не отвечает на стимул совсем, либо отвечает с максимально возможной для неё на данный момент силой. Если стимул слишком слаб и порог не достигнут, ПД не возникает совсем; в то же время, пороговый стимул вызовет ПД такой же амплитуды, как и стимул, превышающий пороговый. Это отнюдь не означает, что амплитуда ПД всегда одинакова — один и тот же участок мембраны, находясь в разных состояниях, может генерировать ПД разной амплитуды. После возбуждения нейрон на некоторое время оказывается в состоянии абсолютной рефрактерности, когда никакие сигналы не могут его возбудить снова, затем входит в фазу относительной рефрактерности, когда его могут возбудить исключительно сильные сигналы (при этом амплитуда ПД будет ниже, чем обычно). Рефрактерный период возникает из-за инактивации натриевых каналов. Условием возникновения ПД является критическая деполяризация мембраны клетки. Для возникновения ПД необходимо, чтобы под влиянием какого-либо раздражителя произошло повышение ионной проницаемости мембраны возбудимой клетки. Однако, возбуждение возможно лишь при условии, если действующий на мембрану агент имеет некоторую минимальную (пороговую) величину, способную изменить мембранный потенциал до некоторого критического уровня. Порог - это когда открываются все натриевые каналы и возникает резкий скачок в положительную сторону, т.е. ПД.
Рефрактерность мембраны нейрона: причины возникновения и значение. Рефрактерность – временное снижение возбудимости одновременно с возникшим в ткани возбуждением. Рефрактерность бывает абсолютной (нет ответа ни на какой раздражитель) и относительной (возбудимость восстанавливается, и ткань отвечает только на очень сильные раздражители). Значение рефрактерности – ограничивать частоту сигналов, предохранять ткань от перевозбуждения, осуществлять ответную реакцию на биологически значимый раздражитель. Дает клетке время восстановить ПП.
Активный и пассивный ионный транспорт. Функциональная роль и механизм работы ионных каналов и насосов. Активный транспорт – это прохождение веществ через клеточную мембрану против электрохимического градиента. 1. При помощи насосов Na\K , Na\K-АТФаза, -насос-фермент обеспечивает движение ионов против градиентов концентрации через мембрану с использованием АТФ. 2. Требуется энергия АТФ. 3. Против градиента концентрации. Свойства: 1. Для обмена веществ необходим транспортный белок. 2. Это ограниченный по скорости и насыщаемый процесс. Пассивный транспорт. 1. По каналам (ионные каналы – это специализированные белки клеточной мембраны, образующие гидрофильный проход, по которому заряженные ионы могут пересекать клеточную мембрану по электрохимическому градиенту). 2. Без затрат энергии. 3. По градиентам (всегда открытые, управляемые – потенциалуправляемые и лигандуправляемые). Основной транспортной системой является насос, который вытесняет Na+ и постоянно накапливает К+.
Виды и значение ионных каналов в мембране возбудимых клеток. Ионные каналы – это специализированные белки клеточной мембраны, образующие гидрофильный проход, по которому заряженные ионы могут пересекать клеточную мембрану по электрохимическому градиенту. Ионные каналы – это пути с воротами, которые могут находиться в открытом или закрытом состоянии и регулировать скорость потока через мембрану. Состояние покоя – канал закрыт, но готов к открытию в ответ на химический или электрический импульс. Состояние активации – канал открыт и обеспечивает прохождение ионов. Состояние инактивации – канал закрыт и неспособен к активации. Главная функция ИК – обеспечивать управляемое перемещение ионов через мембрану. Функции ИК: 1. Регуляция водного обмена клетки: объём и тургор. 2. Регуляция pH: закисление и защелачивание. 3. Регуляция ионного обмена (обмен солей): изменение внутриклеточного ионного состава и концентрации. 4. Создание и изменение мембранных потенциалов: ПП; в возбудимых клетках - локальные потенциалы, ПД. 5. Проведение возбуждения в возбудимых клетках: обеспечение движения нервных импульсов. 6. Трансдукция в сенсорных рецепторах: преобразование раздражения (стимула) в возбуждение. 7. Управление активностью клетки: за счёт обеспечения потоков Са2+. ВИДЫ ионных каналов: 1. Неуправляемые: постоянно пропускают через себя ионы калия. 2. Потенциал-управляемые. Открываются при деполяризации и начинают в этих условиях пропускать через себя в клетку ионы натрия (в постсинаптических окончаниях и нервных отростках) или же ионы кальция (в пресинаптических окончаниях или рецепторных клетках). 3. Хемо-управляемые. Открываются под действием медиатора и начинают пропускать через себя в клетку ионы натрия, что вызывает деполяризацию в виде возбуждающего постсинаптического потенциала (ВПСП). 4. Стимул-управляемые. Находятся в сенсорных рецепторах (рецепторных клетках или рецепторных нервных окончаниях) и открываются под действием стимула (раздражителя), начиная пропускать через себя ионы натрия, что вызывает деполяризацию в виде рецепторного потенциала.
Типы рецепторов к медиаторам. Понятие об агонистах и антагонистах. 1. Ионные рецепторы, представляющие собой ионный канал, для открывания при лиганде. Связаны с каналами для мелких ионов (натрий, калий, хлор). Генерируют очень быстрый ответ мембраны нейрона в виде изменения в ней ионных токов. Примеры: Н-холинорецепторы, серотонин, ГАМК А, рецепторы глутамата. 2. Метаботропные – белковые структуры, запускающие ферментативные реакции внутри клетки. Активируют внутрикл. метаболич. процессы с помощью G-белка и вторичных посредников. Генерируют медленные метаболические ответы подобно действию гормонов. Примеры: М-холинорецепторы, серотонин, ГАМК В, дофаминовые и опиоидные рецепторы. Агонист – вещество, связывающееся с рецептором для медиатора, может открывать канал (действует как медиатор!). Поступают в организм извне, многие из них токсины. Антагонист – вещество противоположного действия, блокирует эффект медиатора.
Симпатический отдел (СО) ВНС и его роль в регуляции жизнедеятельности организма. Симпатические центры лежат в грудных и поясничных сегментах спинного мозга (в боковых рогах). Основным медиатором и в симпатических, и в парасимпатических ганглиях является ацетилхолин, а различия появляются только на окончаниях постганглионарных аксонов – в СО выделяется медиатор норадреналин, а в ПСО – ацетилхолин. СО активируется во время состояния по типу «борьбы или бегства», т.е. в стрессовых ситуациях для организма, когда необходимо напряжение всех систем и подготовка к реагированию. Имеет тенденцию активироваться как единое целое, вызывая диффузные генерализованные реакции по всему организму. Системные эффекты усиливаются хромаффинными клетками мозгового слоя надпочечников. Эти клетки секретируют в кровь адреналин, норадреналин, АТФ и пептиды в качестве гормонов. Адреналин, циркулирующий в крови, поддерживает и продлевает симпатическую активность. Кровеносные сосуды и потовые железы иннервируются только симпатическими нервами, за исключением кровеносных сосудов половых органов, которые иннервируются парасимпатическим отделом. Эффекты, которые будут оказывать СО и ПСО, определяются упомянутой выше принципиальной разницей в их активности. Так, при стрессе, когда особенно активна СО, она будет действовать на кровеносные сосуды, вызывая их сужение (кровеносные сосуды головного мозга расширяются под действием СО) и, как следствие, повышение артериального давления. На сердце СО действует, повышая частоту сердечных сокращений и сердечный выброс, учащает дыхание, расширяет бронхи (вентиляция легких), расширяет зрачки, тормозит работу ЖКТ, увеличивает поступление глюкозы и свободных жирных кислот в кровь (обеспечивая организм дополнительным топливом). Без СО организм может жить, просто будет плохо реагировать на стресс, а без ПСО организм не выживает.
Парасимпатический отдел (ПСО) ВНС и его роль в регуляции жизнедеятельности организма. Центры ПСО лежат в продолговатом мозге и в крестцовом отделе спинного мозга. Основным медиатором и в симпатических, и в парасимпатических ганглиях является ацетилхолин, а различия появляются только на окончаниях постганглионарных аксонов – в СО выделяется медиатор норадреналин, а в ПСО – ацетилхолин. ПСО активен в спокойном состоянии, при восстановлении сил (после принятия пищи, например). ПСО является более избирательной в своей деятельности, ее эффекты локализованы и распространяются на конкретный орган, а не на весь организм в целом. Зрачок может сужаться или расширяться без сопутствующих несвоевременных сокращений стенок мочевого пузыря или ЖКТ. Один из основных нервов ПСО – блуждающий нерв. Он выходит из продолговатого мозга, а его отростки иннервируют большую часть внутренних органов. Активация этого отдела создает организму условия для отдыха и восстановления. Она усиливает секрецию пищеварительных ферментов и усиливает моторику ЖКТ, сужает зрачки, снижает ЧСС и частоту дыхания.
Механизм распространения возбуждения по миелинизированным и немиелинизированным нервным волокнам. По миелинизированным волокнам распространение импульса происходит быстрее. Поскольку миелин - изолятор, то в участках мембраны под миелиновой оболочкой невозможны трансмембранные токи заряженных частиц. Натриевые каналы локализованы в области перехватов Ранвье. Поэтому ПД может возникать только в перехватах Ранвье. По миелинизированным участкам мембраны тоже должна происходить передача возбуждения. В этих участках деполяризация распространяется по мембране пассивным способом. Внутренняя часть нерва заполнена внутриклеточной средой, которая является достаточно хорошим проводником, т.к. содержит свободные заряженные частицы – положительно заряженные ионы металлов. В результате возникновения на мембране в области перехвата Ранвье ПД и, соответственно, разности потенциалов на соседних участках мембраны возникают токи заряженных частиц, и эти токи, распространяясь по волокну, несут с собой деполяризацию. Эти токи по мере удаления от источника тока (участок возбужденной мембраны, где наблюдается ПД и перезарядка мембраны) довольно быстро угасают (тем быстрее, чем выше сопротивление внутриклеточной среды), поэтому возбуждение может распространяться только на очень короткие расстояния. Несмотря на то, что электротон угасает по мере удаления от перехвата Ранвье, на мембрану следующего перехвата все же приходит достаточная деполяризация для того, чтобы порог возбуждения был достигнут и начались активные процессы в мембране (лавинообразное открытие натриевых каналов и т.д.), т.е. возник ПД. Дальше уже этот перехват Ранвье выступает как источник тока, электротон распространяется, угасая, по следующему миелинизированному участку и т.д. Таким образом, успешное распространение импульса по миелинизированному волокну определяется расстоянием между перехватами Ранвье (они не должны быть слишком большими, чтобы деполяризация не угасла до подпорогового уровня) и амплитудой ПД. Если по какой-то причине амплитуда ПД уменьшается (например, выключается часть натриевых каналов или изменяется состояние мембраны), а все остальное в нерве (сопротивление внутриклеточной среды, расстояние между перехватами Ранвье) остается прежним, то в следующем перехвате Ранвье ПД уже может не возникнуть, т.к. деполяризация мембраны может оказаться ниже пороговой. И дальнейшее проведение импульса по волокну прекратится.
Немиелинизированное нервное волокно. Возбужденный участок аксона характеризуется тем, что мембрана, обращенная к аксоплазме, заряжается положительно относительно экстраклеточной среды. Невозбужденные участки мембраны волокна отрицательны внутри. Между возбужденным и невозбужденным участками мембраны возникает разность потенциалов и начинает протекать ток. Линии тока, пересекающие мембрану со стороны аксоплазмы - выходящий ток, который деполяризует соседний невозбужденный участок волокна. Возбуждение движется по волокну только в одном направлении и не может пойти в другую сторону, так как после возбуждения участка волокна в нем наступает рефрактерность — зона невозбудимости. Деполяризация приводит к открыванию потенциал-зависимых натриевых каналов и в соседнем участке мембраны развивается ПД. Затем натриевый канал инактивируется и закрывается, что и приводит к зоне невозбудимости волокна. Эта последовательность событий повторяется для каждого соседнего участка волокна. На каждое такое возбуждение тратится определенное время. Скорость проведения возбуждения немиелинизированных волокон пропорциональна их диаметру: чем больше диаметр, тем выше скорость движения импульсов. Например, немиелинизированные волокна, проводящие возбуждение со скоростью 100 — 120 м/с, должны иметь диаметр около 1 мм.
Классификация нервных волокон. Факторы, определяющие скорость проведения возбуждения по аксонам. 1. группа А - самый короткий потенциал действия, самая толстая миелиновая оболочка, самая высокая скорость проведения возбуждения. а) Альфа (диаметр -13-22 мкм, скорость – 60- 120 м/с, длительность ПД- 0,4-0,5 мс). Эфферентные волокна, проводящие возбуждение к скелетным мышцам от альфа-мотонейронов. Афферентные волокна, проводящие возбуждение от мышечных рецепторов в ЦНС. б) Бета (диаметр – 8-13- мкм, скорость – 40- 70 м/с, длительность ПД – 0,4-0,6 мс). Афферентные волокна, проводящие возбуждение от рецепторов прикосновения и сухожильных рецепторов в ЦНС. в) Гамма (диаметр – 4-8 мкм, скорость – 15- 40 м/с, длительность ПД- 0,5 -0,7 мс). Эфферентные волокна к мышечным веретенам от гамма-мотонейрнов. Афферентные волокна, проводящие возбуждение от рецепторов прикосновения и давления в ЦНС. 2. группа В - миелиновая оболочка менее выражена; (диаметр – 1-3 мкм, скорость -3-14 м/с, длительность ПД- 1,2 мс). Преганглионарные волокна ВНС. 3. группа С - без миелиновой оболочки (диаметр – 0,5—1,0 мкм, скорость -0,5-2,0 м/с, длительность ПД - 2,0 мс). Постганглионарные волокна ВНС. Афферентные волокна, проводящие возбуждение от рецепторов боли, давления и тепла в ЦНС. Скорость проведения возбуждения по нервному волокну зависит от диаметра волокна, расстояния между перехватами Ранвье, амплитуды ПД, наличия миелиновой оболочки, свойств мембраны нервного волокна (плотность натриевых каналов).
Классификация медиаторов и модуляторов ЦНС. 1. Ацетилхолин. 2. Моноамины (биогенные амины). а) Катехоламины (из фенилаланина): дофамин, адреналин, норадреналин. б) Индоламины (из триптофана): серотонин. 3. Аминокислоты. а) Возбуждающие: Глутаминовая к-та (глутамат), Аспарагиновая к-та (аспартат). б) Тормозные: гамма-аминомасляная кислота (ГАМК), глицин. 4. Пуриновые: АТФ (аденозинтрифосфорная кислота), Аденозин. 5. Пептиды: вещество Р, опиоидные пептиды (энкефалины, эндорфины, динорфины), Холецистокинин, Соматостатин, Вазоактивный интестинальный полипептид (ВИП), Нейропептид Y.
Понятие о медиаторах и модуляторах (нейротрансмиттеры). Критерии (признаки) медиатора. Медиаторы способны передавать возбуждение или наводить торможение на клетку-мишень, в то время как модуляторы лишь подают сигнал к началу метаболических процессов внутри клетки. Медиаторы связываются с ионотропными молекулярными рецепторами, которые являются наружной частью ионных каналов. Медиаторы могут открывать ионные каналы и тем самым запускать трансмембранные потоки ионов. Входящие в ионные каналы положительные ионы натрия или кальция вызывают деполяризацию (возбуждение), а входящие отрицательные ионы хлора - гиперполяризацию (торможение). Ионотропные рецепторы вместе со своими каналами сосредоточены на постсинаптической мембране. Всего известно примерно 20 видов медиаторов. Критерии медиатора: 1. Вещество должно присутствовать в теле нейрона и в более высокой концентрации – в синаптическом окончании. 2. В теле или в синаптическом окончании должна существовать система синтеза и распада этого вещества. 3. Это вещество должно выделяться из синаптического окончания в синаптическую щель при естественном возбуждении или при искусственной стимуляции. 4. При введении в синаптическую щель это вещество должно оказывать точно такие же эффекты, как и при естественном высвобождении из окончания. 5. На постсинаптической мембране должны существовать специфические рецепторы для данного вещества. Модуляторы же связываются с метаботропными молекулярными рецепторами, которые сидят отдельно от ионных каналов на любом месте мембраны. С внутренней стороны мембраны к этим рецепторам присоединяются G-белки. Когда модулятор связывается с метаботропным рецептором, то G-белок активируется и запускает каскад биохимических реакций внутри клетки. Таким способом модулируется (т.е. изменяется) внутреннее состояние клетки. Модуляторов - более 600. Модуляторы являются по химическому строению нейропептидами, т.е. аминокислотными цепочками, более короткими, чем белки. Интересно, что некоторые медиаторы "по совместительству" могут играть и роль модуляторов, т.к. к ним имеются метаботропные рецепторы (серотонин и ацетилхолин). Особенности нейромодуляторов: 1. Не обладают самостоятельным физиологическим эффектом, они только модифицируют эффект медиатора. 2. Действие модулятора развивается медленнее, чем действие медиатора, но сохраняется дольше. 3. Образуются не только в нейроне, но могут также освобождаться из глиальных клеток. 4. Действие модулятора не обязательно приурочено к появлению нервного стимула. 5. Мишенью модулятора могут быть не только постсинаптические рецепторы, он может действовать на различные участки нейрона, а также влиять на внутриклеточные процессы.
Дофаминэргическая система мозга. Дофамин (ДА) – нейромедиатор, гормон, вырабатываемый мозговым веществом надпочечников и почками. По химической структуре дофамин относят к катехоламинам. Дофамин является биохимическим предшественником норадреналина и адреналина. В экстрапирамидной системе дофамин играет роль стимулирующего нейромедиатора, способствующего повышению двигательной активности, уменьшению двигательной заторможенности и скованности, снижению гипертонуса мышц. Физиологическими антагонистами дофамина в экстрапирамидной системе являются ацетилхолин и ГАМК. Дофамин является одним из химических факторов внутреннего подкрепления и служит важной частью «системы поощрения» мозга, поскольку вызывает чувство удовольствия. Недостаточность дофаминергической передачи приводит к повышенной инертности больного, которая клинически проявляется замедленностью когнитивных процессов. Данные нарушения являются наиболее типичными когнитивными симптомами болезней с дофаминергической недостаточностью — например, болезни Паркинсона. Известно несколько дофаминовых ядер, расположенных в мозге. Это дугообразное ядро, дающее свои отростки в срединное возвышение гипоталамуса. Дофаминэргические нейроны находятся преимущественно в среднем мозге, в черной субстанции среднего мозга, в гипоталамусе. 3 главных пути распространения аксонов, выделяющих ДА на окончаниях: Путь 1. Тело нейрона находится в гипоталамусе, оттуда идет короткий аксон в гипофиз. Этот путь входит в гипоталамо-гипофизарную систему регуляции деятельности желез внутренней секреции. Путь 2. Тела нейронов находятся в черной субстанции, аксоны от них идут к базальным ганглиям (полосатые тела). К этой системе относится около ¾ всего ДА ЦНС. Эта система участвует в регуляции тонических движений. Дефицит ДА в этих структурах приводит к развитию болезни Паркинсона (гибнут ДА-эргические нейроны). Путь 3. Тела нейронов лежат в среднем мозге, рядом с черной субстанцией. Аксоны от них идут в кору больших полушарий. Нарушения в этой системе могут привести к развитию шизофрении.
Ацетилхолин, его рецепторы и роль как медиатора в ПНС, ВНС и ЦНС. Ацетилхолин играет важную роль в процессах жизнедеятельности. Этот основной нейромедиатор в ВНС связан с функциями памяти, играет важную роль в засыпании и пробуждении. Рецепторы, взаимодействующие с ним, называют холинорецепторами. Различают М-холинорецепторы (мускариночувствительные) и Н-холинорецепторы (никотиночувствительнные). М- и Н-холинорецепторы находятся также в разных отделах ЦНС. Ацетилхолин не оказывает строгого избирательного действия на разновидности холинорецепторов. В той или другой степени он действует на м- и н-холинорецепторы. Ацетилхолин был первым веществом, которое было названо медиатором в ЦНС. Холинэргические нейроны обнаружены в ядрах, разбросанных по всему мозгу, и холинэргические аксоны иннервируют большинство отделов ЦНС. В ЦНС ацетилхолин выполняет функции медиатора в спинном мозге (обеспечивает возвратное торможение в клетках Реншоу); базальных ганглиях (ядро перегородки), где он участвует в регуляции движений и является функциональным антагонистом дофамина; ядрах моста (регуляция уровня бодрствования); коре больших полушарий. Холинэргическая система имеет большое значение для когнитивных процессов, обучения и памяти. Вещества, блокирующие мускариновые рецепторы, как и повреждения базальных ганглиев, нарушают процесс приобретения новых навыков и выполнение уже приобретенных форм поведения. Ингибиторы же ацетилхолинэстеразы могут улучшить выполнение задач на обучение и память и восстанавливать некоторые дефекты, возникшие вследствие повреждения базальных ганглиев. Помимо важной роли ацетилхолина в ЦНС, он также выполняет определенные функции и в других частях нервной системы. В ПНС ацетилхолин является основным медиатором нервно-мышечного синапса, действуя на никотиновые холинорецепторы. В ВНС ацетилхолин осуществляет передачу в симпатических и парасимпатических ганглиях, а также влияет на работу внутренних органов, выделяясь из периферических окончаний парасимпатических нервов (мускариновые рецепторы).
Норадренэргичекая система мозга. Сходство и различие между адреналином и норадреналином. Норадренергическая система осуществляет связь гипоталамуса со структурами продолговатого мозга и гиппокампа. Норадреналин отличается от адреналина гораздо более сильным сосудосуживающим и прессорным действием, значительно меньшим стимулирующим влиянием на сокращения сердца, слабым действием на гладкую мускулатуру бронхов и кишечника, слабым влиянием на обмен веществ. Норадреналин в меньшей степени повышает потребность миокарда и других тканей в кислороде, чем адреналин. Норадреналин принимает участие в регуляции артериального давления и периферического сосудистого сопротивления. Например, при переходе из лежачего положения в стоячее или сидячее уровень норадреналина в плазме крови в норме уже через минуту возрастает в несколько раз. Норадреналин принимает участие в реализации реакций типа «бей или беги», но в меньшей степени, чем адреналин.
Нейропептиды как медиаторы и модуляторы в ЦНС: основные представители и их функции. Нейропептиды – биологически активные соединения, участвующие в регуляции обмена веществ и поддержании гомеостаза. Это малые и средние по размеру пептиды, состоящие из 2–50 остатков аминокислот. 1. Либерины и статины (стимулируют синтез и выделение гормонов клетками передней доли гипофиза). 2. Опиоидные пептиды. В эту группу входит более 30 пептидов. Большинство из них обладает более или менее выраженным обезболивающим эффектом. Помимо обезболивающего эффекта, который является их основной функцией, опиоидные пептиды оказывают воздействие и на высшие психические функции – регулируют эмоциональное поведение (нейролептики), вызывают чувство удовлетворения, внутреннего вознаграждения. 3. Вещество Р. Это первое вещество пептидной природы, для которого были доказаны свойства медиатора. Вызывает сокращения гладкой мускулатуры. Оно содержится в телах сенсорных нейронов спинномозговых ганглиев. Является медиатором в С-волокнах (участвует в передаче болевых сигналов). Высвобождается также из синапсов на гладких мышцах внутренних органов (дыхательных путей, кровеносных сосудов, ЖКТ и т.д.). В качестве модулятора влияет на Н-холинорецепторы. Часто оно сосуществует с серотонином (угнетает его высвобождение). 4. Вазопресины и тодины (долгосрочная память). 5. Вазоактивный интестинальный полипептид (ВИП). ВИП присутствует во многих отделах НС, но больше всего его в коре б.п. и в ВНС. ВИП играет роль медиатора в постганглионарных нейронах ВНС и вызывает расслабление гладких мышц. Как модулятор ВИП подавляет высвобождение ацетилхолина, действуя на М-холинорецепторы в ЦНС и в ПНС. 6. Нейропептид Y. Особенно много в периферических нервах сердечно-сосудистой системы и в центрах ее регуляции. Для гладких мышц кровеносных сосудов характерно сосуществование нейропептида Y с норадреналином. Сам он способен оказывать прямое сосудосуживающее действие, а также стимулировать пищедобывательное поведение. Является умеренным анксиолитиком (снимает состояние тревожности).
Система опиоидных пептидов в нервной системе: рецепторы, механизм действия, связь с наркотической зависимостью. Опиоидные пептиды — группа нейропептидов, являющихся естественными лигандами к опиоидным рецепторам. Система опиоидных пептидов головного мозга играет важную роль в формировании мотиваций, эмоций, поведенческой привязанности, реакции на стресс и боль и в контроле приёма пищи. К эндогенным опиоидным пептидам относят эндорфины, энкефалины и др. Большинство из них обладает более или менее выраженным обезболивающим эффектом. Рецепторы для опиоидных пептидов были обнаружены при изучении действия природных опиатов (опиума, морфина, героина, кодеина). Помимо обезболивающего эффекта, который является их основной функцией, опиоидные пептиды оказывают воздействие и на высшие психические функции – регулируют эмоциональное поведение (нейролептики), вызывают чувство удовлетворения, внутреннего вознаграждения. Большая часть опиоидов образуется в гипофизе, часть – в надпочечниках. Под влиянием морфина тормозятся таламические центры боли и прекращается передача болевых сигналов к коре. Наиболее высокая плотность опиатных рецепторов обнаружена в лимбической системе (связь с эмоциональными реакциями). Опиоиды уменьшают кол-во выдел. в-ва Р, которое отв. за болевые ощущения.
Серотонинэргичекая система мозга. Серотонинергическая система, образованная нейронами, тела которых лежат в ядрах шва продолговатого мозга, тормозит восходящие активирующие системы мозга и тем самым снижает их эффект по активации больших полушарий головного мозга. Система даёт тормозный, успокаивающий эффект. Является составной частью нейрональных сетей, обеспечивающих регуляцию эмоционального состояния и настроения. Серотонин - медиатор, выполняющий функцию вещества-посредника, через которое между нейронами передается импульс. Относится к классу индоламинов. Метаболизируется из триптофана, в основном в ЖКТ (95%) и стволе мозга. Снижение уровня серотонина повышает чувствительность болевой системы организма, влияет на интенсивность мозгового кровотока. Самая высокая концентрация серотанина в ЦНС - эпифиз. Там он превращается в мелатонин, участвует в регуляции цикла сон-бодрствование. Серотонин также участвует в регуляции сенсорных потоков (торможение) и работе антиноцицептивной системы. Антагонистом является ЛСД. С нарушением функции серотонинергической системы связывают развитие психических нарушений, проявляющихся депрессией и тревогой. Снижение серотонинергической функции у животных и человека усиливает агрессивное поведение и импульсивность, тогда как повышение серотонинергической активности уменьшает такие проявления.
Возбуждающие медиаторы-аминокислоты. Типы рецепторов к глутамату и кратковременная память. Глютаминовая кислота - основной возбуждающий медиатор в головном мозге. Глутамат образуется в мозге из глюкозы. Больше всего глутамата в конечном мозге и в мозжечке. Это один из самых распространенных медиаторов в ЦНС. Существует три типа рецепторов к глутамату, при взаимодействии с которыми открываются каналы для натрия, калия или кальция. Один из типов рецепторов к глутамату (NMDA-рецепторы) имеют непосредственное отношение к обучению и памяти. Этот медиатор принимает участие во многих центральных процессах, в том числе и в процессах памяти. Глутамат способствует стабилизации содержания в клетках ионов калия, а также связывает аммиак, образующийся в результате метаболических процессов и являющийся ядовитым для организма веществом. Аспарагиновая кислота. Больше аспарагиновой кислоты в среднем мозге и в сером веществе спинного мозга. Аспарагиновая кислота регулирует спинномозговые рефлексы, участвует в выработке двигательных навыков. Обе возбуждающие аминокислоты предположительно участвуют в регуляции состояния беспокойства. Обнаружено накопление глутамата и аспартата в нервной ткани при ишемии головного мозга.
Тормозные медиаторы-аминокислоты. Гамма-аминомасляная кислота (ГАМК). Этот медиатор образуется из глютаминовой кислоты. Это один из самых распространенных тормозных медиаторов в ЦНС (обнаруживается примерно в 50% нервных окончаний). Много ГАМК в коре б.п., в коре мозжечка, в черной субстанции среднего мозга. Существует два типа рецепторов к гамма-аминомасляной кислоте – ГАМК-А (каналы для хлора) и ГАМК-Б (метаботропные рецепторы). В составе ГАМК-А рецептора есть место для связывания бензодиазепинов (малые транквилизаторы). Бензодиазепины, связываясь с рецептором ГАМК, усиливают ее эффект на собственный рецептор, таким образом усиливая тормозные процессы в ЦНС. Такие рецепторы встречаются в коре б.п. и в гиппокампе. Нарушения в ГАМК-эргической системе мозга связывают с развитием эпилепсии, расстройства сна, дисфункциями в деятельности сердечно-сосудистой системы. Глицин. Простейшая аминокислота, являющаяся распространенным тормозным медиатором спинного и головного мозга. Тела нейронов, синтезирующих глицин, находятся в спинном и продолговатом мозге (в ретикулярной формации), а также в промежуточном мозге. У глицина есть только ионотропный тип рецепторов (канал для ионов хлора). Глицин обеспечивает возвратное торможение мотонейронов спинного мозга, уменьшает психомоторную расторможенность.
Электрические и химические синапсы: их строение и функции. По механизму передачи сигнала. Электрические синапсы – довольно плотные контакты между клетками (синаптическая щель - 2 нм), благодаря чему нервный импульс перескакивает с пресинаптической на постсинаптическую мембрану. Дополнительно в электрическом синапсе между пре- и постсинаптической мембранами существуют мостики, представляющие собой каналы, через которые могут проходить мелкие молекулы и ионы. Благодаря таким каналам не происходит потеря сигнала в результате утечки электрического тока через внеклеточную среду. Вследствие этого изменения потенциала в пресинаптическом окончании могут передаваться на постсинаптическую мембрану практически без потерь. Электрические синапсы были обнаружены в самых разных отделах НС беспозвоночных и низших позвоночных животных. Проведение возбуждения в таких синапсах осуществляется быстро, с небольшой задержкой или даже практически без задержки. В этих синапсах ток возможен в обоих направлениях, но иногда сопротивление в одном из направлений выше, чем в другом. Электрические синапсы позволяют синхронизировать активность групп нейронов, они дают возможность получать постоянные, стереотипные реакции при многократных воздействиях, т.к. они в меньшей степени, чем химические синапсы, подвержены метаболическим и прочим влияниям. Механизм работы химического синапса. Поскольку синаптическая щель в химическом синапсе имеет довольно большие размеры, для эффективной передачи импульса к следующей клетке необходим механизм усиления. Это наличие химического вещества – медиатора (посредника). Медиатор в синапсе содержится в специальных пузырьках – везикулах, а не просто растворен в цитоплазме. Пузырьки формируются путем впячивания мембраны пресинаптического окончания. Бывают пузырьки окаймленные и гладкие. Если медиатора выделилось достаточно много, то амплитуда ПКП достигнет порогового значения и разовьется ПД мышечной клетки. Результатом ПД мышечной клетки является сокращение мышечных волокон.
Процессы, происходящие в нервно-мышечном синапсе. Поскольку синаптическая щель в химическом синапсе имеет довольно большие размеры, для эффективной передачи импульса к следующей клетке необходим механизм усиления. Это наличие химического вещества – медиатора. В случае с концевой пластинкой этим медиатором является вещество ацетилхолин. Медиатор в синапсе содержится в специальных пузырьках – везикулах, а не просто растворен в цитоплазме. Пузырьки формируются путем впячивания мембраны пресинаптического окончания. Ацетилхолин синтезируется в самом окончании, а не в теле клетки. Там находится ферментативная система синтеза этого вещества. Процессы, происходящие в синапсе, которые приводят к появлению ПКП и в результате – к мышечному сокращению. По нервному волокну к окончанию приходит ПД (возбуждение) и начинается деполяризация пресинаптической мембраны. В это время меняется заряд на мембране (внутренняя сторона меняет знак с отрицательного на положительный) и запускается высвобождение ионов Са++. Эти процессы приводят к тому, что пузырьки с медиатором начинают в большом количестве подходить к пресинаптической мембране и встраиваться в нее, в результате чего ацетилхолин выходит в синаптическую щель. Далее ацетилхолин двигается к постсинаптической мембране, т.е. уже к мембране мышечной клетки. На постсинаптической мембране имеются специальные белковые образования – рецепторы, с которыми ацетилхолин и связывается. Холинорецепторы представляют собой структуры, связанные с ионными каналами, поэтому при связывании медиатора со своим рецептором происходит открывание канала для какого-либо иона. В случае с ацетилхолином – это каналы для натрия и калия. Возникает ток ионов натрия внутрь клетки и деполяризация мембраны мышечной клетки. Если ток и, следовательно, деполяризации достаточно сильные, то возникнет ПД в мышечной клетке. Для нормальной работы синапса, в частности для обеспечения передачи параметров (частоты и паттерна) приходящей к синапсу информации, необходимо, чтобы медиатор достаточно быстро удалялся с постсинаптических рецепторов, т.е. из синаптической щели. Это обеспечивается, помимо незначительной утечки медиатора из области синаптической щели, прежде всего двумя механизмами. Во-первых, это ферментативная инактивация медиатора путем расщепления его активной молекулы на неактивные метаболиты. В нервно-мышечном синапсе эту функцию в синаптической щели выполняет фермент ацетилхолинэстераза, которая расщепляет ацетилхолин на составные элементы – холин и уксусную кислоту (ацетат). Вторым способом устранения медиатора из щели является обратный захват медиатора, когда его молекулы поступают в пресинаптическое окончание. Так происходит, например, в норадренэргических синапсах как в ЦНС, так и на периферии (в составе СВНС). Это обеспечивает не только устранение активного вещества из щели, но и более экономное расходование медиатора в синапсе. В случае концевой пластинки обратному захвату подвергается не сам ацетилхолин, а образующийся при его распаде холин, который в дальнейшем снова используется в синаптическом окончании для синтеза ацетилхолина. Для синтеза нового ацетилхолина в окончании аксона существует другой фермент – ацетилхолинтрансфераза.
Постсинаптические потенциалы, их отличие от ПД. Суммация в ЦНС. Возникновение ПСП - локальное изменение мембранного потенциала при действии медиатора. ПСП могут быть двух типов: 1. Деполяризующие (возбуждающие, ВПСП). 2. Гиперполяризующие (тормозные, ТПСП). ВПСП обусловлены суммарным входящим током положительных зарядов внутрь клетки. Такой ток может возникнуть в результате повышения проводимости мембраны для натрия, калия и, возможно, других ионов, например, кальция. В результате мембранный потенциал смещается по направлению к нулю (становится менее отрицательным). Фактически величина ВПСП зависит от того, какие ионы переместились через мембрану и каково соотношение проницаемостей для этих ионов. Перемещения различных ионов происходят одновременно, и их интенсивность зависит от количества выделившегося медиатора. ВПСП необходим для генерации нервного импульса (ПД). Это происходит в том случае, если ВПСП достигнет порогового значения. После этого процессы становятся необратимыми, и возникает ПД. Если в мембране открываются каналы, обеспечивающие суммарный выходящий ток положительных зарядов (ионов калия) или входящий ток отрицательных зарядов (ионов хлора), то в клетке развивается ТПСП. В качестве медиаторов, вызывающих ТПСП, обнаружены глицин и гамма-аминомасляная кислота (ГАМК); их рецепторы связаны с каналами для хлора, и при взаимодействии этих медиаторов со своими рецепторами происходит движение ионов хлора внутрь клетки и увеличение мембранного потенциала. Этот процесс называется постсинаптическое торможение. ПСП представляют собой градуальные реакции (их амплитуда зависит от количества выделившегося медиатора или силы стимула). Этим они отличаются от ПД, который подчиняется закону «все или ничего». Суммация. Бывает временной и пространственной. Временная - объединение эффектов стимулов, пришедших по одному каналу с большой частотой. Пространственная - наложение друг на друга ВПСП от соседних синапсов, расположенных относительно близко друг от друга на мембране клетки.
Пресинаптическое и постсинаптическое торможение. Прямое химическое синаптическое торможение происходит при активации каналов для отрицательно заряженных ионов хлора. Стимуляция тормозных входов вызывает небольшую гиперполяризацию клетки – ТПСП. В качестве медиаторов, вызывающих ТПСП, обнаружены глицин и гамма-аминомасляная кислота (ГАМК); их рецепторы связаны с каналами для хлора, и при взаимодействии этих медиаторов со своими рецепторами происходит движение ионов хлора внутрь клетки и увеличение мембранного потенциала (до -90 или -100 мВ). Этот процесс называется постсинаптическое торможение. В результате пресинаптического торможения происходит уменьшение высвобождения медиатора из возбуждающих окончаний. При пресинаптическом торможении тормозные аксоны устанавливают синаптический контакт с окончаниями возбуждающих аксонов. В качестве медиатора пресинаптического торможения чаще всего встречается ГАМК, реже опиоидные пептиды. В результате действия ГАМК на пресинаптическое окончание также происходит значительное увеличение проводимости для хлора и в результате снижение амплитуды ПД в пресинаптическом окончании. Функциональное значение этих двух видов торможений в ЦНС сильно различается. Постсинаптическое торможение уменьшает возбудимость всей клетки в целом, делая ее менее чувствительной ко всем возбуждающим входам. Пресинаптическое торможение гораздо более специфично и избирательно. Оно направлено на определенный вход, давая возможность клетке интегрировать информацию из других входов.
Функции спинного мозга. Спинной мозг – наиболее просто организованный отдел ЦНС, осуществляющий рефлекторную и проводниковую функции. Проводниковая функция заключается в проведении сигналов от рецепторов и мышц вверх, к высшим отделам головного мозга, а рефлекторная – в осуществлении рефлексов. Помимо этих двух функций, в спинном мозге расположены центры ВНС. В грудном, верхнепоясничном и крестцовом отделах спинного мозга серое вещество образует боковые рога, в которых располагаются тела первых (преганглионарных) вегетативных нейронов.
Функции продолговатого мозга. 1. Проводниковая. 2. Рефлекторная. Рефлексы, осуществляемые с помощью продолговатого мозга: а) вегетативные рефлексы блуждающего нерва (регуляция работы внутренних органов); вегетативная регуляция выделения слюны; рефлексы также бывают двигательными и секреторными. б) соматические рефлексы: пищевые, защитные (рвота, кашель, чихание), рефлексы поддерживания позы (статические рефлексы - направление на изменение тонуса скелетных мышц при изменении положения головы в пространстве; статокинетические рефлексы - обеспечение сохранение позы при изменении скорости его линейного перемещения в пространстве или вращения). в) рефлексы реализации сенсорных функций - обеспечение кожной, слуховой, вкусовой чувствительности.
Функции среднего мозга. Средний мозг образован четверохолмием и ножками мозга. На уровне среднего мозга располагаются ядра глазодвигательного и блокового черепно-мозговых нервов, а также сенсорное ядро тройничного нерва. Ядро глазодвигательного нерва располагается на уровне верхних бугров четверохолмия и иннервирует мышцы глаза, мышцу, поднимающую веко, а также в его составе есть парасимпатическая ветвь, которая иннервирует сфинктер зрачка (приводит к сужению зрачка). Ядро блокового нерва находится на уровне нижних бугров четверохолмия, а сам нерв иннервирует верхнюю косую мышцу глаза. Четверохолмие среднего мозга является важным сенсорным отделом ствола головного мозга. Передние бугры являются первичными зрительными центрами, а задние – первичными слуховыми центрами. Через них проходят и частично обрабатываются сигналы от соответствующих рецепторов. Эти центры также принимают участие в осуществлении ориентировочных рефлексов либо на зрительные, либо на звуковые раздражители. Передние бугры участвуют в рефлексах аккомодации глаза (фокусировка на объекты), в зрачковых реакциях. В крыше среднего мозга локализована нейронная сеть, вычисляющая скорость и направление движения объекта в поле зрения. Кроме того, в среднем мозге находятся ядра, нейроны которых осуществляют синтез некоторых медиаторов из группы моноаминов: а) ядра шва – синтез серотонина, являются частью антиноцицептивной системы; б) голубое пятно – синтез норадреналина; в) черная субстанция – синтез дофамина. В среднем мозге находится красное ядро – важный центр регуляции моторных функций. Оно является элементом экстрапирамидной системы контроля движений.
Ретикулярная формация ствола мозга. Особенности строения и функции. РФ ствола представляет собой массу клеток, лежащую в средней части мозгового ствола от нижних отделов продолговатого мозга до промежуточного. Четких границ она не имеет. Для ретикулярной формации характерны полисинаптические нейронные цепи, образованные нейронами с короткими аксонами, а также множество ответвлений от одного аксона. Благодаря этим особенностям под прямым влиянием одного нейрона РФ оказывается около 30 тыс. других ретикулярных нейронов. В этой структуре все нейроны связаны со всеми и образуют сетчатую структуру. Еще одной особенностью нейронов РФ является их полимодальность, т.е. способность одного и того же нейрона отвечать на разные стимулы (звук, свет, тактильные раздражители). Благодаря этому свойству в РФ происходит взаимодействие сигналов от разных рецепторов. 1. Влияние РФ на двигательные функции. На мотонейроны спинного мозга РФ может оказывать как возбуждающее, так и тормозное действие. Электрическая стимуляция обширной области РФ приводит к ритмическим движениям и тремору. Обычно эти эффекты довольно длительны, сохраняются даже дольше, чем само электрическое раздражение. 2. Влияния РФ на кору б.п. были открыты после экспериментов Ф. Бремера с перерезкой головного мозга на разных уровнях. У кошки он делал перерезку восходящих путей на уровне между спинным и продолговатым мозгом. В результате такой операции животное оставалось бодрствующим и реагировало на разные раздражители. Если же перерезку осуществляли на уровне среднего мозга (между передними и задними буграми четверохолмия), то животное оставалось спящим и на стимулы не реагировало. Был сделан вывод о том, что именно из РФ на кору идут восходящие активирующие влияния, которые поддерживают ее в активном состоянии, поскольку в первом случае пути от РФ в кору были сохранены, а во втором случае большая часть РФ оказывалась ниже места перерезки, и ее связь с корой была нарушена.
Функции мозжечка. Корректирует и дополняет деятельность других двигательных центров. Участвует в регуляции позы и мышечного тонуса, в координации и исправлении медленных движений и рефлексов поддержания позы, в коррекции быстрых целенаправленных движений, которые формируются двигательными областями коры б.п. Червь мозжечка получает информацию от соматосенсорной системы и оказывает влияние на вестибулярное ядро и на РФ ствола мозга. Червь связан со стволовыми центрами, отвечающими за регуляцию позы, управляет тонусом, поддерживающими движениями и равновесием тела. Промежуточная часть мозжечка принимает сигналы от соматосенсорной системы и двигательной коры б.п., передает информацию к красному ядру среднего мозга через вставочное ядро. К этой части мозжечка информация о готовящемся движении поступает заранее, еще до его совершения. Промежуточная часть участвует во взаимной координации движений и в коррекции выполняющихся движений в процессе их выполнения. Подобная коррекция нужна для осуществления не до конца заученных движений или тех, которые выполняются редко. Полушария мозжечка получают сигналы от всех областей коры б.п. Эти пути от коры переключаются в ядрах моста. По ним передается информация о замысле движения. В полушариях и в зубчатом ядре эта информация преобразуется в конкретную программу движения. Программа движения из полушарий мозжечка через ядра таламуса передается в двигательную область коры б.п. И только после этого сигналы о движении из моторной коры посылаются по спинному мозгу к мышцам, и движение выполняется. Каждая половина мозжечка управляет преимущественно соответствующей половиной тела. Особенностью деятельности коры мозжечка является то, что все клетки коры мозжечка, за исключением клеток-зерен, являются тормозными. Ни в одном другом отделе ЦНС нет такого преобладания торможения над возбуждением.
Функции таламуса. Таламус – массивное парное образование, содержащее около 120 ядер серого вещества. Деятельность тесно связана с анализом афферентных сигналов, с регуляцией функционального состояния организма. Определяет зону коры, к которой идет сигнал. От таламуса зависит, какая информация пойдет в мозг. Таламус - высший центр болевой чувствительности. Он осуществляет анализ болевых сигналов и организует болевые ответные реакции. Импульсы, идущие к нейронам таламуса от поврежденных участков тела, активируют эти нейроны и вызывают болевые ощущения. Таламус включает в себя собственно зрительный бугор, затем метаталамус и подушку. По функциональной роли в деятельности НС в таламусе выделяют следующие ядра: 1. Специфические. Ядра имеют локальную проекцию в строго определенные зоны коры. Основную массу клеток составляют переключательные клетки. Раздражение какой-либо рецепторной области сначала вызывает в соответствующем специфическом ядре ответную реакцию в виде потенциала. Затем раздражение самого ядра вызывает ответную реакцию в определенной корковой зоне. В каждом ядре выражена топическая организация, т.е. каждому участку кожи, сетчатки и т.д. соответствует определенная зона таламуса. Специфические ядра представляют собой важнейшую часть основных сенсорных и моторных систем, а разрушение переключательных ядер приводит к полной и необратимой потере соответствующей чувствительности или нарушениям движений. 2. Неспецифические. Не относятся к определенной сенсорной или моторной системе, морфологически и функционально они связаны со многими системами и участвуют вместе с РФ в осуществлении неспецифических функций. Нейронные сети этих ядер имеют ретикулярное строение: густая сеть нейронов с длинными слабо ветвящимися дендритами. Оказывают на кору модулирующее влияние, т.е. регулируют ее функциональное состояние. Так же как и в случае с РФ, деятельность неспецифической таламической системы тесно связана с механизмами развития сна, саморегуляции функционального состояния и ВНД. Неспецифическая система усиливает специфическую, а специфическая подавляет неспецифическую. 3. Ассоциативные. Ассоциативные ядра обеспечивают взаимодействие таламических ядер и различных корковых полей и в определенной степени совместную работу больших полушарий мозга. Ассоциативные ядра проецируются не только на ассоциативные области коры, но и на специфические проекционные поля. Кора головного мозга посылает волокна к ассоциативным таламическим ядрам, осуществляя регуляцию их деятельности. Кроме передачи проекционных влияний на кору, нейроны таламуса сами могут осуществлять замыкание рефлекторных путей без участия коры и таким образом осуществлять самостоятельно сложные рефлекторные функции.
Функции гипоталамуса. Гиппоталамус - центр нейрогумаральной регуляции. Расположен под таламусом. Четких границ он не имеет. Является центральным отделом промежуточного мозга. Гипоталамус регулирует все процессы, необходимые для поддержания гомеостаза. Он служит важным интегративным центром для соматических, вегетативных и эндокринных функций. Нервная регуляция - нервный импульс идет по аксону к нужному органу. Гуморальная регуляция - при помощи веществ, содержащихся в организме. Латеральный гипоталамус получает информацию от нервных структур. В медиальной части гипоталамуса располагаются особые нейроны, которые реагируют на состав крови и спинномозговой жидкости и образуют несколько важнейших центров. 1. Центр голода и насыщения. Регулирует сложное пищевое поведение. Нейроны центра голода - глюкорецепторы, которые активизируются при снижении в крови концентрации глюкозы и других питательных веществ (аминокислот, жирных кислот), а нейроны центра насыщения – наоборот, активируются при повышении содержания этих веществ в крови. 2. Центр жажды и ее удовлетворения. Стимуляция структур ведет к резкому увеличению потребления жидкости, а разрушение этих структур – к полному отказу от воды. Нейроны центра жажды реагируют на изменение осмотического давления (при недостатке воды осмотическое давление крови повышается, что вызывает активацию нейронов гипоталамуса). 3. Центр терморегуляции. Нейроны - терморецепторы, реагирующие на температуру омывающей их крови. Раздражение задней группы ядер приводит к повышению температуры тела в результате повышения теплопродукции за счет усиления обменных процессов и дрожания скелетной мускулатуры. Стимуляция паравентрикулярных ядер приводит к снижению температуры за счет усиления потоотделения, расширения просвета кожных сосудов, а также торможения дрожания мускулатуры. 4. Центр полового поведения. Участвует в регуляции комплекса функций, связанных с размножением. Изолированное разрушение области серого бугра ведет к атрофии половых желез, а при опухоли этой зоны часто наблюдается ускоренное половое созревание. Описаны случаи превращения мужских половых признаков в женские при повреждениях средних областей гипоталамуса. 5. Центр агрессии, ярости и центр удовольствия. Центр удовольствия, локализованный в заднем гипоталамусе, взаимодействуя с другими структурами лимбической системы, участвует в организации эмоциональной сферы и полового поведения. При раздражении же структур переднего гипоталамуса у животных возникают реакции страха и ярости. 6. Центр регуляции цикла сон-бодрствование. Раздражение латеральной части базальной преоптической области у животных вызывает сон и сопутствующие ему изменения биоэлектрической активности головного мозга. У людей поражения гипоталамуса часто сопровождается нарушениями сна и изменениями ЭЭГ, характерными для сна. Супрахиазматическое ядро гипоталамуса – важнейшее звено в организации биоритмов, центрального механизма «биологических часов», организующих суточные циклы.
Гипоталамо-гипофизарная система. Общий принцип действия. Единый комплекс, объединяющий часть гипоталамуса и переднюю долю гипофиза, регулирует деятельность эндокринных желез. ГГС обеспечивает переключение нервных импульсов на эндокринную регуляцию функций, т.е. является центральным звеном нейро-гуморальной регуляции деятельности организма. Гипоталамус синтезирует и выделяет нейрогормоны, которые попадают к аденогипофизу. Среди них выделяют статины и либерины. Статины оказывают тормозное действие на деятельность гипофиза, а либерины – активирующее. Под действием этих факторов гипофиз либо выделяет (либерины), либо снижает выделение (статины) тропных гормонов. Для тропных гормонов гипофиза существуют статины и/или либерины в гипоталамусе. Не для всех гормонов аденогипофиза выявлены соответствующие статины. Регуляция деятельности ГГС осуществляется по принципу отрицательной обратной связи. Суть этой регуляции заключается в том, что при повышении в плазме крови содержания гормонов периферических эндокринных желез уменьшается выброс соответствующего нейрогормона гипоталамуса и тропного гормона гипофиза. Такая регуляция действует даже в отсутствии влияний со стороны ЦНС, ЦНС нужна только для приспособления этой системы к потребностям организма.
Гипофиз и его гормоны. Железа внутренней секреции, играющая ведущую роль в гормональной регуляции. Гормоны: вазопрессин - повышает всасываемость воды из мочи (препятствует диурезу), окситоцин – действует на гладкомышечные стенки матки и протоков молочных желез и семенников. Расположен гипофиз в турецком седле основной кости черепа и как бы висит на ножке под гипоталамусом. В нем различают переднюю долю (аденогипофиз) и заднюю долю (нейрогипофиз). Обильно снабжается кровью. Соматолиберин, соматостатин и гормон роста (соматотропин). Соматолиберин стимулирует выработку аденогипофизом гормона роста, а соматостатин – тормозит. Гипогликемия (снижение уровня глюкозы в крови) и введение аминокислот стимулируют секрецию соматолиберина и соматотропина. Влияние соматотропина на рост объясняется тем, что он усиливает синтез белка и стимулирует клеточное деление в разных тканях, в том числе в костях, что обеспечивает их рост в длину. Гормон роста создает хорошие условия для проникновения аминокислот через клеточную мембрану, усиливает процесс включения аминокислот в белки цитоплазмы клеток костной ткани, печени, почек, стимулирует синтез РНК. Недостаточность продукции соматотропина в детском возрасте приводит к развитию гипофизарной карликовости. При этом заболевании рост мужчин составляет менее 130 см, женщин – менее 120 см, у взрослых сохраняются пропорции тела 4–5-летнего ребенка с недоразвитием вторичных половых признаков. Из-за нарушений синтеза белка соединительной ткани кожа сухая, дряблая, морщинистая, что придает старческий вид даже лицу ребенка. Однако умственное развитие таких людей вполне нормально. Проявление повышенной секреции соматотропина в детском возрасте приводит к гипофизарному гигантизму. Рост таких людей превышает 200 см, они имеют длинные конечности, недостаточность половых функций, пониженную физическую выносливость. Кортиколиберин и кортикотропин. Синтезируется ядрами гипоталамуса. Действие проявляется в стимуляции роста коры надпочечников и секреции глюкокортикоидов и андрогенов, поэтому длительное их введение приводит к гипертрофии коры надпочечников. Стимулирует распад жиров, выход в кровь свободных жирных кислот. Тиреолиберин и тиреотропин. Его секреция активируется норадреналином, а тормозится серотонином. Выделение усиливается при понижении температуры окружающей среды. Под его влиянием происходит усиление роста ткани щитовидной железы, захвата клетками щитовидки йода, йодирование тирозина (образование гормонов щитовидки).
Периферические железы внутренней секреции, их гормоны и функциональная роль в организме. К эндокринным железам относятся органы, не имеющие протоков и выделяющие гормоны в кровь. Также к ним относят две центральные железы – гипофиз и эпифиз. Щитовидная железа. 2 йодированных гормона – тироксин и трийодтиронин, а также кальцитонин. Синтез йодированных гормонов связан с поступлением в организм неорганического йода, который человек и животные получают с пищей и водой. Тироксин и трийодтиронин стимулируют процессы обмена веществ и энергии, участвуют в терморегуляции (усиливают теплопродукцию, повышают потребление кислорода некоторыми органами и тканями). Большие дозы гормонов усиливают распад белка (катаболический эффект), а малые дозы, особенно во время роста и развития организма, необходимы для синтеза белка (анаболический эффект). При нехватке - снижается основной обмен, кожа теряет эластичные свойства, волосяной покров редеет, замедляется работа сердца, появляется медлительность в двигательных актах и мыслительной деятельности, нарушается терморегуляция (плохо переносится охлаждение), снижается аппетит, но при этом увеличивается вес. При избытке - основной обмен усиливается, возникает учащенное сердцебиение, повышается артериальное давление, появляется бессонница, нервозность, аппетит повышается, а вес снижается. Кальцитонин снижает уровень кальция в крови. Под его действием усиливается деятельность клеток, участвующих в формировании костной ткани. Поджелудочная железа. Железа смешанной секреции – часть ее выделяет панкреатический сок (внешняя секреция), а часть синтезирует и выделяет два основных гормона – инсулин и глюкагон. Инсулин – единственный гормон в организме, понижающий содержание глюкозы в крови. Он усиливает утилизацию глюкозы мышцами, печенью, жировой тканью, стимулирует отложение гликогена в печени. В скелетных мышцах и в сердечной мышце способствует накоплению АТФ, усиливая их энергетический потенциал. Высокий уровень глюкозы крови является одним из источников части болезненных проявлений диабета. Глюкагон необходим для регуляции углеводного обмена. Под его воздействием происходит расщепление гликогена в печени и высвобождение глюкозы в кровь, т.е. он является антагонистом инсулина. Глюкагон также стимулирует распад жира в жировой ткани с высвобождением свободных жирных кислот в кровь. Надпочечники – парные органы, располагающиеся у человека над почками. Состоят из двух разнородных компонентов – коркового слоя и мозгового слоя. Исходным субстратом для синтеза гормонов коры надпочечников является холестерин. К гормонам мозгового слоя надпочечников относятся адреналин и норадреналин (катехоламины). Адреналин способствует мобилизации энергетических ресурсов организма, что особенно важно при стрессовых реакциях. Вызывает быструю перестройку функций организма, направленную на повышение его работоспособности. Кора надпочечников. 1. Глюкокортикоиды – гормоны, влияющие преимущественно на углеводный обмен. Под их влиянием происходит усиленное новообразование углеводов из других соединений (продукты распада белка). После введения глюкокортикоидов значительно уменьшаются лимфатические узлы, меняется соотношение клеток крови, связанных с иммунитетом, подавляется иммунитет. Это свойство позволяет использовать эти гормоны при пересадке органов и тканей для избежания их отторжения. 2. Минералокортикоиды. Жизненно важные гормоны, регулирующие минеральный и водный обмен. Основной минералокортикоид – альдостерон. Он присутствует у всех животных, кроме обитающих в море. Действует на некоторые отделы почек, где под его влиянием усиливается обратное всасывание натрия и уменьшается обратное всасывание калия. При усиленной секреции альдостерона повышается осмотическое давление крови, лимфы, тканевой жидкости, в результате чего в организме накапливается вода и повышается артериальное давление. 3. Половые стероиды. Андрогены надпочечников противодействуют материнским эстрогенам во время внутриутробного развития плода. Эстрогены выделяются надпочечниками в небольших количествах, и их роль по сравнению с одноименными гормонами яичников невелика. Половые гормоны надпочечников наибольшую роль играют в детском и старческом возрасте, в те периоды онтогенеза, когда внутрисекреторная функция половых желез незначительна. Половые железы. Парные органы, в мужском организме - семенники, в женском – яичники. Основным гормоном семенников является тестостерон. Он влияет на формирование мужских половых органов и вторичных половых признаков: рост бороды, оволосение по мужскому типу, строение скелета и гортани. Андрогены оказывают анаболический эффект – под их влиянием усиливается синтез белка в разных органах, но особенно в скелетных мышцах. Гормоны необходимы для первых проявлений половых признаков и функций и определяют агрессивность самцов животных. Основным женским половым гормоном является эстроген. Значение – создание такого состояния половых путей самки, которое благоприятствует оплодотворению яйцеклетки. Эстрогены оказывают анаболическое действие на обмен веществ, что особенно выражено по отношению к половым органам во время беременности. Вилочковая железа (тимус) играет важную роль в иммунологической защите организма. Под ее влиянием образуются Т-лимфоциты, которые затем поступают в лимфатические узлы. Удаление резко ослабляет иммунитет организма. Ей принадлежит важная роль в противоопухолевой защите организма.
Моно- и полисинаптические рефлексы. Рефлекс – стереотипная ответная реакция организма на любое (внешнее или внутреннее) воздействие. Схема строения рефлекторной дуги: рецепторы→афферентный путь→ЦНС→эфферентный путь→эффектор. По особенностям строения рефлекторной дуги рефлексы бывают моносинаптические и полисинаптические (несколько вставочных нейронов в ЦНС). Моносинаптические: Коленный, Закрывания рта, Растяжения локтевого сустава, Подошвенный (раздражение подошвы). Полисинаптические: Сосательный, Глотательный, Чихательный, Зрачковый, Отдергивания руки. В неврологии для исследования состояния НС человека используются моносинаптические рефлексы. Обычно коленный рефлекс проверяют на обеих конечностях (справа и слева). В норме рефлексы от симметричных конечностей должны быть выражены примерно одинаково. Различные моносинаптические рефлексы замыкаются на разных уровнях спинного мозга (поясничные, грудные, шейные отделы), и при подозрении на поражение какого-либо участка спинного мозга на основе проявлений разных рефлексов можно выяснить, на каком уровне спинного мозга существует поражение или нарушение функции. В случае полисинаптических рефлексов рецептор и эффектор обычно находятся в разных органах. В связи с наличием вставочных нейронов в ЦНС и явления суммации полисинаптические рефлексы обладают особыми свойствами, которых нет у моносинаптических рефлексов, а именно: а) зависимость времени рефлекса от силы раздражения – чем сильнее стимул, тем короче время рефлекса; б) зависимость силы ответа от интенсивности раздражения – при усилении интенсивности стимула происходит вовлечение новых дополнительных групп мышц в ответную реакцию; в) привыкание – ослабление рефлекторного ответа на неболевой и неповреждающий стимул, который часто повторяется в одном и том же месте с одинаковой интенсивностью. Это явление характерно для тактильных рецепторов кожи.
Экстрапирамидная и пирамидная системы регуляции движений. Экстрапирамидная система – совокупность структур мозга, расположенных в больших полушариях и стволе головного мозга и участвующих в центральном управлении движениями, минуя пирамидную систему. К ней относятся базальные ганглии, красное ядро среднего мозга, покрышка среднего мозга, черная субстанция, РФ моста и продолговатого мозга, ядра вестибулярного комплекса и мозжечок. Имеет особое значение в построении и контроле движений, не требующих активации внимания. Экстрапирамидная система осуществляет непроизвольную регуляции и координацию движений, регуляцию мышечного тонуса, поддержание позы, организацию двигательных проявлений эмоций (смех, плач). Обеспечивает плавность движений, устанавливает исходную позу для их выполнения. При поражении экстрапирамидной системы нарушаются двигательные функции, снижается мышечный тонус. Функционально экстрапирамидная система неотделима от пирамидной системы. Она обеспечивает упорядоченный ход произвольных движений, регулируемых пирамидной системой; регулирует врожденные и приобретенные автоматические двигательные акты, обеспечивает установку мышечного тонуса и поддержание равновесия тела; регулирует сопутствующие движения (движения рук при ходьбе) и выразительные движения (мимика). Пирамидная система - система нервных структур, участвующих в сложной и тонкой координации двигательных актов. Низшие позвоночные пирамидальной системы не имеют, она появляется только у млекопитающих, и достигает наибольшего развития у обезьян и особенно у человека. Пирамидная система играет особую роль в прямохождении. Наибольшее количество пирамидных клеток (клеток Беца) иннервирует мелкие мышцы, отвечающие за тонкие дифференцированные движения кисти, мимику и речевой акт. Значительно меньшее их количество иннервирует мышцы туловища и нижних конечностей.
Структуры, входящие в систему базальных ганглиев, и их функции. Базальные ганглии — комплекс подкорковых нейронных узлов, расположенных в центральном белом веществе полушарий большого мозга. Они обеспечивают регуляцию двигательных и вегетативных функций. Базальные ганглии входят в состав переднего мозга, расположенного на границе между лобными долями и над стволом мозга и включают в себя: чечевицеобразное ядро, полосатое тело, хвостатое ядро, бледный шар, ограду. Базальные ядра связаны с обучением моторной деятельности. Полосатое тело отвечает за повороты головы и туловища в сторону противоположную раздражению. Хвостатое ядро и бледный шар также отвечают за простейшие двигательные рефлексы (мимика, позы). Ограда отвечает за пищевые, ориентировочные и эмоциональные ощущения, жевательные и глотательные движения. Нарушения в базальных ядрах приводит к моторным дисфункциям, таким как, замедленность движения, изменения мышечного тонуса, непроизвольные движения, тремор. Эти нарушения фиксируются при болезни Паркинсона.
Лимбическая система: структуры, входящие в лимбическую систему и их функции. К лимбической системе относят целый ряд различных структур головного мозга, участвующих в организации мотивационно-эмоционального поведения и тесно связанных с гипоталамусом. Функции лимбической системы не ограничиваются только участием в эмоциях. Она также регулирует вегетативные и эндокринные функции, гомеостаз, цикл "сон-бодрствование". Изначально к лимбической системе относились только те структуры, которые описал Е.В. Папец как отделы мозга, связанные с эмоциями. Он объединил их в круг, по которому циркулирует возбуждение в процессе возникновения эмоций: Гиппокамп→маммиллярные тела гипоталамуса→передние ядра таламуса→поясная извилина →гиппокамп. Гипоталамус управляет соматическими реакциями (сокращениями мышц лицевой мускулатуры) и вегетативными процессами (секреция желез и мускулатуры внутренних органов). Средний мозг отвечает за агрессивное поведение и двигательные проявления при эмоциях. Гиппокамп отвечает за процессы, связанные с памятью. Миндалина образует связи с корой б.п., таламусом, областью перегородки, структурами среднего мозга, также отвечает за эмоциональное поведение, участвует в обработке обонятельной и вкусовой информации. Поясная извилина - центр координации между деятельностью зрительной и соматической систем, что необходимо для выражения эмоций.
Морфо-функциональная организация коры больших полушарий головного мозга. 1. Проекционные зоны осуществляют высший уровень анализа внешних и внутренних сенсорных сигналов. а) Зрительная зона – затылочная часть, слуховые – височная. б) Зона Вернике – понимание и восприятие речи. в) Соматосенсорные проекционные области – кожная, мышечная чувствительность. 2. Ассоциативные зоны. а) Теменная височная доля – воссоздание образов и явлений, осуществление интеграции афферентных потоков от разных сенсорных систем. б) Лобные ассоциативные доли связаны с организацией социального поведения. в) Лобная доля коры б.п. (зона Брока) – произнесение слов. 3. Моторные зоны – вертикальные структуры (колонки), отвечающие за сокращения мышц. а) Первичная моторная кора – топическая проекция конкретных мышц. б) Вторичная – отвечает за сокращение целых групп мышц.
Морфофункциональная организация новой коры представлена, с одной стороны, горизонтальной структурой (слои коры и основанные на особенностях клеточного строения цитоархитектонические поля по Бродману), а с другой стороны - вертикальной структурой (вертикальными колонками). Практически все сигналы, поступающие в кору, вначале обязательно переключаются в таламусе.
Функции различных областей коры головного мозга. 1. Проекционные зоны коры осуществляют высший уровень анализа внешних и внутренних сенсорных сигналов. Получают информацию от специфических ядер таламуса. Каждая сенсорная зона имеет топический принцип организации – каждому участку рецепторной поверхности соответствует четко определенный участок в проекционной коре. Основными сенсорными зонами являются зрительные, слуховые и соматосенсорные области. Зрительные проекционные зоны занимают затылочную область коры. На уровне первичной зрительной зоны происходит детектирование отдельных признаков зрительного образа. Вторичные и третичные зрительные зоны осуществляют взаимодействие зрительного сигнала с информацией от других сенсорных систем. Слуховые проекционные зоны находятся в височных областях коры. В первичных слуховых областях происходит анализ звуков разной частоты. Здесь происходит анализ тона, громкости и характера коротких звуков. Во вторичных слуховых зонах осуществляется оценка значимости звуковых сигналов (видовая и индивидуальная). Особое значение для человека имеет область височной коры левого полушария (зона Вернике). Эта область отвечает за понимание и восприятие речи, является сенсорным центром речи. Соматосенсорные проекционные области осуществляют высший уровень анализа кожной, мышечной и висцеральной чувствительности (топическая организация). 2. Ассоциативные зоны коры. Теменная ассоциативная зона обеспечивает воссоздание целостных образов предметов и явлений. Создает возможности для восприятия целостного образа предмета и его пространственно-временных отношений с другими предметами. При повреждении этой области нарушается способность комплексного восприятия предметов во всей совокупности их признаков, нарушается дифференцировка предметов, их пространственное различение. Лобные ассоциативные зоны сформированы полностью только у приматов и человека. Нейроны этих зон полимодальны и имеют множество связей с другими корковыми областями, а также с подкорковыми структурами. У человека передние участки лобных долей участвуют в реализации наиболее сложных процессов, связанных с сохранностью личности, формированием социальных отношений, адекватностью поведения. Участки лобной коры связаны с организацией целенаправленного поведения: программирование, прогнозирование последствий и контроль поведения, а также с функцией принятия решения. Участвуют в организации речевой деятельности – нижняя треть задней лобной извилины содержит моторную речевую зону (зону Брока), ответственную за произнесение слов. 3. Моторные зоны. Расположены в прецентральной области и на медиальной поверхности есть еще дополнительная моторная область. Электрическая стимуляция различных участков моторной коры приводит к сокращениям отдельных мышц противоположной стороны тела. Топическая организация. Нейронные группировки моторной коры, связанные с движениями различных мышц, занимают разные по размеру площади и распределены неравномерно. Большие участки коры отвечают за движения пальцев рук, кистей, языка, мышц лица, и существенно меньше – за движения крупных мышц спины и нижних конечностей. Повреждение моторной коры у человека приводит к параличам соответствующей мускулатуры.
Биоэлектрическая активность коры больших полушарий. Метод ЭЭГ. ЭЭГ – регистрация суммарной электрической активности головного мозга. Регистрирует суммарный постсинаптический потенциал. Ритмы ЭЭГ: 1. Альфа-ритм (8-13Гц) – ритм функционального покоя коры; активность из таламуса. 2. Бета-ритм (14-35Гц) – корковая, подкорковая активность. 3. Тета-ритм (4-7Гц) – из лимбической системы (эмоции). 4. Дельта-ритм (0,5-3Гц) – из стволовых структур. 5. Гамма-ритм (>35Гц).
Когерентность – мера синхронности колебаний в 2 точках мозга от 0 до 1.
