- •Лекция №15 квантовые свойства атома
- •Опыт Франка и Герца.
- •Квантование энергий и орбит электрона в атоме как проявление волновых свойств электрона
- •Квантовомеханическое описание водородоподобных атомов
- •Лекция №16 квантовые свойства атома
- •Квантовые числа и их физический смысл
- •Опыт Штерна и Герлаха. Гипотеза о спине электрона
- •Атом в магнитном поле
Квантование энергий и орбит электрона в атоме как проявление волновых свойств электрона
Э![]() лектрон
двигаясь по круговой орбите с точки
зрения квантовой механики представляет
собой волну. Находясь на замкнутой
орбите эта волна может существовать в
виде стоячей волны. Отсюда на орбите
длиной
лектрон
двигаясь по круговой орбите с точки
зрения квантовой механики представляет
собой волну. Находясь на замкнутой
орбите эта волна может существовать в
виде стоячей волны. Отсюда на орбите
длиной
Может разместиться только целое число волн отсюда
![]()
Для электрона, как квантовой частицы справедливо равенство
![]()
О![]() тсюда
тсюда
 или
или
Таким образом, волновые свойства электрона определяют условие квантования момента его импульса в атоме.
Приравнивая кулоновскую силу притяжения электрона к ядру и центростремительную силу
![]()
П![]() олучим
выражение для r
олучим
выражение для r
П![]() одставляя
в это выражение значение скорости
электрона найденное из выражения для
его моментаполучим
одставляя
в это выражение значение скорости
электрона найденное из выражения для
его моментаполучим
Мы получили условие квантования электронных орбит в атоме.
Равенство Кулоновской и центростремительной силы дает
![]()
Таким образом полная энергия равна
![]()
![]()
Подставляя значение
Получим выражение для энергии электрона в атоме, аналогичное выражению полученному Бором.
![]()
Квантовомеханическое описание водородоподобных атомов
Как следует из соотношений, полученных при решении задачи 5.1, длина волны де Бройля для движущегося в атоме электрона сравнима с размером атома. Мы знаем, что в этих условиях нельзя пренебречь волновыми свойствами электрона, и его движение в атоме не может быть описано законами классической физики.
Поэтому атомные системы являются важнейшими объектами физики, для описания которых следует обязательно использовать законы квантовой механики. При этом существенно, что для такого описания квантовая механика не требует каких-либо дополнительных предположений, условий и постулатов, аналогичных постулатам в теории Бора.
Сформулируем
постановку стационарной задачи квантовой
механики для водородоподобного атома,
описывающей движение электрона в
электрическом поле неподвижного ядра
с зарядом
![]() ,
где
,
где
![]() для
атома водорода и
для
атома водорода и
![]() для
других водородоподобных атомов (ионов).
Такая модель является важнейшей моделью
атомной физики. Для этой модели потенциал
поля, в котором движется электрон, может
быть записан точно. Поэтому все выводы
квантовой теории водородоподобных
атомов могут быть проверены непосредственно
в эксперименте.
для
других водородоподобных атомов (ионов).
Такая модель является важнейшей моделью
атомной физики. Для этой модели потенциал
поля, в котором движется электрон, может
быть записан точно. Поэтому все выводы
квантовой теории водородоподобных
атомов могут быть проверены непосредственно
в эксперименте.
Потенциальная энергия электрона в электрическом поле ядра определяется выражением
|
(15.1) |
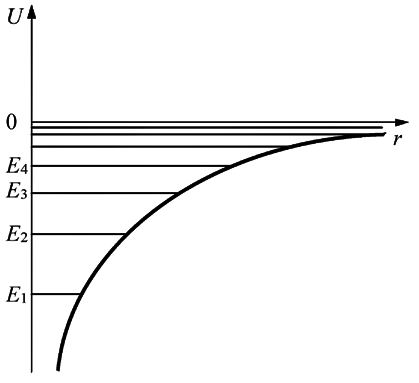
Движение электрона в таком поле можно рассматривать как движение в некоторой сферической потенциальной яме, форма которой изображена на рис. 15.3.
По
аналогии с задачей о движении частицы
в потенциальной яме простой формы, можно
ожидать, что спектр энергии электрона
в атоме будет дискретным, то есть состоять
из отдельных энергетических уровней
со значениями полной энергии электрона
![]() ,
,
![]() ,
,
![]() и
т.д. Для атома водорода этот энергетический
спектр должен совпасть с полученным в
теории Бора спектром энергий, который
подтверждается в оптических экспериментах.
и
т.д. Для атома водорода этот энергетический
спектр должен совпасть с полученным в
теории Бора спектром энергий, который
подтверждается в оптических экспериментах.
|
Рис. 15.3. |

 .
.