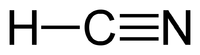- •Синильная кислота
- •[Править]Свойства [править]Химические
- •[Править]Физиологические
- •[Править]Действие на нервную систему
- •[Править]Действие на дыхательную систему
- •[Править]Действие на сердечно-сосудистую систему
- •[Править]Изменения в системе крови
- •[Править]Получение
- •[Править]Применение [править]в химическом производстве
- •[Править]Как отравляющее веществo
- •[Править]Соли
- •[Править]Биологические свойства
- •[Править]Антидоты синильной кислоты
Синильная кислота
[править]
Материал из Википедии — свободной энциклопедии
Синильная кислота |
|
|
|
|
|
|
|
Общие |
|
Традиционные названия |
циановодород, синильная кислота |
Химическая формула |
HCN |
Молярная масса |
27,0253 г/моль |
Физические свойства |
|
Состояние(ст. усл.) |
бесцветный газ или бесцветная легколетучая жидкость |
Плотность |
0,687 г/см³ |
Динамическая вязкость(ст. усл.) |
0,201 Па·с (при 20 °C) |
Термические свойства |
|
Температура плавления |
−13,4 °C |
Температура кипения |
26,7 °C |
Температура вспышки |
−17,8 °C |
Молярная теплоёмкость(ст. усл.) |
(средняя для газа и жидкости) 1,97 Дж/(моль·К) |
Химические свойства |
|
pKa |
9,21 |
Растворимостьв воде |
в любых пропорциях г/100 мл |
Оптические свойства |
|
Показатель преломления |
1,2675 |
Структура |
|
Дипольный момент |
2,98 Д |
Классификация |
|
Рег. номер CAS |
74-90-8 |
SMILES |
C#N |
Номер ООН |
1051 (безводная) |
Регистрационный номер EC |
200-821-6 |
RTECS |
MW6825000 |
Токсикология |
|
ЛД50 |
мыши (перорально) 3.7 мг/кг |
Токсичность |
4 4 1 |
Синильная кислота содержится в некоторых растениях, коксовом газе, табачном дыме, выделяется при термическом разложении нейлона,полиуретанов. Смешивается во всех отношениях с водой, этанолом, диэтиловым эфиром.
Содержание [убрать]
|
[Править]Свойства [править]Химические
Молекула HCN сильно полярна (μ = 0,96×10−29 Кл·м). Циановодород состоит из молекул двух видов, находящихся в таутомерномравновесии (превращение циановодорода в изоциановодород), которое при комнатной температуре смещено влево:
![]()
Большая стабильность первой структуры обусловлена меньшими значениями эффективных зарядов атомов.
Безводная синильная кислота является сильно ионизирующим растворителем, растворенные в нем электролиты хорошо диссоциируют на ионы. Его относительная диэлектрическая проницаемость при 25 °C равна 107 (выше, чем у воды). Это обусловлено линейной ассоциацией полярных молекул HCN за счет образования водородных связей.
Очень слабая одноосновная кислота К = 1,32×10−9 (18 °C). Образует с металлами соли — цианиды. Взаимодействует с оксидами игидроксидами щелочных и щёлочноземельных металлов.
Пары синильной кислоты горят на воздухе фиолетовым пламенем с образованием Н2О, СО2 и N2. В смеси кислорода со фтором горит с выделением большого количества тепла:
![]() кДж.
кДж.
Синильная кислота широко применяется в органическом синтезе. Она реагирует с карбонильными соединениями, образуя циангидрины:
![]()
С галогеналканами образует нитрилы (реакция Кольбе):
![]()
С алкенами и алкинами реагирует, присоединяясь к кратным связям:
![]()
![]()
![]()
Легко полимеризуется в присутствии основания (часто со взрывом). Образует аддукты, например HCN-CuCl.