
- •1.Основные этапы развития геохимии
- •2.Задачи геохимии
- •3.Строение атома
- •4.Типы химической связи
- •5.Гомодесмические и гетеродесмические структуры
- •7.Геометрические типы структур
- •Радиоактивность
- •9.Типы радиоактивного распада
- •10.Радиогенные изотопы
- •11. Закон радиоактивного распада, период полураспада
- •12.Радиогенные изотопы как трассеры геохимических процессов
- •13.Методы определения абсолютного возраста.
- •14.Методы датирования по обычному свинцу
- •17.Классификация силикатов и алюмосиликатов
- •18. Силикаты с непрерывными цепочками или лентами тетраэдров SiO4
- •19. Номенклатура пироксенов
- •20. Силикаты со сдвоенными анионными цепочками
- •21.Силикаты с непрерывными трехмерными каркасами из тетраэдров (Si, Al) o4
- •22.Правило фаз Гиббса
- •23. Однокомпонентные системы
- •24.Двухкомпонентные системы при отсутствии твердых растворов и соединений
- •25.Двухкомпонентная система при отсутствии твердых растворов с промежуточным соединением
- •26. Двухкомпонентные системы с соединением плавящимся инконгруэнтно
- •27.Диаграммы двухкомпонентных систем с твердыми растворами.
- •28. Астероиды
- •29. Классификация метеоритов
- •30. Происхождение Солнечной системы
- •31. Планеты земной группы
- •32. Планеты-гиганты
- •33. Хондритовая модель происхождения Земли
- •34. Происхождение Луны
- •35. Образование слоистой структуры Земли
- •36.Ядро и мантия Земли
- •37.Космохимическая оценка состава мантии.
- •38.Номенклатура ультраосновных пород
- •39.Причины существования скачков в скоростях распространения сейсмических волн в мантии.
- •40.Факторы, контролирующие распределение элементов между корой и мантией.
- •41. Свидетельства мантийной гетерогенности.
- •42. Причины химических вариаций в мантии
- •43. Геохимические отличия базальтов срединно-океанических хребтов от базальтов океанических островов.
- •44. Минералы земной коры
- •45. Классификации вулканических и плутонических пород
- •46.Фации метаморфизма
- •47.Строение континентальной коры
- •48. Методы оценки состава верхней коры
- •49.Средняя континентальная кора
- •50.Нижняя континентальная кора
- •51.Образование континентальной коры
- •52.Происхождение адакитов
- •53.Происхождение тоналит-трондьемит-гранодиоритовой серии
- •54.Проблема формирования гранитоидов
- •55. Состав и строение атмосферы Земли
- •56.Происхождение атмосферы Земли.
- •57.Атмосфера на ранней стадии развития Земли
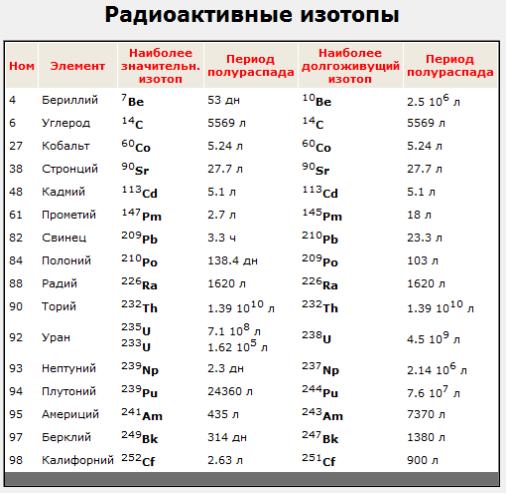
10.Радиогенные изотопы
Радиоакти́вные изото́пы — изотопы, ядра которых нестабильны и испытывают радиоактивный распад. Большинство известных изотопов радиоактивны (стабильными являются лишь около 300 из более чем 3000 нуклидов, известных науке). У любого химического элемента есть хотя бы несколько радиоактивных изотопов, в то же время далеко не у всех элементов есть хотя бы один стабильный изотоп; так, все известные изотопы всех элементов, которые в таблице Менделеева идут после свинца, радиоактивны.
Радиоактивны все химические элементы с порядковым номером, большим 82 (то есть начиная с висмута), и многие более лёгкие элементы (прометий и технеций не имеют стабильных изотопов, а у некоторых элементов, таких как индий, калий или кальций, часть природных изотопов стабильны, другие же радиоактивны).
Изотопы - разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре. Все изотопы одного элемента имеют одинаковый заряд ядра.
Изотоны - атомы (или ядра) с разным количеством протонов в ядре, но с одинаковым количеством нейтронов.
Изобары – атомы (или ядра) с одинаковым значением массового числа А, но с разными количествами протонов Z и нейтронов N.
11. Закон радиоактивного распада, период полураспада
Закон радиоактивного распада — закон, открытый Фредериком Содди и Эрнестом Резерфордом экспериментальным путём и сформулированный в 1903 году.
С![]() овременная
формулировка закона:
овременная
формулировка закона:
что означает, что число распадов за интервал времени в произвольном веществе пропорционально числу имеющихся в образце атомов .
В этом математическом выражении — постоянная распада, которая характеризует вероятность радиоактивного распада за единицу времени и имеющая размерность с-1. Знак минус указывает на убыль числа радиоактивных ядер со временем.
Этот закон считается основным законом радиоактивности, из него было извлечено несколько важных следствий, среди которых формулировки характеристик распада — среднее время жизни атома и период полураспада.
П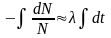 ериод
полураспада
T1/2
-
время, за которое первоначальное
количество радиоактивных ядер уменьшится
в два раза. T1/2
=
ln2/λ=0.693/λ = τln2.
ериод
полураспада
T1/2
-
время, за которое первоначальное
количество радиоактивных ядер уменьшится
в два раза. T1/2
=
ln2/λ=0.693/λ = τln2.
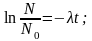
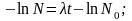
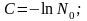
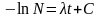
п
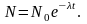 ри
t=0,
N=N0,
откуда:
ри
t=0,
N=N0,
откуда:
12.Радиогенные изотопы как трассеры геохимических процессов
При использовании процессов радиоактивного распада для изучения пород и минералов удобно соотносить число атомов радиогенного и дочернего продуктов распада не с первоначальным числом атомов, а с числом родительского радионуклида.
D*=N0-N, подставляем N=N0*e-λt , тогда: D*= N*( e-λt – 1).
В общем случае число атомов дочернего продукта (D),присутствующих в системе,
определяется уравнением, где D0 – первоначальное (t=0) число атомов дочернего нуклида. D= D0+D* это равносильно D= D0+ N*( e-λt – 1).
Условия при которых уравнение можно решить относительно t:
Порода или минерал не должен терять ни родительский, ни дочерний нуклиды. Образец породы или минерал должен быть закрытой системой относительно родительского и дочернего нуклидов.
Величина D0 необходимо приписывать реальные значения. Это обычно возможно. Особенно когда D* намного больше D0.
Значение постоянной распада l должно быть точно известно.
И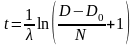 змерение
D
и N
должно производиться с достаточной
точностью, и полученные значения должны
быть представительными по отношению к
датируемой породе или минералу.
змерение
D
и N
должно производиться с достаточной
точностью, и полученные значения должны
быть представительными по отношению к
датируемой породе или минералу.
