
- •Бхм сердца и сосудов. Бхм крови. Обменгемоглобина (120-145)
- •Оксид азота и супероксид. Пути образования и инактивации. Эндотелин 1. Схема образования, эффекты на тонус сосудов в норме и при повышенной продукции.
- •Механизм регуляции тонуса резистивных сосудов оксидом азота и супероксидом. Нарушения эндотелийзависимой регуляции тонуса сосудистой стенки при артериальной гипертензии.
- •Механизм эндотелий-зависимой вазодилатации (события в эндотелиоците) :
- •Механизм эндотелий-зависимой вазодилатации (события в гмк):
- •Метаболические особенности миокарда: механизм сокращения миоцитов, основные энергетические субстраты и пути их утилизации. Роль миоглобина и креатинфосфата в энергетическом обмене миокарда.
- •Лабораторные маркеры повреждения кардиомиоцитов (тропонин т, креатинкиназа, миоглобин, лактатдегидрогеназа, аминотрансферазы).
- •Неорганические вещества плазмы крови (натрий, калий, кальций, фосфор). Общие закономерности обмена. Функции, нарушения при изменении концентрации в плазме крови.
- •Альбумин плазмы крови: функции, понятие о причинах и проявлениях гипоальбумиемии.
- •Транспортные белки плазмы крови (белки, переносящие витамины, гормоны, ионы переходных металлов). Место синтеза. Зависимость эффекта лиганда от концентрации транспортного белка.
- •Белки острой фазы воспаления, иммуноглобулины. Функции.
- •Внутриклеточные белки и белки секретов в плазме крови. Клинико-диагностическое значение исследования.
- •Эритроциты, место образования и распада. Регуляция эритропоэза эритропоэтином. Особенности метаболизма эритроцитов и структуры их мембран.
- •Гемоглобин: строение, структура гема, основные этапы синтеза гема, типы и виды гемоглобина.
- •Функции эритроцитов. Механизм транспорта кислорода эритроцитами, аллостерическая регуляция сродства гемоглобина к кислороду. Роль эритроцитов в транспорте углекислого газа.
- •Обмен железа. Лабораторные показатели дефицита железа в организме. Понятие о физиологической желтухе новорожденных.
- •Гемолитическая желтуха. Механизм развития. Лабораторные маркеры.
- •Паренхиматозная желтуха. Механизм развития. Лабораторные маркеры.
- •Обтурационная желтуха. Механизм развития. Лабораторные маркеры.
- •Лейкоциты. Особенности метаболизма фагоцитирующих клеток (моноциты, гранулоциты). Образование лейкоцитами активных форм кислорода, их биологическая роль.
- •Компоненты свертывающей, противосвертывающей, фибринолитической систем гемостаза. Последовательность гемостатических реакций после повреждения сосудистой стенки.
- •Тромбоциты, место образования, биологическая роль. Основные структурно-функциональные элементы тромбоцита.
- •Механизм адгезии и агрегации тромбоцитов. Фактор Виллебранда: структура, участие в гемостазе. Тромбоксан простациклин: схема синтеза, участие в гемостазе.
- •Реакции в свертывающей системе плазмы крови, ведущие к образованию фибрина. Факторы свертывания, строение, место синтеза. Кофакторы. Значение витамина к для синтеза факторов свертывания.
- •Антикоагулянты (гепарин, антитромбин III, ингибитор тканевого пути свертывания, протеины с и s): химическая природа, место синтеза, механизм действия.
- •Фибринолитическая система крови: компоненты, механизмы активации и функционирования.
Функции эритроцитов. Механизм транспорта кислорода эритроцитами, аллостерическая регуляция сродства гемоглобина к кислороду. Роль эритроцитов в транспорте углекислого газа.
Функции эритроцитов:
Дыхательная - транспорт кислорода и участие в транспорте углекислого газа.
Адсорбция и транспорт питательных веществ.
Адсорбция и транспорт токсинов.
Регуляция ионного состава плазмы крови.
Формирует реологические характеристики крови/вязкость и т.д./
Гемоглобин присоединяет кислород, с образованием оксигемоглобина Эта реакция обратима:
Нв+О2=НвО2
Направленность реакции зависит от содержания кислорода: если количество кислорода в крови увеличивается, то реакция идет в сторону образования оксигемоглобина, если уменьшается - то в противоположную сторону.
С понижением рН освобождение О2 гемоглобином облегчается. То же происходит при повышении концентрации СО2. Это чрезвычайно важно с физиологической точки зрения, так как в тканях с быстро протекающим обменом веществ, таких, как мышечная ткань, образуется много СО2 и кислот. Высокие уровни СО2 и Н+ стимулируют освобождение О2 из гемоглобина, и таким образом удовлетворяется потребность в большом количестве кислорода в метаболически активных тканях. После освобождения кислорода дезоксигемоглобин присоединяет Н+ и СО3. Для альвеолярных капилляров легких характерна более высокая концентрация кислорода, и там по мере связывания дезо-ксигемоглобином кислорода происходит освобождение Н+ и СО2.
Транспорт СО2 эритроцитами.С02 диффундирует из тканей в плазму крови, а из нее — в эритроциты по градиенту парциального давления С02. В эритроцитах С02 образует с водой угольную кислоту, которая диссоциирует на Н+ и HCO3. (С02 + Н20 = Н2СО3 = Н+ + HCO3). Эта реакция протекает быстро, поскольку С02 + Н20 = Н2СОэ катализируется ферментом карбоангидразой мембраны эритроцитов, которая содержится в них в высокой концентрации.
Н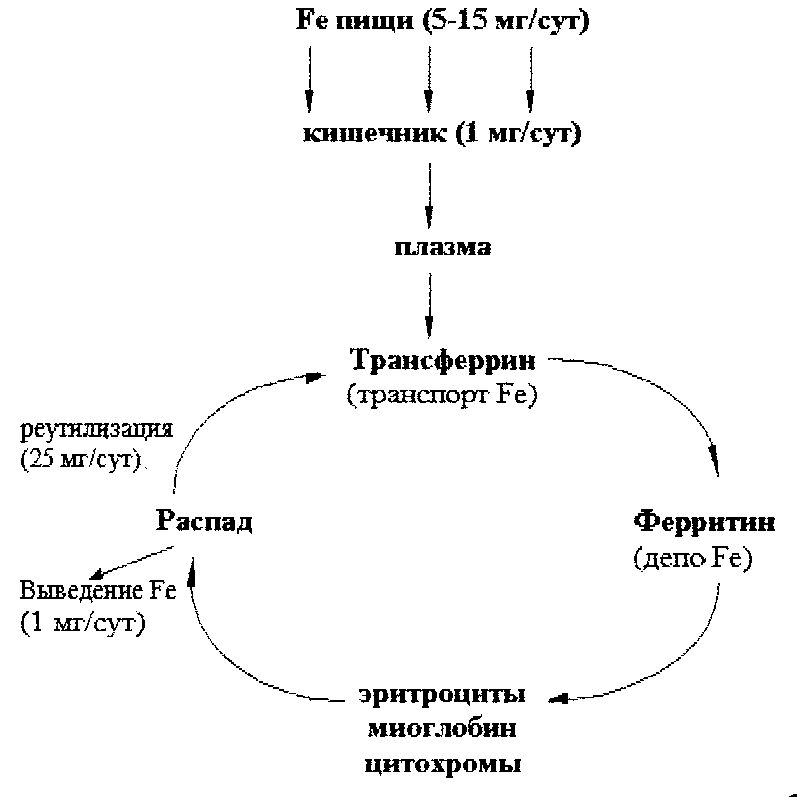 ебольшое
количество углекислого газа (10%)
транспортируется в виде карбогемоглобина
– соединения CO2 c
гемоглобином.
ебольшое
количество углекислого газа (10%)
транспортируется в виде карбогемоглобина
– соединения CO2 c
гемоглобином.
Обмен железа. Лабораторные показатели дефицита железа в организме. Понятие о физиологической желтухе новорожденных.
В организме взрослого человека содержится 3-4 г железа, из этого количества около 3,5 г находится в плазме крови. Гемоглобин эритроцитов содержит примерно 68 % всего железа организма, ферритин – 27 % (резервное железо печени, селезенки, костного мозга), миоглобин (в мышцах) – 4 %, трансферрин (в плазме крови) – 0,1. На долю всех содержащих железо ферментов приходится примерно 1 % железа, имеющегося в организме.
В обмене железа принимает участие ряд белков.
Апоферритин. Белок связывает железо в эритроцитах и превращается в ферритин, который остается в энтероцитах. Таким способом регулируется поступление железа в капилляры крови из клеток кишечника. Когда потребность организма в железе невелика, скорость синтеза апоферритина повышается. При недостатке железа в организме апоферритин в энтероцитах почти не синтезируется.
Трансферрин. Это транспортный белок, относится к гликопротеинам, синтезируется в печени. Он имеет два центра связывания железа. Трансферрин транспортирует железо с током крови к местам депонирования и использования. В норме трансферрин насыщен железом приблизительно на 33 %.
Ферритин. Олигомерный белок с молекулярной массой 450 к Да. Он состоит из 24 идентичных протомеров, образующих полую сферу. Железо депонируется в ферритине в виде гидроксифосфата. Содержание железа в молекуле ферритина непостоянно. Функция ферритина – депонирование железа. Ферритин содержится почти во всех тканях, но в наибольшем количестве в печени, селезенке, костном мозге.
Дефицит железа. В общем анализе крови при железодефицитной анемии будут регистрироваться снижение уровня гемоглобина и эритроцитов. Умеренная эритроцитопения может проявляться при Нb <98 г/л, однако снижение эритроцитов <2 х 1012/л для ЖДА не характерно. При ЖДА будут регистрироваться изменения морфологических характеристик эритроцитов и эритроцитарных индексов, отражающих количественно морфологические характеристики эритроцитов.При развитии ЖДА в биохимическом анализе крови будут регистрироваться: • уменьшение концентрации сывороточного ферритина; • уменьшение концентрации сывороточного железа; • повышение ОЖСС (общая железосвязывающая способность сыворотки ); • уменьшение насыщения трансферрина железом.
Физиологическая желтуха новорожденных — физиологическое преходящее состояние, которое отмечается у большинства здоровых новорожденных и является следствием временного повышения уровня билирубина в крови ребенка. У новорожденных после рождения отмечается повышенный распад красных кровяных телец (эритроцитов), что приводит к увеличению содержания в крови продукта их распада — желтушного пигмента (билирубина). Вследствие возрастной незрелости печени билирубин выводится из организма несколько медленно, благодаря чему у некоторых детей кожные покровы и склеры глаз временно могут приобретать желтый оттенок. Симптомы физиологической желтухи новорожденных появляются в большинстве случаев на вторые или третьи сутки после рождения ребенка, а затем медленно исчезает к двум-трем неделям.
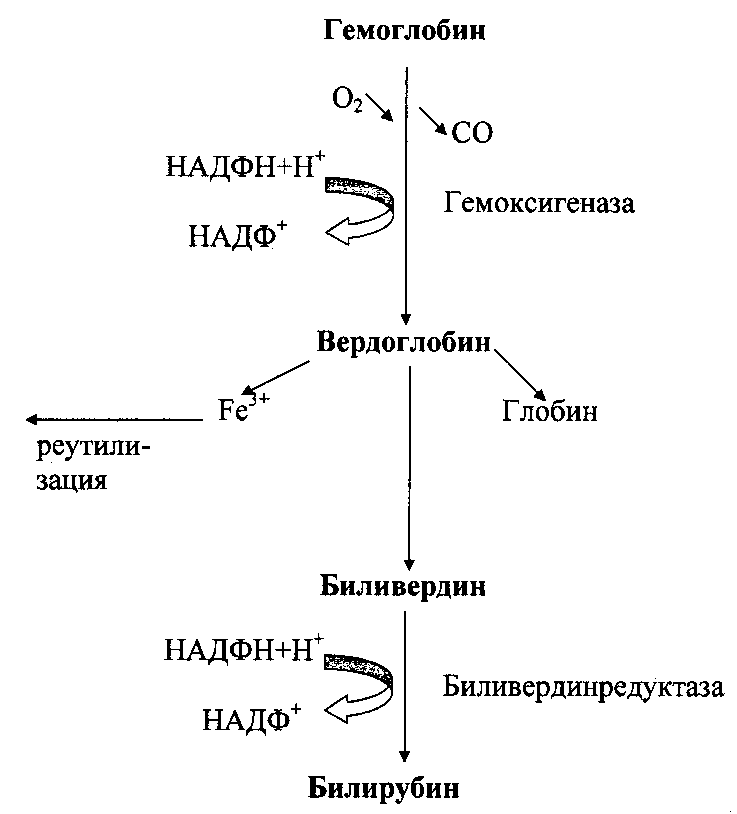
Схема распада гемоглобина. Механизм токсического действия билирубина. Продукты распада гемоглобина в крови, моче, кале в норме.
Начальным этапом распада гемоглобина является разрыв одного метинового мостика с образованием вердоглобина. В дальнейшем от молекулывердоглобина отщепляются атомжелеза и белокглобин. В результате образуется биливердин. Затем биливердин, восстанавливаясь,превращается в билирубин – пигмент, выделяемый с желчью и поэтому называемыйжелчным пигментом. Образовавшийся билирубин называется непрямым(неконъю-гированным) билирубином,поскольку вследствие плохой растворимости в воде он легко адсорбируется на белках плазмы крови (альбуминах).
Комплекс альбумин-билирубин с током крови попадает в печень, где происходит его превращение в прямой билирубин путем коньюгации с глюкуроновой кислотой. Реакцию катализирует фермент УДФ-глюкуронилтрансфераза. Образующийся билирубиндиглюкуронид получил название прямого (коньюгированного) билирубина или связанного.Прямой билирубин – это нормальный компонент желчи, попадающий в кровь в незначительном количестве.
Механизм токсического действия билирубина:
- снижение синтеза АТФ
- снижении скорости реакций, идущих с затратой АТФ
- разобщение процессов тканевого дыхания и окислительного фосфорилирования
Распределение желчных пигментов в норме: кровь – общий билирубин – 8,5 – 20,5 мкмоль/л; непрямой билирубин – 1,7 – 17,1 мкмоль/л; прямой билирубин – 2,2 – 5,1 мкмоль/л; моча – стеркобилиноген – 4 мг/сутки; кал – стеркобилиноген.
