
Часть.3. Некоторые гетерофункциональные соединения, имеющие биологическое значение.
3.1. Аминоспирты.
Аминоспирты, соединения с двумя различными функциональными группами, именно амино - и гидроксильной группой. Особый интерес представляет 2 – аминоэтанол ( этаноламин ), или коламин.
NH2-CH2-CH2-OH .
Получение этаноламина уже упоминалось в разд. ”Простые эфиры. Сам этаноламин широко используется в качестве эмульгатора и других ПАВ. Но производные этаноламина имеют большое биологическое значение. Так, холин – гидроксид гидроксиэтилтриметиламмония наряду с этаноламином входит в состав сложных липидов, фосфолипидов, являющихся важнейшим компонентом клеточных мембран. Сложный эфир холина и уксусной кислоты – ацетилхолин - является нейромедиатором.
х олин
ацетилхолин
олин
ацетилхолин
 Важную
роль в организме играют аминоспирты,
содержащие структуру пирокатехина (
1,2 - дигидроксибензола). Они носят общее
название катехоламины. Катехоламины
являются представителями биогенных
аминов, аминов, образующихся в результате
жизнедеятельности организма. К
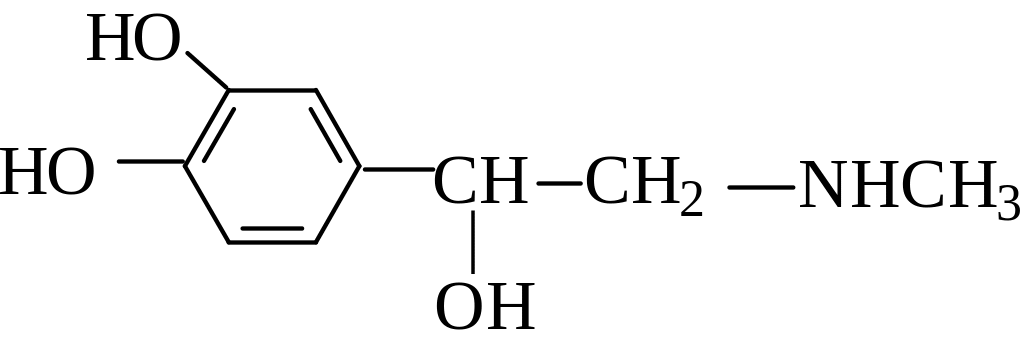
катехоламинам относится и адреналин,
который как и ацетилхолин, выполняет
роль нейромедиатора.
Важную
роль в организме играют аминоспирты,
содержащие структуру пирокатехина (
1,2 - дигидроксибензола). Они носят общее
название катехоламины. Катехоламины
являются представителями биогенных
аминов, аминов, образующихся в результате
жизнедеятельности организма. К
катехоламинам относится и адреналин,
который как и ацетилхолин, выполняет
роль нейромедиатора.
адреналин
3.2.Гидроксикислоты.
Гидроксикислоты содержат в своей молекуле одновременно гидроксильную группу и карбоксильную. В зависимости от взаимного расположения этих групп гидроксикислоты подразделяются на -, -, - и т .д. гидроксикислоты.
г![]() идроксиэтановая
3-гидроксипропановая 4- гидроксибутановая
идроксиэтановая
3-гидроксипропановая 4- гидроксибутановая
гликолевая -гидроксимасляная
Гидроксикислоты - кристаллические вещества, хорошо растворимые в воде, обычно являются более сильными кислотами по сравнению с предельными карбоновыми кислотами. Наличие в молекуле гидроксикислот карбоксильной и спиртовой групп приводит к тому, что эти соединения вступают в реакции, характерные как спиртам, так и кислотам. Например при взаимодействии со спиртом может образоваться сложный эфир кислоты:
э![]() тиловый
эфир гликолевой кислоты
тиловый
эфир гликолевой кислоты
В то же время известен сложный эфир, образованный этой кислотой как спиртом с уксусным ангидридом:
![]()
Гидроксикислоты при нагревании легко отщепляют воду, но в зависимости от положения гидроксильной группы получаются различные вещества. -Гидроксикислоты при нагревании легко теряют воду и образуют циклические сложные эфиры, называемые лактидами:
Л актид
молочной кислоты
актид
молочной кислоты
-Гидроксикислоты при нагревании отщепляют воду, образуя непредельные кислоты:

-гидроксипропионовая пропеновая кислота (акриловая кислота)
- и -Гидроксикислоты при нагревании образуют пяти- и шестичленные циклические внутренние сложные эфиры - лактоны:
 лактон
-гидроксимасляной
кислоты
(γ -
бутиролактон)
лактон
-гидроксимасляной
кислоты
(γ -
бутиролактон)
Фактором,определяющим направление дегидратации гидроксикислот , является устойчивость образующегося цикла. Образование лактидов приводит к устойчивому шестичленному циклу, то же наблюдается при образовании лактонов (5- и 6- членные циклы ). В случае -гидроксикислот должен был бы образоваться четырехчленный лактон, последний мало устойчив, следствием чего является образование - , - непредельных кислот.
3.3.Аминокислоты.
Аминокислоты - это органические соединения, в состав которых входят карбоксильная и аминогруппа. В зависимости от их взаимного расположения различают -, -, - аминокислоты. Например:

- аминопропановая - аминопропановая - аминопропановая
кислота кислота кислота
Наибольшее значение среди природных соединений имеют - аминокислоты, так как природные белки построены именно из этих аминокислот. Среди - аминокислот выделяют группу из 20 наиболее важных .
Таблица.3.3.1.
Важнейшие α - аминокислоты

Нейтральные (моноаминомонокарбоновые)
Строение R |
Название |
Сокращенное название аминокислотного остатка |
H- |
Глицин |
Гли |
CH3- |
Аланин |
Ала |
(CH3)2CH- |
Валин |
Вал |
(CH3)2CH-CH2- |
Лейцин |
Лей |
CH3CH2CH(CH3)2- |
Изолейцин |
Иле |
C6H5CH2- |
Фенилаланин |
Фен |
Кислые (моноаминодикарбоновые)
HOOC-CH2- |
Аспарагиновая |
Асп |
HOOC-CH2CH2- |
Глутаминовая |
Глу |
NH2CO-CH2- |
Аспарагин |
Асн |
NH2CO-CH2CH2- |
Глутамин |
Глн |
Основные (диаминомонокарбоновые)
NH2-(CH2)3-CH2- |
Лизин |
Лиз |
NH2-C-NH-(CH2)3-CH2- NH
|
Аргини |
Арг |
Гидроксилсодержащие
HO-CH2- |
Серин |
Сер |
CH3-CH(OH)- |
Треонин |
Тре |
п- HO- C6H4- CH2- |
Тирозин |
Тир |
Серусодержащие
HS-CH2- |
Цистеин |
Цис |
S-CH2- S- CH2- |
Цистин |
Цис-S-S-Цис |
CH3-S-CH2-CH2- |
Метионин |
Мет |
Гетероциклические
|
Триптофан |
Три |
|
Гистидин |
Гис |
|
Пролин |
Про |
|
Гидроксипролин |
Про-ОН |
Номенклатура аминокислот. Любую аминокислоту можно назвать согласно правилам ИЮПАК, но в химии - аминокислот обычно используются тривиальные названия. В биохимии используются трехбуквенные сокращения тривиальных названий природных - аминокислот. Основные природные аминокислоты приведены в табл.3.3.1.
- Аминокислоты классифицируют различным образом: в зависимости от природы углеводородного радикала: ароматические, алифатические, гетероциклические; c учетом общего числа карбоксильных и аминогрупп в молекуле - аминокислоты подразделяются на нейтральные, кислые, основные. (см. табл.3.3.1.).
Стереохимия - аминокислот.
Все природные - аминокислоты, кроме простейшей аминокислоты - глицина, содержат хотя бы один хиральный центр и могут существовать в виде пары энантиомеров.
 -Аминокислота
L -
- Аминокислота D- -
Аминокислота
-Аминокислота
L -
- Аминокислота D- -
Аминокислота
Почти все природные - аминокислоты принадлежат к L-ряду. Использование для построения белков человеческого организма только одного вида стереоизомеров - аминокислот имеет важнейшее значение для формирования пространственной структуры белков и проявления ими биологической активности.
Cинтез - аминокислот.
Из приведенного выше материала видно, что аминокислоты имеют разнообразное строение и способы синтеза их также различны. Мы остановимся на наиболее общих, включающих введение одной амино- или карбоксильной группы .
1.Замена галогена в - галогензамещенной кислоте на аминогруппу.
При действии на бромуксусную кислоту аммиаком получают глицин
![]() изб.
изб.
2. Циангидридный метод.
- Аминокислоты получаются при действии на альдегиды и кетоны цианистым аммонием с последующим гидролизом промежуточно образующихся соединений:
3 .
Восстановительное аминирование
оксокислот.
.
Восстановительное аминирование
оксокислот.
- Аминокислоты получают при каталитическом восстановлении оксокарбоновых кислот водородом в присутствии аммиака:
Н аиболее
удобным способом получения -
аминокислот L -ряда служат белки, которые
подвергают гидролизу. Синтетическим
путем получают только рацемические
смеси -
аминокислот. Для получения нужного
энантиомера рацемическую смесь,
полученную синтезом, подвергают
расщеплению. Один из способов расщепления
-
аминокислот описан ранее (см.раздел
1.3.3. ).
аиболее
удобным способом получения -
аминокислот L -ряда служат белки, которые
подвергают гидролизу. Синтетическим
путем получают только рацемические
смеси -
аминокислот. Для получения нужного
энантиомера рацемическую смесь,
полученную синтезом, подвергают
расщеплению. Один из способов расщепления
-
аминокислот описан ранее (см.раздел
1.3.3. ).
- Аминокислоты представляют собой бесцветные кристаллические вещества, большинство из них легко растворимы в воде.
- Аминокислоты плавятся с разложением при высоких и довольно близких температурах. Определение температуры плавления недостаточно для их идентификации и поэтому для этой цели используют данные хроматографии.
- Аминокислоты содержат одновременно основную, аминную, и кислую, карбоксильную группы, которые взаимодействуют между собой, образуя внутреннюю соль - биполярный ион
(цвиттер – ион )
В водном растворе внутренняя соль, как
соль слабой кислоты и слабого основания,
гидролизуется, при этом образуются
катионы и анионы аминокислоты.
водном растворе внутренняя соль, как
соль слабой кислоты и слабого основания,
гидролизуется, при этом образуются
катионы и анионы аминокислоты.
И ными
словами,
- аминокислоты являются амфотерными
соединениями и в зависимости от рН среды
образуются катионы и анионы, которые
под действием электрического тока могут
передвигаться к катоду или аноду. Если
этот процесс проводят на хроматографической
бумаге или в гелях, то такой процесс
называется электрофорезом. Этот метод
используется для идентификации или
разделения аминокислот.
ными
словами,
- аминокислоты являются амфотерными
соединениями и в зависимости от рН среды
образуются катионы и анионы, которые
под действием электрического тока могут
передвигаться к катоду или аноду. Если
этот процесс проводят на хроматографической
бумаге или в гелях, то такой процесс
называется электрофорезом. Этот метод
используется для идентификации или
разделения аминокислот.
с![]() опряженная
нейтральный биполярный ион сопряженное
кислота глицина глицин основание глицина
опряженная
нейтральный биполярный ион сопряженное
кислота глицина глицин основание глицина
( кислая среда) щелочная среда
В связи с тем, что в зависимости от строения
в молекуле могут преобладать либо
кислотные свойства карбоксила, либо
основные свойства аминогруппы, в водных
растворах аминокислот рН среды отличается
от нейтральной. Но на кривой титрования
аминокислоты имеется значение рН ,при
котором количество групп NH3+
оказывается точно равным количеству
групп -СОО-.
Следовательно, при этом рН в условиях
электрофореза переноса заряженных
частиц не будет . Такое значение рН
называют изоэлектрической точкой (
рНi).
Изоэлектрическая точка глицина 6.0.
Глутаминовая кислота содержит вторую
карбоксильную группу, и при рН = 6 большая
часть ее молекул находится в виде
анионов:
связи с тем, что в зависимости от строения
в молекуле могут преобладать либо
кислотные свойства карбоксила, либо
основные свойства аминогруппы, в водных
растворах аминокислот рН среды отличается
от нейтральной. Но на кривой титрования
аминокислоты имеется значение рН ,при
котором количество групп NH3+
оказывается точно равным количеству
групп -СОО-.
Следовательно, при этом рН в условиях
электрофореза переноса заряженных
частиц не будет . Такое значение рН
называют изоэлектрической точкой (
рНi).
Изоэлектрическая точка глицина 6.0.
Глутаминовая кислота содержит вторую
карбоксильную группу, и при рН = 6 большая
часть ее молекул находится в виде
анионов:
Чтобы достигнуть изоэлектрической точки, некоторые из этих анионов надо протонировать, что возможно только при понижении рН. рНi глутаминовой кислоты равна 3.22.
Реакции аминокислот.
Аминокислоты содержат амино - и карбоксильную группы и проявляют все свойства, характерные для соединений с такими функциональными группами. При написании реакций аминокислот пользуются формулами с неионизированными амино- и карбоксигруппами.
1)реакции по аминогруппе. Аминогруппа в аминокислотах проявляет обычные свойства аминов : амины являются основаниями, а в реакциях выступают в роли нуклеофилов.
Реакция аминокислот как основания. При взаимодействии аминокислоты с кислотами образуются аммонийные соли:
х
 лоргидрат
глицина, хлороводородная соль глицина
лоргидрат
глицина, хлороводородная соль глицина
2. Действие азотистой кислоты. При действии азотистой кислоты образуются гидроксикислоты и выделяется азот и вода:
 Эту
реакцию используют для количественного
определения свободных аминных групп в
аминокислотах, а также и в белках.
Эту
реакцию используют для количественного
определения свободных аминных групп в
аминокислотах, а также и в белках.
3.Образование N - ацильных производных, реакция ацилирования.
Аминокислоты реагируют с ангидридами и галогенангидридами кислот, образуя N - ацильные производные аминокислот:
б![]() ензиловый
эфир натриевая соль N карбобензоксиглицин
- хлормуравьиной глицина
ензиловый
эфир натриевая соль N карбобензоксиглицин
- хлормуравьиной глицина
Ацилирование - один из способов защиты аминогруппы. N-ацильные производные имеют большое значение при синтезе пептидов, так как N-ацилпроизводные легко гидролизуются с образованием свободной аминогруппы.
4.Образование оснований Шиффа. При взаимодействии - аминокислот с альдегидами образуются замещенные имины ( основания Шиффа ) через стадию образования карбиноламинов:

α-аминокислота альдегид карбиноламин основание Шиффа
Эта реакция имеет практическое значение для количественного определения - аминокислот методом формольного титрования. Вследствие амфотерного характера - аминокислоты не могут быть непосредственно оттитрованы щелочью в аналитических целях. При взаимодействии -аминокислот с формальдегидом получаются относительно устойчивые карбиноламины – N - метилольные производные, имеющие свободную карбоксильную группу, которую можно оттитровать щелочью как обычную карбоновую кислоту.

аланин формальдегид N-метилольное производное аланина
5.Реакция алкилирования. Амииногруппа в -аминокислоте алкилируется с образованием N – алкилпроизводных:
Н аибольшее
значение имеет реакция с 2,4 -
динитрофторбензолом. Получаемые
динитрофенильные производные (
ДНФ-производные ) используются при
установлении аминокислотной
последовательности в пептидах и белках.
Взаимодействие -
аминокислот с 2,4-динитрофторбензолом
является примером реакции нуклеофильного
замещения в бензольном ядре. За счет
наличия в бензольном кольце двух сильных
электроноакцепторных групп галоген
становится подвижным и вступает в
реакцию замещения:
аибольшее
значение имеет реакция с 2,4 -
динитрофторбензолом. Получаемые
динитрофенильные производные (
ДНФ-производные ) используются при
установлении аминокислотной
последовательности в пептидах и белках.
Взаимодействие -
аминокислот с 2,4-динитрофторбензолом
является примером реакции нуклеофильного
замещения в бензольном ядре. За счет
наличия в бензольном кольце двух сильных
электроноакцепторных групп галоген
становится подвижным и вступает в
реакцию замещения:
2 ,4
– динитро -
,4
– динитро -
фторбензол N - 2,4 - динитрофенил - - аминокислота
(ДНФБ) ДНФ - производные - аминокислот
6.Реакция с фенилизотиоцианатом. Эта реакция широко используется при установлении строения пептидов. Фенилизотиоцианат является производным изотиоциановой кислоты H-N=C=S. Взаимодействие - аминокислот с фенилизотиоцианатом протекает по механизму реакции нуклеофильного присоединения. В образовавшемся продукте далее осуществляется внутримолекулярная реакция замещения, приводящая к образованию циклического замещенного амида: фенилтиогидантоин.
Циклические соединения получаются с количественным выходом и представляют собой фенильные производные тиогидантоина (ФТГ - производные) - аминокислот. ФТГ - производные различаются строением радикала R.
 Фенилтиогидантоиновые
производные аминокислот
Фенилтиогидантоиновые
производные аминокислот
(ФТГ - производные α – аминокислот)
Реакции карбоксильной группы.
-Аминокислоты образуют с основаниями обычные соли, например:
 Кроме
обычных солей -
аминокислоты могут образовывать в
определенных условиях внутрикомплексные
соли с катионами тяжелых металлов. Для
всех
- аминокислот очень характерны красиво
кристаллизующиеся, интенсивно окрашенные
в синий цвет внутрикомплексные (хелатные)
соли меди ):
Кроме
обычных солей -
аминокислоты могут образовывать в
определенных условиях внутрикомплексные
соли с катионами тяжелых металлов. Для
всех
- аминокислот очень характерны красиво
кристаллизующиеся, интенсивно окрашенные
в синий цвет внутрикомплексные (хелатные)
соли меди ):

медная соль глицина
2 Образование сложных эфиров. При действии на - аминокислоту спиртом в присутствии кислотного катализатора (газообразный HCl) образуются сложные эфиры (в виде гидрохлоридов). Для выделения свободных эфиров реакционную смесь обрабатывают газообразным аммиаком:
 Этиловый
эфир аланина
Этиловый
эфир аланина
Образование сложных эфиров - один из методов защиты карбоксильной группы в синтезе пептидов.
3.Образование галогенангидридов. При действии на - аминокислоты с защищенной аминогруппой оксидихлоридом серы ( тионилхлоридом ) или оксид-трихлоридом фосфора ( хлорокисью фосфора ) образуются хлорангидриды:
П олучение
галогенангидридов - один из способов
активации карбоксильной группы в
пептидном синтезе.
олучение
галогенангидридов - один из способов
активации карбоксильной группы в
пептидном синтезе.
4.Получение ангидридов - аминокислот. Галогенангидриды обладают очень высокой реакционной способностью, что снижает селективность реакции при их использовании. Поэтому более часто используемый способ активации карбоксильной группы в синтезе пептидов - это превращение ее в ангидридную. Ангидриды по сравнению с галогенангидридами кислот обладают меньшей активностью. При взаимодействии - аминокислоты, имеющей защищенную аминогруппу, с этиловым эфиром хлормуравьиной кислоты(этилхлорформиатом) образуется ангидридная связь:
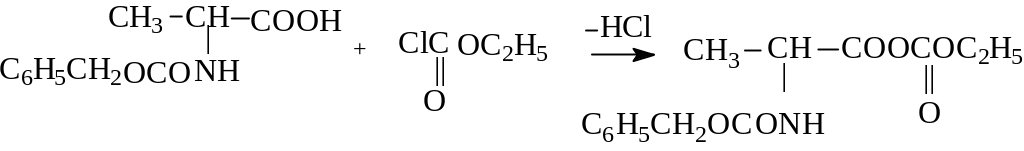 5.
Декарбоксилирование.
- Аминокислоты, имеющие две
электроноакцепторные группы при одном
и том же атоме углерода, легко
декарбоксилируются. В лабораторных
условиях это осуществляется при
нагревании аминокислот с гидроксидом
бария.Эта реакция протекает в организме
при участии ферментов декарбоксилаз с
образованием биогенных аминов:
5.
Декарбоксилирование.
- Аминокислоты, имеющие две
электроноакцепторные группы при одном
и том же атоме углерода, легко
декарбоксилируются. В лабораторных
условиях это осуществляется при
нагревании аминокислот с гидроксидом
бария.Эта реакция протекает в организме
при участии ферментов декарбоксилаз с
образованием биогенных аминов:

2-аминоэтанол ( коламин )
Качественная реакция на - аминокислоты. В качестве специфического реактива на - аминокислоты используется нингидрин. При нагревании его с - аминокислотами возникает фиолетовое окрашивание разных оттенков.
н ингидрин
ингидрин
Отношение аминокислот к нагреванию. При нагревании - аминокислот образуются циклические амиды, называемые дикетопиперазинами:
Д икетопиперазин
икетопиперазин
 -
Аминокислоты при нагревании образуют
,
-
- ненасыщенные кислоты с отщеплением
аммиака:
-
Аминокислоты при нагревании образуют
,
-
- ненасыщенные кислоты с отщеплением
аммиака:
 -
и
- Аминокислоты легко отщепляют воду и
циклизуются с образованием внутренних
амидов, лактамов:
-
и
- Аминокислоты легко отщепляют воду и
циклизуются с образованием внутренних
амидов, лактамов:
- лактам ( бутиролактам )
В тех случаях, когда амино - и карбоксильная группы разделены пятью и более углеродными атомами, при нагревании происходит поликонденсация с образованием полимерных полиамидных цепей с отщеплением молекулы воды.



