
Санкт-Петербургский Государственный Университет
Химический Факультет
Реферат по предмету «Химические основы экотоксикологии»:
Алюминий в окружающей среде
Выполнила: студентка VI курса
Ясакова О.Г.
Преподаватель: Бессонова Е.А.
Санкт-Петербург
2012 г
Оглавление
Введение . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Источники и пути поступления алюминия в окружающую среду. . . . . . . . . . . . . . . . . . . . . .4
Методы определения алюминия . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .5
Фотометрические методики . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .-
Флуориметрические методики. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .6
Методы атомно-абсорбционного спектрального анализа . . . . . . . . . . . . . . . . . . . . . . .7
Титриметрические методы . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .-
Сравнительная характеристика методов определения. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .9
Литература . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .10
Введение
Алюминий по распространенности в земной коре занимает третье место после кислорода и кремния. Его содержание в земной коре составляет 8,8% по массе. В природе встречается исключительно в виде соединений. Наиболее распространенные из них – глинозем, полевой шпат, слюда, бокситы. Содержание алюминия в почвах колеблется от 150 до 600 мг/кг, в атмосферном воздухе городов около 10 мкг/м3. Накоплению алюминия в почве содействует ее закисление. Содержание алюминия в водоисточниках колеблется в широких пределах от 2,5 до 121 мкг/л [1,2].
Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. Наиболее ядовиты хлориды, нитраты, ацетаты, сульфаты и др. В первую очередь действует на центральную нервную систему [3].
Источники и пути поступления алюминия в окружающую среду
Алюминий попадает в природные воды естественным путем при частичном растворении глин и алюмосиликатов, а также в результате вредных выбросов отдельных производств (электротехническая, авиационная, химическая и нефтеперерабатывающая промышленность, машиностроение, строительство, оптика, ракетная и атомная техника) с атмосферными осадками или сточными водами. Соли алюминия также широко используются в качестве коагулянтов в процессах водоподготовки для коммунальных нужд [4].
Методы определения алюминия Фотометрические методики
А) Определение с алюминоном
Максимум полосы поглощения комплекса алюминона с алюминием находится по разным данным от 528 до 540 нм. Водный раствор алюминона при этих длинах волн почти не поглощает. Алюминий и алюминон входят в комплекс в соотношении 1:1. Строение алюминона и его комплекса с Al можно представить следующими формулами:
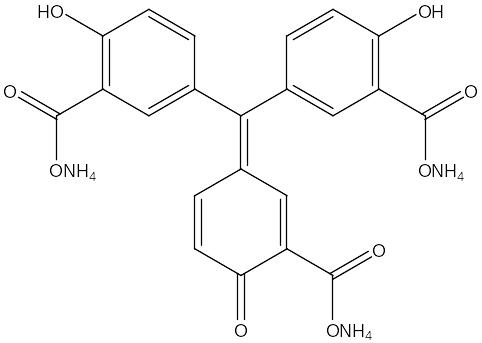

Алюминон Комплекс алюминона с алюминием
Реакция проводится в слабокислой среде: рН = 4,4 – 4,7. Алюминон – неспецифический реагент на алюминий. Многие элементы с алюминоном дают окрашенные соединения. Наибольшие помехи при анализе проявляются со стороны Fe(III). При длине волны 525 нм комплекс алюминона с трехвалентным железом окрашен в 2,5 раза меньше, чем соединение алюминия. Влияние небольших количеств Fe(III) устраняется восстановлением до Fe(II) тиогликолевой кислотой, аскорбиновой кислотой или гидроксиламином. При обычной температуре окраска комплекса развивается медленно, нагревание ускоряет ее развитие. Поэтому при проведении анализа следует либо производить измерение аналитического сигнала через строго определенное время после начала реакции, либо перед измерением аналитического сигнала производить нагревание раствора на кипящей водяной бане в течение 5 минут. Диапазон определяемых концентрация колеблется от 0,04 до 0,4 мг/л [1].
Б) Определение с хромазуролом S
Хромазурол S является одним из самых чувствительных реагентов на алюминий. При их взаимодействии при разных значениях рН образуются комплексы с разным соотношением реагентов. При рН > 3,5 алюминий и хромазурол S входят в комплекс в соотношении 1:2, а при рН < 3 образуется другой комплекс состава 1:1. Для аналитического определения обычно используется комплекс состава 1:2, дающий максимум поглощения при 545 нм. При этой длине волны водный раствор чистого хромазурола S практически не поглощает. Формула хромазурола S:
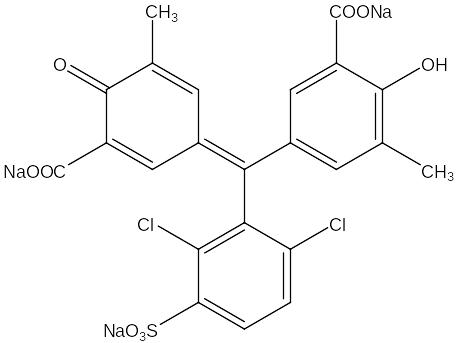
Окраска раствора комплекса развивается быстро. Для достижения максимальной окраски достаточно 10 минут, в дальнейшем окраска устойчива в течение продолжительного времени. Интенсивность окраски не зависит от изменения температуры в широких пределах. Оптимальной средой для проведения анализа считается рН = 5,7 – 5,8. В этой области зависимость оптической плотности от рН незначительна. Кроме того, при этих рН реагент поглощает мало, в то время как при рН от 3 до 5,5 реагент сильно окрашен. Определению алюминия по данной методике главным образом мешают Fe(III), Cu(II). Маскирование железа производят аскорбиновой или тиогликолевой кислотами. Влияние меди устраняется тиогликолевой кислотой или тиосульфатом. Чувствительность метода 0,006 мг/л. График зависимости оптической плотности от количества алюминия прямолинеен до 1 мг/л[1].
Так же для фотоместрического определения алюминия используются такие реагенты как эриохромцианин R, ксиленоловый оранжевый, метилтимоловый синий и другие. Общая воспроизводимость всех фотометрических методов составляет от 1 до 5 % [1].
