
- •1. Аналитическая атомная спектроскопия
- •1.1. Метод эмиссионной фотометрии пламени
- •1.1.1. Физические основы
- •1.1.2. Аппаратурное оформление
- •1.1.3. Аналитические возможности
- •Работа №1. Определение натрия и калия при совместном присутствии способом градуировочного графика
- •Работа №2. Определение натрия и калия в минеральной воде способом ограничивающих растворов
- •1.2. Пламенный атомно-абсорбционный метод анализа
- •1.2.1. Физические основы
- •1.2.2. Аппаратурное оформление
- •1.2.3. Аналитические возможности
- •Работа №3. Определение меди в природной воде способом градуировочного графика
- •1.3. Рентгенофлуоресцентный метод анализа
- •1.3.1. Физические основы
- •1.3.2. Аппаратурное оформление
- •1.3.3. Аналитические возможности
- •Работа №4. Качественный анализ образца латуни
- •Работа №5. Определение примесей в образце стали способом градуировочного графика
- •2. Аналитическая молекулярная спектроскопия
- •2.1. Спектрофотометрический метод анализа
- •2.1.1. Физические основы
- •2.1.2. Аппаратурное оформление
- •2.1.3. Аналитические возможности
- •Работа №6. Определение никеля в виде комплекса с диметилглиоксимом в присутствии окислителей
- •Работа №7. Определение хрома в виде комплекса с дифенилкарбазоном
- •Работа №8. Определение аналитической концентрации метилового оранжевого в растворах различной кислотности
- •Работа №9. Определение константы кислотной диссоциации фенолового красного (фенолсульфофталеина)
- •2.2. Флуориметрический метод анализа
- •2.2.1. Физические основы
- •2.2.2. Аппаратурное оформление
- •2.2.3. Аналитические возможности
- •Работа №10. Проверка правила зеркальной симметрии спектров поглощения и флуоресценции рибофлавина
- •Работа №11. Определение рибофлавина в инъекционном растворе способом градуировочного графика
- •7. Спектральное оборудование для выполнения практических работ
- •7.1. Пламенный фотометр Jenway pfp7
- •7.1.1. Технические характеристики
- •7.1.2. Порядок работы
- •Капилляр для подачи жидкой пробы в пламя газовой горелки должен быть погружён в химический стакан ёмкостью 100 – 150 мл с дистиллированной водой.
- •7.2. Пламенный спектрофотометр квант-2а
- •7.2.1. Технические характеристики
- •7.2.2. Порядок работы
- •7.3. Рентгенофлуоресцентный спектрометр Спектроскан макс-gf2e
- •7.3.1. Технические характеристики
- •7.3.2. Порядок работы
- •7.4. Нерегистрирующий спектрофотометр Leki ss1207
- •7.4.1. Технические характеристики
- •7.4.2. Порядок работы
- •7.5. Регистрирующий спектрофотометр unico uv-2804
- •7.5.1. Технические характеристики
- •7.5.2. Порядок работы
- •7.6. Спектрофлуориметр Флюорат-02-Панорама
- •7.6.1. Технические характеристики
- •7.6.2. Порядок работы
Работа №7. Определение хрома в виде комплекса с дифенилкарбазоном
Дифенилкарбазид в кислой среде взаимодействует с хромом (VI) с образованием растворимого соединения красно-фиолетового цвета. В спектре поглощения продукта реакции наблюдается интенсивная полоса с λmax = 546 нм и εmax = 4,2.104. Эту фотометрическую реакцию изучали неоднократно, однако механизм её до конца не выяснен. Предполагают, что сначала дихромат-ион окисляет дифенилкарбазид до дифенилкарбазона:
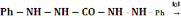
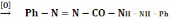
Образующиеся в результате этой окислительно-восстановительной реакции продукты Cr(III) и дифенилкарбазон далее взаимодействуют друг с другом с образованием хелата неустановленного состава. В ряде исследований высказывается точка зрения, что соотношение Cr(III) : дифенилкарбазон в хелате равно 1:1. В пользу такого механизма свидетельствует тот факт, что спектр поглощения соединения, образующегося из Cr(VI) и дифенилкарбазида, совпадает со спектром поглощения соединения Cr(III) с дифенилкарбазоном. Однако раствор Cr(III) нельзя использовать для анализа, так как его кинетически инертные аква- и галогенаквакомплексы взаимодействую с дифенилкарбазоном крайне медленно. В то же время при реакции с хромат- или дихромат-ионом хелат образуется мгновенно. Установлено, что на интенсивность окраски образующегося хелата существенное влияние оказывают чистота реагента и кислотность раствора. Оптимальной является кислотность 0,05 – 0,1 М по серной кислоте. Не следует использовать для подкисления соляную кислоту. Реакция Cr(VI) и дифенилкарбазидом очень чувствительна и достаточно селективна. Подобно Cr(VI) и дифенилкарбазидом реагирует Mo(VI), но реакция менее чувствительна. Окрашенные соединения с реагентом способны давать Fe(III) и V(V).
Реагенты и аппаратура
Стандартный раствор дихромата калия с содержанием хрома 0,01 мг/мл
Дифенилкарбазид, 0,25%-ный водно-ацетоновый (1:1) раствор
Серная кислота, 3 М раствор
Спектрофотометр Leki SS1207
Выполнение определения
В мерную колбу ёмкостью 50,0 мл вводят стандартный раствор дихромата калия с содержанием хрома 0,03 мг, 20 мл воды, 2 мл раствора серной кислоты, 1 мл раствора дифенилкарбазида. Содержимое колбы разбавляют водой до метки. Раствор фотометрируют в интервале длин волн от 500 до 600 нм с шагом 10 нм. Полученный массив данных используют для построения спектра поглощения в координатах A(λ) и T(λ). Полученные спектры используют для экспериментального нахождения максимума полосы поглощения.
Затем, используя процедуру, описанную выше, готовят 5 стандартных растворов дихромата калия с содержанием хрома 0,01; 0,02; 0,03; 0,04 и 0,05 мг соответственно. Растворы фотометрируют на выбранной длине волны относительно воды и строят градуировочный график. Для определения хрома в анализируемом растворе аликвоту этого раствора помещают в мерную колбу ёмкостью 50,0 мл. С раствором проводят те же операции и в той же последовательности, что и приготовлении растворов, используемых для градуировки, а затем фотометрируют относительно воды. Содержание хрома находят по градуировочному графику.
