
Температура
Температура – это:
макроскопическая характеристика теплового движения.
Температура есть мера содержащегося в теле тепла. Она же определяет направление перехода тепла — от более нагретого тела к менее нагретому. Если температуры тел одинаковы, то передачи тепла от одного тела к другому не происходит.
Температура – это мера средней кинетической энергии хаотического движения молекул.
Средняя кинетическая энергия одной молекулы:
![]() .
(1)
.
(1)
Следовательно, абсолютная температура:
![]() ,
(2)
,
(2)
где
![]() - постоянная Больцмана.
- постоянная Больцмана.
Принятая в физике шкала температур называется абсолютной шкалой, или шкалой Кельвина. В этой шкале температура замерзания воды, то есть 0°С, соответствует 273,15 градусов Кельвина, что обозначается 273,15 К. При T = 0 всякое тепловое движение частиц в веществе прекращается. Эта температура имеет название абсолютного нуля.
![]() (3)
(3)
Подчеркнем статистический характер определения температуры, поскольку она связана со средней энергией частиц. Поэтому можно говорить лишь о температуре системы достаточно большого числа частиц — макроскопической системы, и нельзя говорить о температуре одной или, допустим, десяти частиц. В процессе измерения температуры происходит обмен теплом между системой частиц — объектом измерения и измерительным прибором — термометром. Понятие температуры тела приобретает смысл в том случае, если обмен теплом между телом и прибором в процессе измерения температуры мало изменяет состояние тела.
Функция распределения Максвелла
Распределение скоростей молекул по Максвеллу.
Молекулы идеального газа совершают беспорядочное тепловое движение. Ввиду полной беспорядочности движения молекул и огромного их числа нет возможности судить о скорости каждой молекулы в любой момент времени. Возможно определить лишь число молекул, скорости которых лежат в определенном интервале скоростей.
Теоретически задачу о распределении молекул идеального газа по скоростям поступательного движения решил Максвелл. Он показал, что число молекул, имеющих малые скорости и большие скорости относительно мало. Оказывается, что скорости большинства молекул лежат в окрестности некоторой средней скорости. С помощью теории вероятностей (1859) Максвеллу удалось вывести формулу для относительной частоты, с которой в газе при данной температуре встречаются молекулы со скоростями в определенном интервале значений.
Если N - общее число молекул газа,
![]() - число молекул, скорости которых
заключены в интервале от
до +d
, то закон распределения
Максвелла запишется в виде:
- число молекул, скорости которых
заключены в интервале от
до +d
, то закон распределения
Максвелла запишется в виде:
![]() .
(1)
.
(1)
Функция
![]() ,
определяемая выражением (1), представляет
собой плотность вероятности того, что
частицы имеют заданное значение
абсолютной величины скорости.
,
определяемая выражением (1), представляет
собой плотность вероятности того, что
частицы имеют заданное значение
абсолютной величины скорости.
Итак, плотность вероятности имеет вид:
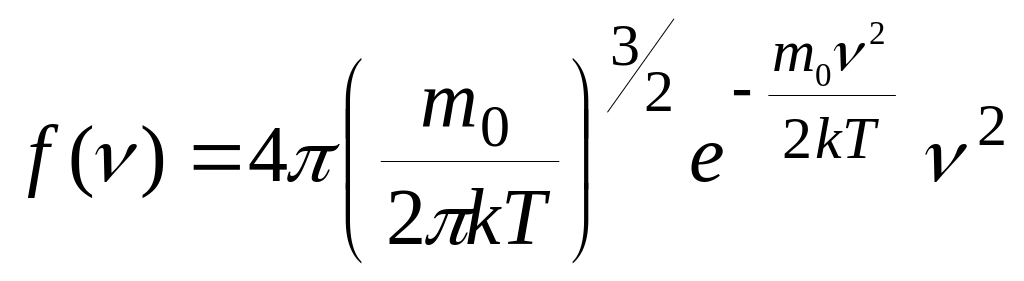 (2)
(2)
Здесь f()– функция распределения Максвелла. Она указывает долю молекул dN/N, обладающих скоростями, лежащими в интервале dv около значения скорости v. Из этой формулы видно, что конкретный вид функции зависит от рода газа (m) и от параметров состояния (Т).
![]() уменьшается быстрее, чем растет множитель
v2, то функция
уменьшается быстрее, чем растет множитель
v2, то функция
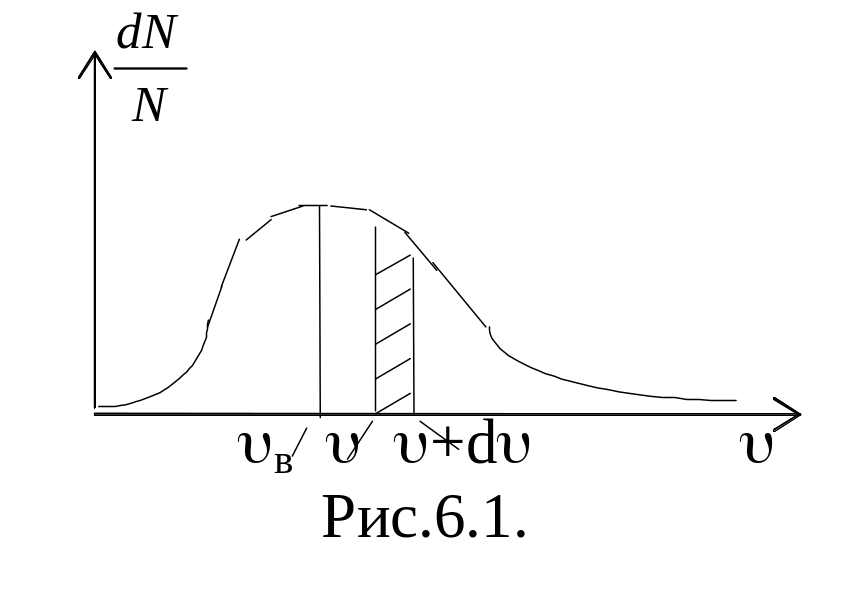
![]() ,
начинаясь от нуля, достигает максимума
при vв и
затем асимптотически стремится к нулю.
Положение максимума характеризует
наиболее часто встречающуюся скорость,
которую называют наиболее вероятной
скоростью в.
Скорости, превышающие в,
встречаются чаще, чем меньшие скорости.
Кривая асимметрична относительно в.
,
начинаясь от нуля, достигает максимума
при vв и
затем асимптотически стремится к нулю.
Положение максимума характеризует
наиболее часто встречающуюся скорость,
которую называют наиболее вероятной
скоростью в.
Скорости, превышающие в,
встречаются чаще, чем меньшие скорости.
Кривая асимметрична относительно в.
Относительное число молекул, скорости которых находятся в интервале от до +d, находится как площадь заштрихованной полоски. Площадь, ограниченная кривой распределения и осью абсцисс, равна единице. Это означает, что f() удовлетворяет условию нормировки:
![]() .
.

