
Описание установки.
Исследование спектра излучения водорода в данной работе производится с помощью монохроматора УМ-2. Монохроматор выделяет монохроматические участки спектра в видимой и инфракрасной областях в диапазоне длин волн от 380 до 1000 нм (1 мкм = 10-6м, 1 нм = 10-9м). Если на входную щель направить сложный свет, то на выходе получается спектр. В монохроматоре на выходе ставят еще одну щель, которая выделяет из спектра только лучи определенной длины волны. Но в данной работе выходная щель удалена и с помощью окуляра можно наблюдать спектр (или отдельные его части), т.е. монохроматор используется как спектроскоп.
В работе используется стеклянно-призменный
монохроматор УМ2,
предназначенный
для спектральных исследований в диапазоне
от 3800 до 10000 Å. В состав прибора входят
следующие основные части (рис. 3).
работе используется стеклянно-призменный
монохроматор УМ2,
предназначенный
для спектральных исследований в диапазоне
от 3800 до 10000 Å. В состав прибора входят
следующие основные части (рис. 3).
В
Рис. 2
Задания и указания к их выполнению
Задание 1. Ознакомиться с устройством монохроматора. Выяснить назначение ручек управления.
Задание 2. Перейдите непосредственно к измерениям.
Проградуируйте деления барабана монохроматора в значениях длин волн. Используйте для этого известный спектр ртути.
Для этого, осветите входную щель спектроскопа светом от ртутной лампы (включать только под наблюдением лаборанта!). Сделайте щель узкой и пронаблюдайте в окуляр спектр. Линии должны быть яркими и узкими.
Занесите в таблицу 1 значения делений барабана для наблюдаемых линий и укажите цвет каждой линии. Следует иметь в виду, что установка указателя на барабане может сбиваться (указатель может соскочить на соседнюю дорожку).
Таблица 1
№ |
Цвет линии |
Длина волны , нм |
Показания шкалы барабана L, град. |
1. |
Темно красная слабая |
623.43 |
|
2. |
Светло желтые: 1 ая 2 ая |
579.06 576.96 |
|
3. |
Зеленая |
546.07 |
|
4. |
Зелено голубые: 1 ая 2 ая |
496.03 491.60 |
|
5. |
Синяя |
435.83 |
|
6. |
Фиолетовые: 1 ая 2 ая |
407.78 404.65 |
|
Постройте по спектру ртути градуировочную кривую, отложив по горизонтали деления барабана, а по вертикали – значения длин волн.
Задание 3. Поставьте теперь в качестве источника света трубку с водородом ТВС-15, через которую пропускается ток от питающего устройства ОУ-2.
Занесите в таблицу 2 значения делений барабана для наиболее ярких линий водорода.
Пользуясь градуировочной кривой, переведите эти значения в длины волн. Сравните экспериментальные данные с рассчитанными по формуле (5), т.е. с теоретическими значениями. Объясните возможные причины погрешностей экспериментальных данных.
Укажите, каким переходам на энергетической диаграмме на рисунке 2 соответствуют наблюдаемые вами линии.
Таблица 2
№ |
Цвет линии |
Показания шкалы барабана L, град. |
Длина волны , нм |
Длина волны, рассчитанная по формуле (5), нм |
1. |
|
|
|
|
2. |
|
|
|
|
3. |
|
|
|
|
4. |
|
|
|
|
Контрольная карточка № 1.
Перечислите серии спектра водорода. Какому переходу соответствует головная линия в каждой серии?
О
 ценить
скорость движения электрона в атоме
согласно модели Бора.
ценить
скорость движения электрона в атоме
согласно модели Бора.
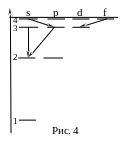
В энергетическом спектре атома водорода (рис. 4) какой переход является запрещенным?
Атом водорода излучил квант света с длиной волны λ = 6,65 10-7 м. Во сколько раз изменился при этом радиус электронной орбиты?
Вычислить энергию фотона ε, испускаемого при переходе электрона в атоме водорода с третьего уровня на первый.
Контрольная карточка № 2
Запишите формулу Бора для каждой серии спектра водорода.
В каком диапазоне электромагнитных волн находятся линии серии Бальмера?
Электрон в атоме водорода перешел из основного состояния в возбужденное, получив энергию Е=12,8 эВ. Какую наибольшую длину волны может теперь излучить атом водорода?
Определить наибольшую и наименьшую энергию фотонов в серии Лаймана спектра водорода.
Найти радиусы трех первых боровских электронных орбит в атоме водорода и скорости электрона на них.
Контрольная карточка № 3
Определить длину волны λ, соответствующую третьей спектральной линии в серии Бальмера.
Найти наибольшую λmax и наименьшую λmin длины волн в первой инфракрасной серии спектра водорода (серии Пашена).
Вычислить радиусы второй и третьей орбит в атоме водорода.
Определить частоту обращения электрона на второй орбите атома водорода.
Найти наибольшую длину волны в ультрафиолетовой области спектра водорода. Какую наименьшую скорость должны иметь электроны, чтобы при возбуждении атомов водорода ударами электронов появилась эта линия?
Контрольная карточка № 4
Оценить длину волны де-Бройля для электрона на каком-либо конкретном уровне, сравнить ее с радиусом орбиты. Объяснить полученный результат.
В каком диапазоне может лежать излучение положительного атомарного иона водорода?
Определить скорость электрона на второй орбите атома водорода.
Определить угловую скорость электрона на первой боровской орбите атома водорода.
Найти кинетическую, потенциальную и полную энергии электрона на первой боровской орбите.
