
- •Общие сведения о горении
- •1.1. Введение
- •1.2. Основные понятия
- •1.3. Горение и условия его протекания
- •1.4. Понятие о кинетическом и диффузионном горении
- •1.5. Химические реакции горения
- •1.6. Горение в атмосферном воздухе
- •1.7. Классификация и характеристика пожароопасных веществ [3]
- •Трудногорючие вещества
- •Негорючие вещества
- •1.8. Показатели пожаро- и взрывоопасности веществ и материалов
- •Особенности горения различных веществ
- •2.1. Горение газов
- •Влияние температуры смеси
- •Влияние давления смеси
- •Влажность воздуха
- •Содержание примесей, замедляющих реакции горения
- •Температура горения
- •2.2. Горение жидкостей
- •Криогенные вещества – вещества, у которых критическая температура ниже температуры окружающей среды. Хранение и транспортировка их – в криогенных сосудах.
- •2.3. Горение твердых веществ
- •Горение древесины
- •Горение полимерных материалов
- •Скорость горения органических веществ
- •2.4. Горение пылевоздушных смесей
- •Горючие пыли
- •Взрывоопасные
- •Пожароопасные
- •3. Общие сведения о взрыве
- •3.1. Взрыв и его разновидности
- •3.2. Классификация взрывных явлений
- •Классификация взрывов
- •Атомные группировки, сообщающие соединению взрывчатость
- •3.3. Характеристика аварийных взрывов
- •4. Общие сведения о взрывчатых веществах (вв)
- •4.1. Основные понятия
- •Формы взрывчатого превращения
- •4.2. Классификация взрывчатых веществ
- •4.3. Характеристика взрывчатых веществ
- •Температура вспышки и чувствительность к удару
- •Характеристика взрывчатых веществ
- •4.4. Химические реакции взрывных превращений
- •4.5. Объем продуктов взрывчатого разложения
- •4.6. Теплота и температура взрыва
- •4.7. Давление продуктов взрыва
1.5. Химические реакции горения
Горение – сложный физико-химический процесс, основу которого составляют химические реакции окислительно-восстановительного типа, приводящие к перераспределению валентных электронов между атомами взаимодействующих молекул.
Примеры реакций горения
метана: СН4 + 2О2 = СО2 + 2Н2О;
ацетилена: С2Н2 + 2,5О2 = 2СО2 + Н2О;
натрия: 2Na + Cl2 = 2NaCl;
водорода: Н2 + Cl2 = 2НCl, 2Н2 + О2 = 2Н2О;
тротила: С6Н2(NO2)3CH3 = 2,5H2O + 3,5CO + 3,5C +1,5N2.
Сущность окисления – отдача окисляющимся веществом валентных электронов окислителю, который, принимая электроны, восстанавливается, Сущность восстановления – присоединение восстанавливающимся веществом электронов восстановителя, который, отдавая электроны, окисляется. В результате передачи электронов изменяется структура внешнего (валентного) электронного уровня атома. Каждый атом при этом переходит в наиболее устойчивое в данных условиях состояние.
В химических процессах электроны могут полностью переходить из электронной оболочки атомов одного вещества (элемента) в оболочку атомов другого.
Так, при горении металлического натрия в хлоре атомы натрия отдают по одному электрону атомам хлора. При этом на внешнем электронном уровне атома натрия оказывается восемь электронов (устойчивая структура), а атом, лишившийся одного электрона, превращается в положительно заряженный ион. У атома хлора, получившего один электрон, внешний уровень заполняется восемью электронами, и атом превращается в отрицательно заряженный ион. В результате действия кулоновских электростатических сил происходит сближение разноименно заряженных ионов и образуется молекула хлорида натрия (ионная связь):
Na+ + Cl– = Na+Cl– или 2Na + Cl2 = 2Na+Cl–.
Атом магния имеет в наружном слое два электрона. При взаимодействии с кислородом два атома магния отдают четыре электрона молекуле (двум атомам) кислорода и превращаются в положительные двухзарядные ионы. Последние связываются с образовавшимися отрицательно заряженными ионами кислорода в кристаллы оксида магния MgO:
4е–

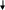

2Mg + O2 = 2Mg2+O2–.
Таким образом, горение магния (окисление) сопровождается переходом его электронов к кислороду. В других процессах электроны внешних оболочек двух разных атомов поступают как бы в общее пользование, стягивая тем самым атомы молекул (ковалентная или атомная связь):
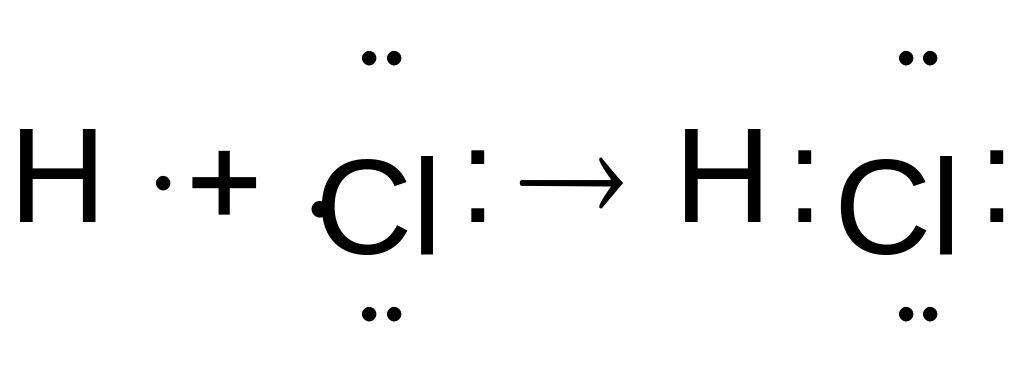 .
.
И, наконец, один атом может отдавать в общее пользование свою пару электронов (молекулярная связь):
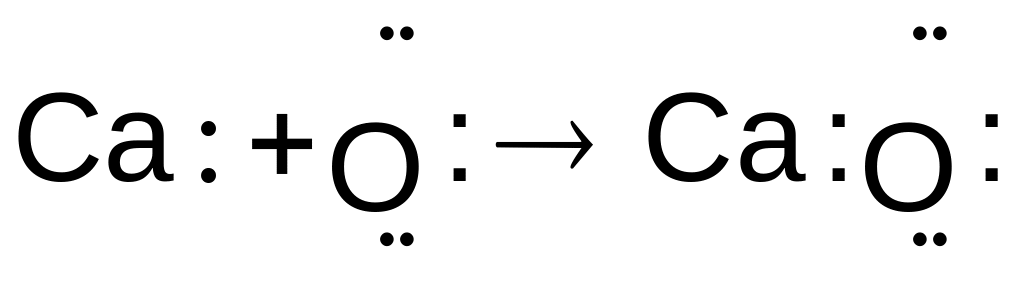 .
.
Выводы из положений современной теории окисления–восстановления:
Сущность окисления заключается в потере электронов атомами или ионами окисляющегося вещества, а сущность восстановления – в присоединении электронов к атомам или ионами восстанавливающегося вещества. Процесс, при котором вещество теряет электроны, называется окислением, а присоединение электронов – восстановление.
Окисление какого-либо вещества не может произойти без одновременного восстановления другого вещества. Например, при горении магния в кислороде или воздухе происходит окисление магния и одновременно – восстановление кислорода. При полном сгорании образуются продукты, неспособные к дальнейшему горению (СО2, Н2О, НСl и т.д.), при неполном – получившиеся продукты способны к дальнейшему горению (CO, H2S, HCN, NH3, альдегиды и т.д.). Схема: спирт – альдегид – кислота.
В условиях пожара при горении органических веществ в воздухе чаще всего полного сгорания не происходит. Признаком неполного сгорания является наличие дыма, содержащего несгоревшие частицы углерода.
