
- •Аннотация
- •1. Введение
- •1.1 Общие правила выполнения лабораторных работ.
- •1.2. Лабораторное оборудование.
- •1.3 Вычисления.
- •1.4 Количество и концентрация вещества.
- •Общие указания по выполнению лабораторных работ.
- •Работа 1. Ознакомление с некоторыми операциями лабораторной практики и измерительными приборами.
- •Работа 2. Классы неорганических соединений.
- •Работа 3. Определение молярной массы диоксида углерода.
- •Работа 4. Электронная структура атомов и одноатомных ионов.
- •Работа 5. Кинетика химических реакций.
- •Работа 6. Химическое и адсорбционное равновесие.
- •Работа 7. Концентрация растворов.
- •Работа 8. Свойство водных растворов электролитов.
- •Работа 9.Гидролиз солей.
- •Работа 10. Окислительно-восстановительные реакции.
- •Работа 11. Основы электрохимии.
- •Работа 12. Электролиз.
- •Работа 13. Общие химические свойства металлов.
- •Работа 14. Свойства d-элементов 4-го периода.
- •Работа 15. Свойства элементов, применяемых в полупроводниковой технике.
- •Работа 16. Определение жесткости и умягчение воды.
- •Работ 17 Органические соединения.
- •Работа. 18. Свойства элементов подгруппыViв иViiв
- •Работа 19. Свойства элементов подгруппыViiib.
- •Работа 20. Свойства элементов подгруппыIva.
- •Работа 21, Свойства элементовVAиVia.
Работа 7. Концентрация растворов.
Цель работы - приобретение навыков приготовления растворов различной концентрации из сухой соли или более концентрированного раствора.
Приведем несколько примеров расчета по теме "Концентрации растворов".
Пример
1. Рассчитайте молярную концентрацию,
титр и массовую долю (в %)
![]() в 2М растворе, плотность которого
1,12г/см3.
в 2М растворе, плотность которого
1,12г/см3.
Решение.
а)
Молярная масса
![]() равна 98 г/моль. Так как 1м раствора
равна 98 г/моль. Так как 1м раствора
![]() содержит 2 моля эквивалентов кислоты,
а в 2м раствор - 4, раствор будет
четырехнормальный (4н).
содержит 2 моля эквивалентов кислоты,
а в 2м раствор - 4, раствор будет
четырехнормальный (4н).
б)
Для определения массовой доли (в %)
![]() необходимо найти массу 1л 2М раствора
необходимо найти массу 1л 2М раствора![]() :
:
![]()
Зная,
что в литре 2М раствора содержится 196г
![]() ,
определяем массу кислоты в 100г раствора:
,
определяем массу кислоты в 100г раствора:
1120г раствора содержит 196г кислоты
100г Х г кислоты
Х = 17г. Следовательно, массовая доля кислоты в растворе составляет 17%.
Пример
2. Сколько граммов
![]() и воды потребуется для приготовления
40 г раствора, с массовой долей
и воды потребуется для приготовления
40 г раствора, с массовой долей![]() 10%:
10%:
100
г раствора содержит 10 г
![]()
40
г раствора содержит Х г
![]()
![]()
Вычисляем
массу кристаллогидрата
![]() ,
в котором содержится 4 г безводной соли
(молярная масса
,
в котором содержится 4 г безводной соли
(молярная масса![]() - 142 г/моль,
- 142 г/моль,![]() - 322 г/моль):
- 322 г/моль):
322
г
![]() содержит 142 г
содержит 142 г![]()
Х
г
![]() содержит 4 г
содержит 4 г![]()
![]()
Масса
воды, необходимая для приготовления 40
г раствора с массовой долей
![]() 10% равна: 40 - 9,07 = 30,93 г.
10% равна: 40 - 9,07 = 30,93 г.
Экспериментальная часть.
ОПЫТ 1. Приготовление раствора заданной молярности из навески твердого вещества.
а)
Получите у преподавателя задание на
приготовление раствора соли (![]() или
или![]() )
заданной концентрации.
)
заданной концентрации.
б)
Вычислите требуемое количество соли и
отвесьте на технических весах с точностью
до 0,01 г. Примечание: молярную массу буры
рассчитайте исходя из молярной массы
кристаллогидрата
![]() и реакции.
и реакции.
![]()
в) Осторожно перенести в мерную колбу навеску (навеску соли высыпать через сухую воронку, вставленную в горлышко колбы). Растворить соль в дистиллированной воде, заполнив сначала ее на 1/3. После растворения всей соли довести дистиллированной водой раствор до метки на шейке колбы. Закрыть колбу пробкой и тщательно перемешать раствор.
г) Определим точную концентрацию соли: - сухой пипеткой или ополоснутой раствором соли отмерить в две колбы по 10 мл раствора и добавить две капли индикатора метилоранжа;
-
в предварительно ополоснутую бюретку
налить раствор кислоты концентрация
которой точно - известна (0,1M
![]() )
)
- отобранный раствор титруйте из бюретки раствором кислоты с точно известной концентрацией до изменения окраски от желтой до оранжевой (сравнивая окрашивание с эталоном). Результат титрования запишите.
Повторите титрование. Результаты титрования не должны отличатся друг от друга более чем на 0,1 мл.
д) Вычислите молярную концентрацию и титр приготовленного раствора.
![]()
где
![]() - объем взятого раствора буры.
- объем взятого раствора буры.![]() - молярность раствора буры (искомая
величина)
- молярность раствора буры (искомая
величина)![]() - количество
- количество![]() ,
которое пошло на титрование раствора
буры.
,
которое пошло на титрование раствора
буры.![]() - молярность
- молярность![]() ,
взятой для титрования.
,
взятой для титрования.
Результаты опыта сведите в таблицу:
|
Молярная масса буры, М |
Масса соли для приготовления раствора, г |
|
Молярная концентрация приготовленного раствора | |||
|
1 |
2 |
среднее |
заданная |
полученная | ||
|
|
|
|
|
|
|
|
ОПЫТ 2. Приготовление раствора кислоты заданной молярности.
Получите у преподавателя задание на приготовление заданного объема раствора серной кислоты определенной концентрации.
а) Определим ареометром плотность раствора кислоты, и определите по таблице его процентную концентрацию.
б) Рассчитайте, какой объем концентрированной кислоты необходим для приготовления раствора заданной молярности.
в) Отметьте маленьким цилиндром подсчитанный объем концентрированного раствора и прилейте в мерную колбу. Цилиндр ополосните несколько раз водой. Раствор осторожно довести до метки и перемешать.
г) Сухой пипеткой отобрать в две колбы по 10 мл раствора соли, приготовленного ранее и добавить 2 капли индикатора метилоранжа.
д) В предварительно ополоснутую приготовленным раствором кислоты бюретку налить раствор до нулевого деления и протитровать отобранный раствор соли.
Вычислить молярную концентрацию приготовленного раствора. Уравнение реакции между серной кислотой и бурой:
![]()
Результаты опыта сведите в таблицу, аналогичную опыту 1.
Контрольные вопросы.
Назовите способы выражения концентрации растворов.
Что называется молярной концентрацией раствора?
В одном литре раствора содержится 10,6 г карбоната натрия
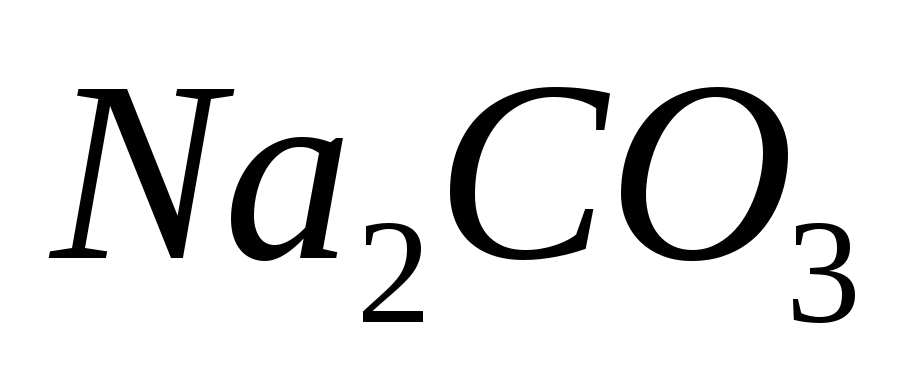 .
Рассчитайте молярную концентрацию.
Ответ: 0,1м.
.
Рассчитайте молярную концентрацию.
Ответ: 0,1м.Сколько граммов гидроксида натрия
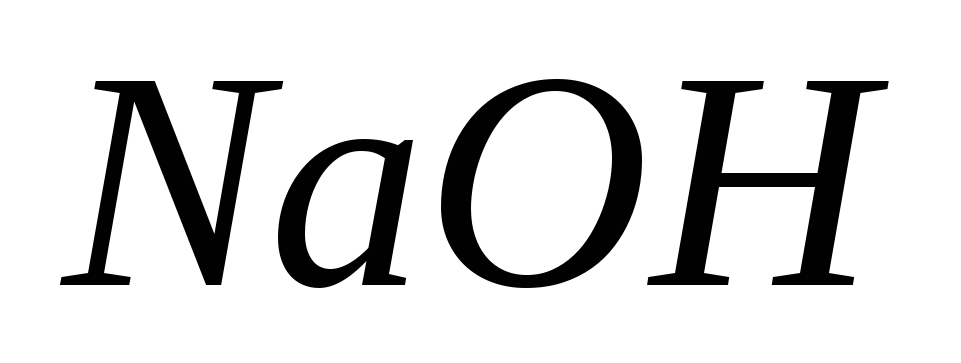 нужно взять, чтобы приготовить 5л 0,1м
раствора
нужно взять, чтобы приготовить 5л 0,1м
раствора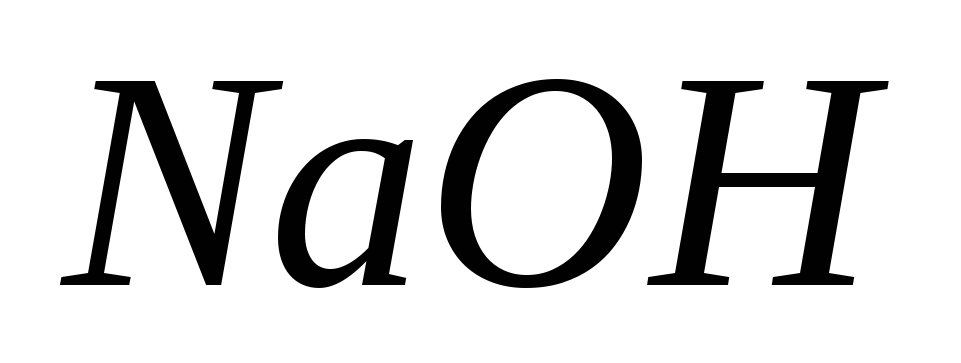 ?
Ответ: 20 г.
?
Ответ: 20 г.Сколько граммов тиосульфата натрия (
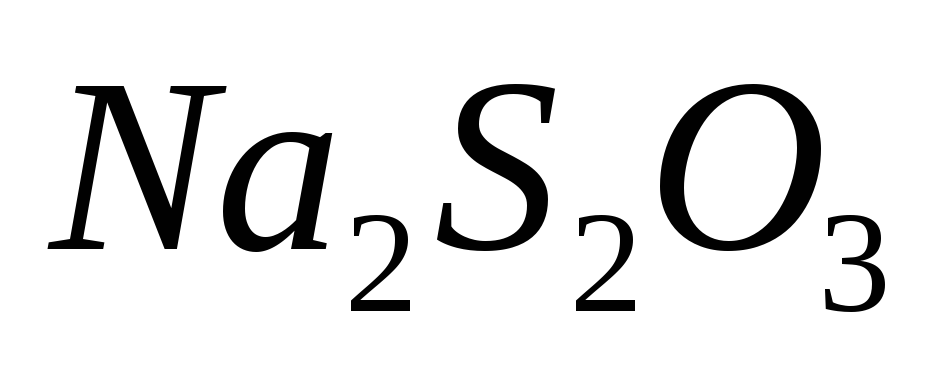 )
необходимо для приготовления 300 г
раствора, в котором массовая доля
тиосульфата натрия равна 5%? Ответ: 15 г.
)
необходимо для приготовления 300 г
раствора, в котором массовая доля
тиосульфата натрия равна 5%? Ответ: 15 г.Какой объем 0.1М раствора можно приготовить из двух литров 2.0 М раствора?
