
- •Физическая химия. Спец. 320700. Тест № 2
- •Физическая химия. Спец. 320700. Тест № 3
- •Физическая химия. Спец. 320700. Тест № 4
- •Физическая химия. Спец. 320700. Тест № 5
- •Физическая химия. Спец. 320700. Тест № 6
- •Физическая химия. Спец. 320700. Тест № 7
- •Физическая химия. Спец. 320700. Тест № 8
- •Физическая химия. Спец. 320700. Тест № 9
- •Физическая химия. Спец. 320700. Тест № 9
- •Физическая химия. Спец. 320700. Тест № 10
- •Физическая химия. Спец. 320700. Тест № 11
- •Физическая химия. Спец. 320700. Тест № 12
- •Физическая химия. Спец. 320700. Тест № 13
- •Физическая химия. Спец. 320700. Тест № 14
- •Физическая химия. Спец. 320700. Тест № 15
- •Физическая химия. Спец. 320700. Тест № 16
- •Физическая химия. Спец. 320700. Тест № 17
- •Физическая химия. Спец. 320700. Тест № 18
- •Физическая химия. Спец. 320700. Тест № 19
Физическая химия. Спец. 320700. Тест № 14
1. Уравнение Каммерлинг-Оннеса состояния реального газа:
1 ) 2) 3)
4) рV = nRT 5) р1V1 = р2V2
2. Экстенсивными (не зависящими от количества вещества) являются свойства: 1)плотность, температура 2)объем, давление 3)внутренняя энергия, объем 4)масса, температура 5)давление, плотность
3. Изменение энтропии в химической реакции при стандартных условиях рассчитывают по уравнению:
Sр-ции = S298(продукты) - S298(исх.реагенты)
Sр-ции = S298(исх.реагенты) - S298(продукты)
Sр-ции = Q р-ции /T
Sр-ции = Н р-ции /298
Sр-ции = k lnW
4.
Фундаментальное уравнение термодинамики, выраженное через естественные переменные V и Т:
1) dH = TdS + Vdp 2) dU = TdS – pdV 3) dF = - pdV – SdT 4) dH = dU + pdV
5) dG = Vdp - SdT
5. Если все участники химической реакции: А + 3В = С являются газами, то соотношение между КС и КР равно:
1) КР = КС(RT)-3 2) КР = КС(RT)+3 3) КР = КС(RT)+2 4) КР = КС(RT)-2
5 ) КР = КСRT.
6. Для точки E на диаграмме справедливо:
Одна жидкая фаза; число степеней свободы: с = 2
Две фазы – жидкая и твердая; с = 1
Две фазы – жидкая и твердая; с = 2
Три фазы; число степеней свободы: с = 0
Одна твердая фаза ; число степеней свободы: с = 2
7. Уравнение Вант-Гоффа для идеального раствора:
1) 2) Р = СRT 3)Tзам = Кm 4)Tкип = Еm 5) i = i + RTlnсi
8. ЭДС электрохимической цепи с учетом диффузионного потенциала будет:
1 ) 2) Е = к + А 3)
4) Е = к - А Д 5) Е = к - А
9. Электрохимический метод количественного определения содержания ионов в растворе называется:
1) кондуктометрия; 2) кулометрия; 3)ионометрия; 4)полярография;
5) вольтамперометрия.
10. Для реакции 2-ого порядка с неравными концентрациями реагентов основной кинетический закон в дифференциальной форме имеет вид
1) dx/dt = k(a-x) 2) dx/dt = k(a-x) 2 3) dx/dt = k(a-x)(b-x)
4) dx/dt = k(a-x) 3 5) kt =ln a/(a-x)
Физическая химия. Спец. 320700. Тест № 15
1. Работа расширения идеального газа в вакуум равна:
1) А = 0 2) А = p(V2-V1) 3) А = nRT ln(V2/V1) 4) А = nRT ln(V2/V1)
5) А = Q - U
2. Изменение энтальпии в химической реакции при стандартных условиях рассчитывают по уравнению
1) H298р-ции = H298(продукты) - H298(исх.реагенты)
2) H298р-ции = H298(исх.реагенты) - H298(продукты)
3)
4) H298р-ции = Hсгор.(продукты) - Hсгор.(исх.реагенты)
5) H298р-ции = H298(продукты) + H298(исх.реагенты)
3. Если стандартная энтальпия образования жидкой воды равна 258 кДж/моль, то энтальпия её разложения составляет:
1) + 516 кДж/моль 2) - 129 кДж/моль 3) - 516 кДж/моль 4) – 258 кДж/моль
5) + 258 кДж/моль
4. Фундаментальное уравнение термодинамики, выраженное через естественные переменные Р и Т:
1) dH = TdS + Vdp 2) dU = TdS – pdV 3) dF = - pdV – SdT 4) dH = dU + pdV
5) dG = Vdp - SdT
5. Уравнение Гиббса-Гельмгольца:
1) G = Н + Т(дG/дT)p 2) G = Н + ТS 3) F = U + ТS
4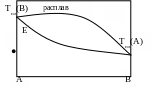 )
5) C = K – Ф
+ n
)
5) C = K – Ф
+ n
6. Для точки E на диаграмме справедливо:
Одна жидкая фаза А; число степеней свободы: с = 2 ●
Две фазы – жидкая и твердая; с = 1
Одна твердая фаза В; число степеней свободы: с = 1
Одна твердая фаза А ; число степеней свободы: с = 2
5) Одна твердая фаза А; число степеней свободы: с = 1
7. Закон разбавления Оствальда:
1) 2) Р = iСRT 3) 4)Tкип = iЕm 5) i = i + RTlnсi
8. Химическим условием фазового равновесия является:
1) ТiI = ТiII = ... = ТiФ 2) НiI = НiII = ... = НiФ
3) РiI = РiII = ... = РiФ 4) iI = iII = ... = iФ 5) ViI = ViII = ... = ViФ
9. Периодом полураспада t1/2 химической реакции является:
1) время, в течение которого первоначальная скорость реакции уменьшается в два раза;
2) время, в течение которого реагирует половина взятого количества вещества;
3) время достижения состояния химического равновесия;
4) время, в течение которого первоначальная константа скорости реакции уменьшается в два раза;
5) время, в течение которого выделяется половина расчетной для данной реакции теплоты.
10. Для реакции 1-ого порядка основной кинетический закон в интегральной форме имеет вид
1) kt = x/a(a-x) 2) kt = ½(a-x) 2 - 1/2a 2 3) kt = x
4) kt =[1/(a-b)]*ln[b(a-x)/a(b-x)] 5) kt =ln a/(a-x)
