
Выполнение работы.
Путем разбавления исх-го р-ра укс-й к-ты готовим в 6 колбах р-ры по 50 мл в каждой колбе (I - 50 мл неразб-й к-ты; II -1:2; III -1:3 т.д.). Для опр-я точной конц-ции получ-х р-ров отбираем по 5 мл в отдельную колбу и титруем 0,5 н. р-ром щелочи в присутствии фенолфталеина. Отмечаем по бюретке количество пошедшего на титрование р-ра щелочи в мом. появления розовой окраски р-ра в колбе. Рассч-м точную конц-цию рабочих р-ров к-ты до адсорбции по след. ф-ле: Сщ · Vщ = Ск·Vк . В оставшиеся р-ры (6 колб по 45 мл) всыпаем в каждый по 0,125 г порошка адсорбента, предварит. измельч-го порошка активир-го угля. Р-ры с адсорбентом перемеш. в теч. 30 мин., фильтруем и опр-м титрованием конц-цию ки-ты. Рассч-м конц-цию р-ра после адсорбции. Рез-ты эксперим. заносим в табл. График изотермы адсорбции строим в координатах Х/м от Со.
Лаб. раб. 4.
МОЛЕКУЛЯРНО-КИНЕТИЧ. ТЕОРИЯ АГРЕГ-ГО СОСТ-Я В-ВА. ОПРЕД-Е ПОВЕРХН-ГО НАТЯЖЕНИЯ СТАЛАГМОМЕТРИЧ-М МЕТОДОМ
Цель: 1.Изуч. схему взаимод-я мол-л поверхн-го и глубинных слоев жид-ти. 2.Дать опред-е поверхн-й энергии и поверхн-го натяжения. 3.Опр-ть поверхн-е натяжение исслед-х жид-й сталагмометрич. способом.
Поверхн-й слой жид-и по физико-хим. св-вам отлич-ся от внутр-х слоев. На каждую мол-лу внутри жид-и равномерно действуют силы притяжения со стороны окружающих мол-л, поэтому силовое поле каждой молекулы внутри жид-и симметрично насыщено. Равнод-я сила межмолекулярного взаимод-я равна нулю. На мол-лы, кот. наход. в поверхн-м слое жидкости, действуют силы притяж. только со стороны жид-и, мол-л, наход-ся в нижней полусфере. Равнод-я молекулярных сил не равна нулю и направлена вниз. Пов-ть жид-и стремится к сокращению. Наличие у поверхн-х мол-л жид-и неиспользованных сил явл-ся источником избыточной поверхн-й энергии. Поверхн-я энергия жид-и на границе с данной средой количественно хар-ся удельной поверхн-й энергией или коэфф. поверхн-го натяжения: G = А/S, Дж/м2=Нм/м2, Н/м (103эрг/см2) А- поверхн-я энергия, Дж; S- площадь пов-ти, м2. Для водных цементных р-ров поверхностная энергия играет большую роль. В-ва, значительно снижающие поверхн-е натяжение, наз. поверхностноактивными в-вами или ПАВ. В-ва, повышающие поверхн-е натяжение жид-и, наз. поверхностнонеактивными. Сталагмометрич. способ опр-ния поверхн-го натяжения основан на завис-ти между числом капель, вытекающих из сталагмометра, определенного объема жидкости и поверхн-м натяжением. Gж =GH2O ρж nH2O / ρH2O nж, Gж- поверхн-я энергия иссл-го р-ра; ρH2O, ρж - плотность р-ров; n - число капель воды и иссл-й жид-и.
Прибор для опр-я числа капель наз. сталагмометр.
Выполнение работы.
В стакан налив-ся вода или исследуемая жид-ть и в нее опускается сталагмометр. С пом. груши закачивается жид-ть в сталагмометр до верхней отметки, грушу убираем, чтобы жидкость самотеком выливалась в стакан. Подсчитываем число капель вытекаемой жид-ти до того мом., пока ур. жид-ти в сталагмометре достигнет нижней отметки. Плотность р-ра опр-м при пом. пикнометра. Результаты сводим в таблицу. Зарисовать: 1. Схему взаимод-я мол-л поверхн-го и глубинных слоев, сталагмометр, пикнометр.
Лаб. раб. 5.
ЭЛЕКТРОХИМИЯ. ЭЛЕКТРОДНЫЙ ПОТЕНЦ. ЭЛЕКТРОДВИЖ. СИЛЫ. ОПРЕД-Е ЭДС ГАЛЬВАНИЧ.О ЭЛЕМ-ТА
Цель: 1.Изуч. устройство и работу гальванич.о элемента и электродов и опр-ть знач-я их электродных потенциалов. 2.Опр-ть Э.Д.С. элемента Якоби-Даниэля. 3.Опр-ть pH водного р-ра цементной вытяжки; провести потенциометрическое титрование р-ра и построить графич. завис-ть pH от объема к-ты.
На границе двух фаз, содержащих заряженные компоненты, возникает межфазный потенциал:
Me10 / Ме1+ // Ме2+n / Ме20
G1 G2 G3
G1,3- на границе «металл-р-р» - электродный потенциал;
G2 - на границе двух р-ров- диффузный потенциал.
Потенциал на границе двух различных металлов - контактный; на границе «металл- газ» - контактный. Если активность потенциалобразующих ионов в р-ре не равна 1, то электродный потенциал не явл. стандартным и его значение опр-ся по ур-ю Нернста.
G=Go+(2,3 RT/nF)lg а; G - определяемый электродный потенциал, В; Go- стандартный электродный потенциал, В; R - газовая постоянная; Т – темпер.; n - заряд иона; F - число Фарадея; а - активность иона. Различают следующие типы электродов: электроды 1-го рода (металлы); электроды 2-го рода (р-ры электролитов); газовые; окислительно-восст-е. Гальванич. эл-т - это система, в кот. энергия хим. р-ции преобраз-ся в электрич. Он состоит из двух электродов, погруженных в р-ры электролитов. Устанавливается контакт мезду р-рами с пом. электролитического мостика для устранения диффузного потенциала. При соединении электродов внешним проводником на одном электроде происх. хим. р-ция окисления, на др. - восстановления. Электродвиж. сила такого гальванич. эл-та, или Э.Д.С. (Е), равна разности электродных потенциалов: E = G2-G1. Если Э.Д.С. опр-ся при активности ионов, равной единице, то Э.Д.С. обозн-ся Е0 (Е0 =G20 -G10).
Выполнение работы.
1.Зарис-ть электроды (каломельный, хлорсеребрянный, хингидронный, водородный, стеклянный), записать электродные процессы и их электродные потенциалы. 2.Сост-ть и зарис-ть гальванич-й эл-т Якоби-Даниэля, рассч-ть знач. электродвиж. силы, написать электродные процессы. 3.Водную вытяжку из бетонных образцов установить в электродную систему потенциометра. Вкл-ть потенциометр. Замерить pH водного р-ра вытяжки, оттитровать ее р-ром к-ты, кот. предварит. необходимо налить в бюретку. Для построения графич. завис-ти pH от объема щелочи, необх. провести 7-10 измерений. 4.Постр. график потенциометрического титрования водной вытяжки из бетонных образцов.
Лаб. раб. 6
КОЛЛ. ХИМИЯ. ПОЛУЧЕНИЕ КОЛЛОИДНЫХ Р-РОВ И ОПРЕД-Е ПОРОГА КОАГУЛЯЦИИ
Цель: Получить колл. р-р методом пептизации. Изуч. строение колл. частицы - мицеллы. Опр-ть порог коагуляции золя.
Колл. химия изуч. строение и св-ва дисперсных систем. К дисперсным системам отн-ся двух- или многокомпонентные системы, в кот. одно в-во находится в сост. более или менее высокой степени раздробленности и равномерно распределено в окруж-й ср. Колл. дисперсные сист. – сист. с размером частиц дисперсной фазы 10-9 – 10-7 м хар-ся отсутствием взаимод-ия между фазами. Их относят к ультромикрогетерогенным системам. Колл. системы термодинамически неустойчивы, обладают высокой адсорбционной способностью и самопроизвольно могут разрушаться путем агрегирования частиц.
Колл. системы с тв. дисперсной фазой наз. золями, а с жидкой - эмульсиями. Структурной единицей золя явл. мицелла. Мицелла - электрически нейтральная частица, окруженная двойным слоем ионов. Образование двойного слоя ионов может проходить двумя путями: 1- преимущественная адсорбция одного из присутствующих ионов, входящего в состав твердой фазы; 2- за счет диссоциации поверхностных молекул твердого тела с образованием в растворе ионов определенного знака. Ионы, сообщающие заряд твердой фазе, называются потенциалопределяющими, а остающиеся в растворе - противоионами. Получение коллоидных растворов возможно двумя путями: дроблением в-ва до опред-х размеров колл. частиц и конденсацией из истинных р-ров.
Коагуляция золей - укрупнение частиц, кот. может происходить по различным причинам, в частности при действии р-ра электролита. Порог коагуляции - это минимальное количество электролита, кот. способно вызвать коагуляцию золя.
Спор = 1000 СМ/V, где С - минимальная конц-ция электролита, вызывающая коагуляцию, мл.; М - объем р-ра электролита, вызывающий коагуляцию; V- объем золя.
Выполнение работы.
1.В колбе нагреваем 50 мл дистил-й воды до кипения и добавляем 10 мл 2% р-ра хлорида железа (+3), продолжаем кипятить еще 3-5 мин. Мицелла золя образ-ся за счет адсорбции ионов, получившихся в рез. гидролиза хлорида железа на пов-ти частиц. Противоионами служат хлорид ионы. 2.Написать ур-е хим. р-ции получения золя, ф-лу мицеллы золя.
Определить порог коагуляции (таблица).
Лаб. раб. 7
КОЛЛ. ХИМИЯ. ИССЛЕД-Е ГИДРОФОБНОСТИ ПОРОШКОВ И ВЛИЯНИЕ РАЗЛ-Х ДОБ-К НА СВ-ВА ЦЕМЕНТНЫХ СУСПЕНЗИЙ
Цель: 1.Изуч. влияние разл-х доб-к на седиментационные св-ва цементных суспензий. 2.Получить кривые седиментации разл-х дисперсных систем.
Способность дисп-й сист. сохранять равномерное распредепение дисп-й фазы в дисперсионной среде наз. седиментационной устойчивостью. Принцип седиментационного анализа дисп-х систем закл-ся в измерении скор. оседания дисп-х частиц в какой-либо дисперсионной среде. Метод опр-я седиментационной уст-ти путем непрерывного взвешивания закл-ся в опр-и скор. накопления осадка на чашке весов.
Кривая седиментации представл. на рис.1. Р-f (t), где Р - масса осадка на чашке весов.
При данной конц-ции суспензии и высоте оседания Н угол наклона линии ОА или ОВ завис. от размера частиц дисп-й фазы. Для дисп-й системы с 3-мя видами частиц находят 2 точки излома кривой оседания и т.д.
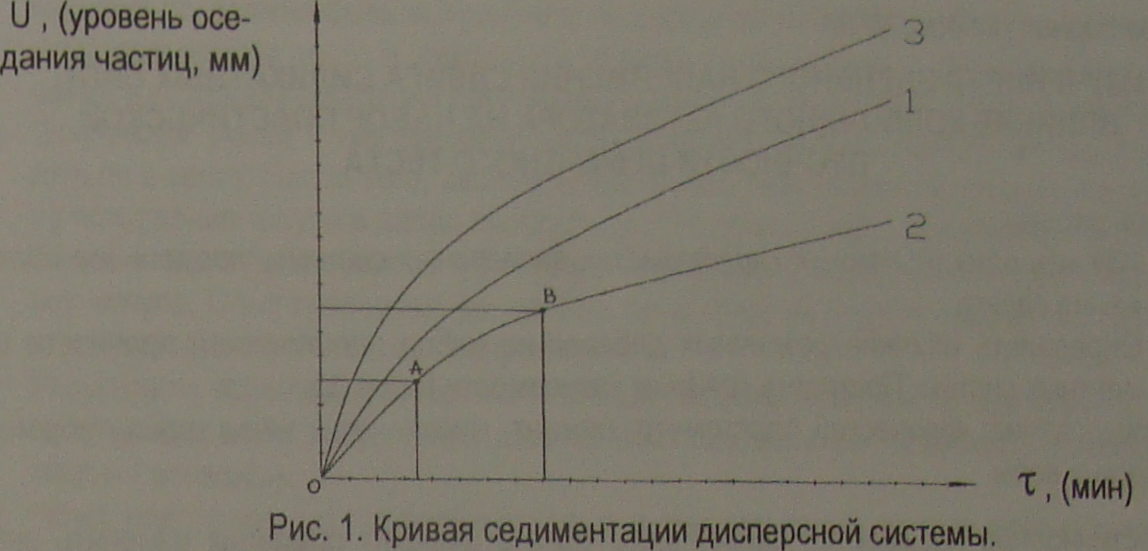
Завис-ть скор. оседания частиц опр-ся законом Стокса: V=2/9gr2(d1-d2) / n0, где g – ускор-е силы тяжести,м/с2; n0 - вязкость жид-ти,нс/м2; d1,d2 - плотность частицы и жид-ти,кг/м3; r-радиус частицы,м.
Выполнение работы.
1.Исслед-е цементной суспензии. Навеску цемента высыпаем в седиметометр и устанавл-м нулевую отм. Перемеш. суспензию в течение 5 мин. и через кажд. 30 сек отмеч. ур-нь оседания частиц до их полн. оседания. Знач-я посл-х 3-х замеров должны быть одинак. 2.Аналогично 1-му оп., но вводим доб-ку в эту же суспензию, т.е. добавл. в цементную сусп-ю р-р добавки - электролита или колл. р-ра. Перемеш. и проводим седиментацию. 3.Готовим новую цементную суспензию, с таким же колич. цемента, как и в 1-ом оп., но вводим др. доб-ку. Перемеш. и проводим исслед-е. Для всех получ-х знач-й изменения ур. оседания частиц опр-м скор. оседания и строим график кривых оседания для исслед-х систем - суспензий.
Лаб. раб. 8
ИЗУЧ. ПРЕД-ГО НАПРЯЖЕНИЯ СДВИГА СИЛИКАТНЫХ ПАСТ.
ВЛИЯНИЕ КОЛЛ. АКТИВАТОРА НА НАБОР ПЛАСТИЧЕСКОЙ ПРОЧНОСТИ ЦЕМЕНТНОГО ТЕСТА
Цель: 1.Изуч. одну из важных хар-к дисп-х систем – предельное напряжение сдвига. 2.Опр-ть влияние разл-х доб-к на набор пластической прочности цементных систем. Построить графики завис-ти Rnn =f (t).
Пластичностью наз. способность тела в широких пределах изменять свою форму под влиян. внешн. возд.я, не давая трещин, разрывов, и сохранять эту форму после прекращения возд-я вн-х сил. Пласт-ть явл. одним из осн. св-в керамич-х формовочных паст. Свежезатворенное цементное тесто явл. тоже пластичным телом. Тела, облад-е пластичными св-вами, явл. структурированными дисп-ми системами. Одной из важных хар-к таких систем явл. предельное напряжение сдвига. Механич. св-ва цементного теста значительно изм-ся при введении в его состав поверхностноактивных в-в (ПАВ). Исп-т конический пластометр конструкции М. Волоровича и А. Маркова. Знач. предельного напряжения сдвига, выражающее эту прочность, опр-ся по ф-ле: F =KP/h2; К = f(а), где К=0,92; а - угол осевого сечения конуса,30°; Р - постоянно действ-я на конус сила,кг (0,32); h- макс-я глубина погр-я конуса.
