
- •Физика коллоквиум 19.12.11
- •Уравнение состояние идеального газа.
- •Давление. Основное уравнение молекулярно-кинетической теории.
- •Температура.
- •Внутренняя энергия. Теплота и работа. Первое начало термодинамики.
- •Распределение молекул газа по скоростям. Функция распределения Максвелла.
- •Наиболее вероятная, средняя квадратичная и средняя арифметическая скорости молекул газа.
- •Распределение Максвелла по значениям кинетической энергии.
- •Формула Максвелла по значениям кинетической энергии.
- •Изобарный процесс.
- •Изотермический процесс.
- •Адиабатный процесс.
- •Обратимый цикл Карно.
Физика коллоквиум 19.12.11
Уравнение состояние идеального газа (уравнение Менделеева-Клапейрона)
Давление. Основное уравнение молекулярно-кинетической теории.
Температура.
Внутренняя энергия. Теплота и работа. Первое начало термодинамики.
Распределение молекул газа по скоростям. Функция распределения Максвелла.
Наиболее вероятная, средняя квадратичная и средняя арифметическая скорости молекул газа.
Распределение Максвелла по значениям кинетической энергии.
Формула Максвелла по значениям кинетической энергии.
Барометрическая формула.
Распределение Больцмана.
Теплоемкость газа. Формула Майера.
Изохорный процесс.
Изобарный процесс.
Изотермический процесс.
Адиабатный процесс.
Обратимый цикл Карно.
Необратимый цикл Карно.
Энтропия.
Изменение энтропии при обратимых и не обратимых процессах.
Второе начало термодинамики.
Свободная и связанная энергия. Физический смысл энтропии.
Статистический смысл энтропии.
Третье начало термодинамики.
Примечание:
Буквой J обозначается степень свободы, т.е по-нашему «i».
Уравнение состояние идеального газа.
Уравнение Клапейрона-Менделеева связывает только микроскопические параметры и непосредственно вытекает из:
 >/3=nkT=(N/V)kT
>/3=nkT=(N/V)kT
(Отсюда видно, что произведение PV зависит от суммарной кинетической энергии молекул, т.к средняя кинетическая энергия определяется абсолютной температурой.
В уравнение:
 , которое фактически
определяет абсолютную температуру.
, которое фактически
определяет абсолютную температуру.
Давление. Основное уравнение молекулярно-кинетической теории.
Идеальный газ – газ, молекулы которого не взаимодействуют между собой, исключая лишь кратковременный процесс столкновений, во время которого происходит взаимный обмен энергией и импульсом.
Давление – поток нормальной проекции импульса на стенку.
Рассчитываем
давление:

Молекулярно-кинетическая теория (МКТ) — теория, рассматривавшая строение вещества, в основном газов, с точки зрения трёх основных приближенно верных положений:
все тела состоят из частиц: атомов, молекул и ионов;
частицы находятся в непрерывном хаотическом движении (тепловом);
частицы взаимодействуют друг с другом путём абсолютно упругих столкновений;
Основными доказательствами этих положений считались:
Диффузия
Броуновское движение
Изменение агрегатных состояний вещества
Основное
уравнение МКТ:
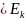 >=
>=
Температура.
Температура – зависимость легко измеримых физических параметров от степени нагретости (на этом основано действие различных термометров: жидкостных, резистивных, пирометров, газовых)
Введем понятие термостата, как очень большой системы, температура которого неизменна при контакте с другими системами.
Постулат – по истечению некоторого времени релаксации любое пробное тело, приведенное в контакт с термостатом, принимает его температуру. Изотермы одного и того же вещества никогда не пресекаются между собой => условная температура – функция состояния, определяемая P и V.
PV=const
; термическое уравнение состояния
идеального газа: t= (PV)
(PV)
Принцип температуры: существует функция термодинамической системы, называемая условной температурой, которая остается постоянной при любом процессе, протекающем в термостате.
