
- •Лабораторная работа №1. Исследование теплоемкости твердых тел в интервале температур от 350 к до 900 к.
- •Краткая теория.
- •Молекулярная теплоемкость химических соединений в твердом состоянии
- •Теория метода и описание установки.
- •Задание 1. Получение экспериментальных данных по температуре (т) и времени (t) охлаждения образца.
- •Задание 2. Нахождение производных в окрестностях температур.
- •Задание 3. Определение удельной теплоемкости железа и алюминия. Построение графика зависимости молярной теплоемкости от температуры.
- •Задание 4. Определение коэффициента теплоотдачи.
- •2. Определение газовой постоянно r.
- •3. Проверка первого начала термодинамики.
- •Описание установки:
- •Порядок выполнения работы:
- •Обработка результатов измерений:
- •Контрольные вопросы:
- •Лабораторная работа № 3 Определение отношения Ср/Сv (для воздуха методом Клемана - Дезорма).
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №4 «Определение отношения молярных теплоемкостей Ср/Сv методом измерения скорости звука»
- •Порядок выполнения работы.
- •Контрольные вопросы
- •Лабораторная работа №5. Изучение зависимости сопротивления проводника и полупроводника от температуры. Определение энергии активации полупроводника.
- •Методические указания
- •Описание установки
- •Порядок выполнения работы Задание 1
- •Задание 2
- •Литература
Обработка результатов измерений:
Вычислите массу газа по формуле (2.7).
Постройте график зависимости объема V от температуры T. Для этого на оси абсцисс откладывайте интервал температур
 ,
а на оси ординат – интервал изменения
объема
,
а на оси ординат – интервал изменения
объема
 .
По графику определите угловой коэффициент
b
полученной прямой, учитывая весь
интервал изменения температуры
.
По графику определите угловой коэффициент
b
полученной прямой, учитывая весь
интервал изменения температуры
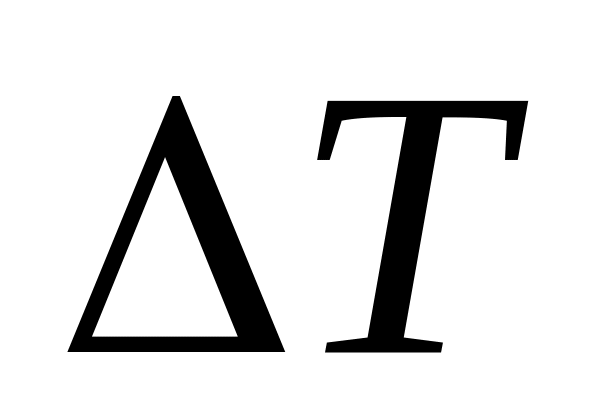 и объема
и объема
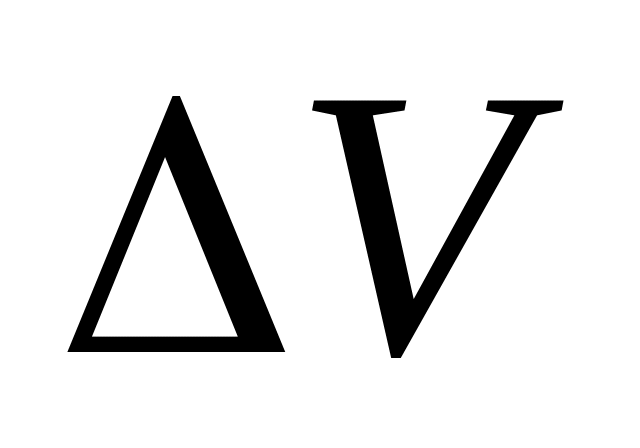 .
.По формуле (2.11) рассчитайте значение газовой постоянной R. Сравните получившееся значение с табличным.
По формуле (2.2) рассчитайте значение работы А. За понижение уровня положения мениска в левом колене манометрической трубки примите разность ∆h, соответствующую изменению температуры за все время эксперимента.
Вычислите сообщенное воздуху количество теплоты
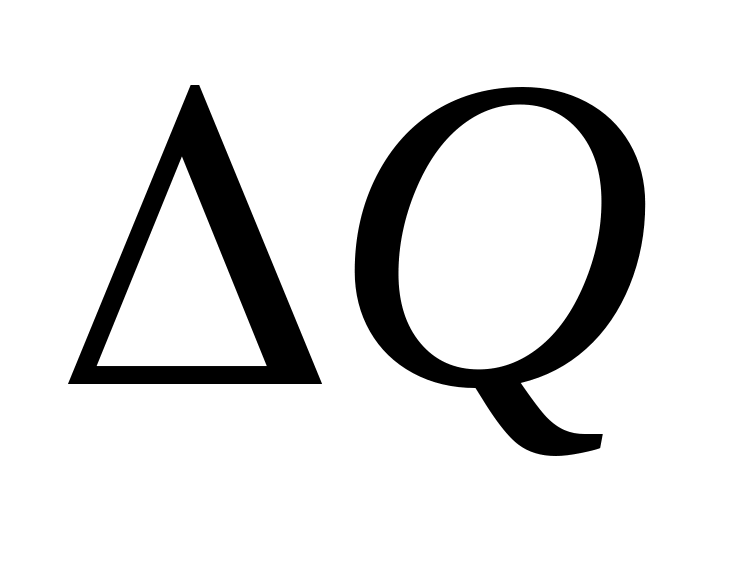 соответствующее
изменению температуры
за все время эксперимента,
используя выражение (2.15).
соответствующее
изменению температуры
за все время эксперимента,
используя выражение (2.15).Вычислите изменение внутренней энергии
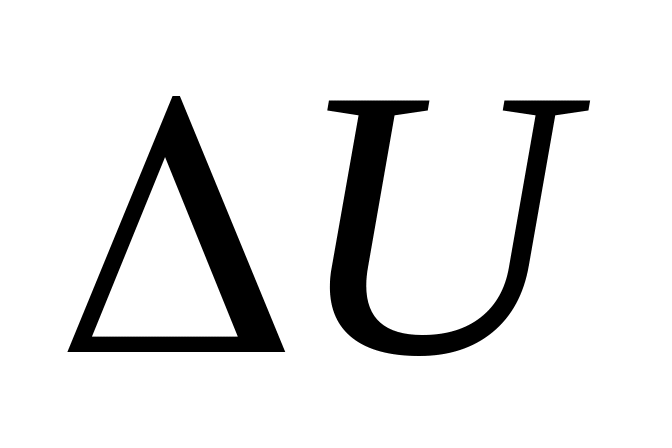 ,
соответствующее
изменению температуры
за все время эксперимента,
используя выражение (2.14).
,
соответствующее
изменению температуры
за все время эксперимента,
используя выражение (2.14).Проверьте выполнение равенства (2.13). Сделайте вывод.
Необходимые постоянные:
![]()
Контрольные вопросы:
Сформулируйте первое начало термодинамики и примените его к различным процессам в идеальном газе.
Запишите в дифференциальной форме первое начало термодинамики для адиабатического процесса.
Выведите уравнение Пуассона.
Выведите уравнение Майера.
Получите связь со степенями свободы теплоемкостей Ср и СV.
Лабораторная работа № 3 Определение отношения Ср/Сv (для воздуха методом Клемана - Дезорма).
Цель работы: Определить отношение Ср/С для воздуха методом Клемана– Дзорма, основанном на исследовании газа, последовательно переходящего в различные состояния.
Приборы и принадлежности: стеклянная колба, насос, манометр,секундомер
В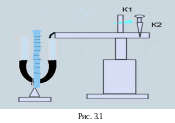 настоящей работе определение отношенияСр/С
производится одним из классических
методов – методом Клемана – Дезорма.
Большой сосуд при помощи крана (К1)
сообщается с наружным воздухом (рис.
3.1), а с помощью крана (К2) –с водяным
манометром и нагнетательным насосом.
настоящей работе определение отношенияСр/С
производится одним из классических
методов – методом Клемана – Дезорма.
Большой сосуд при помощи крана (К1)
сообщается с наружным воздухом (рис.
3.1), а с помощью крана (К2) –с водяным
манометром и нагнетательным насосом.
В предстоящем опыте полная масса газа в сосуде будет изменяться. Поэтому будем оперировать удельным объемом
![]() , (3.1)
, (3.1)
где m – масса газа, V – объем. Выделяя мысленно единичную массу газа, которая при всех изменениях остается внутри сосуда, для адиабатического процесса можно записать уравнение Пуассона:
![]() или
или
![]() (3.2)
(3.2)
Рассмотрим последовательно процессы, происходящие с газом (рис 3.2).
Закроем
кран и быстро накачаем в сосуд воздух
до тех пор, пока манометр не покажет
разность давлений 115-120 мм вод.ст. Перекроем
краном К2
трубку, соединяющую баллон с насосом.
Процесс соответствует адиабате 0-1. Через
2-3 мин давление снизится от p1
до p2,,
а температура снизится от Т1
до Т2
= Т0,
т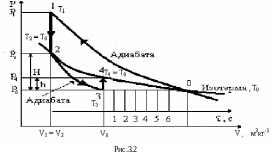 .е.комнатной.
Воздух изохорически перейдет из состояния
(P1,T1,V1)
в состояние (P2,T0,V2
=V1)
–процесс 1-2.
.е.комнатной.
Воздух изохорически перейдет из состояния
(P1,T1,V1)
в состояние (P2,T0,V2
=V1)
–процесс 1-2.
Если соединить сосуд с атмосферой на секунд, открыв кран К1, то воздух в сосуде будет расширяться адиабатически до тех пор, пока его давление не установится равным атмосферному p0, при этом температура понизиться до Т3 < Т0 – процесс 2-3. Для него имеем:
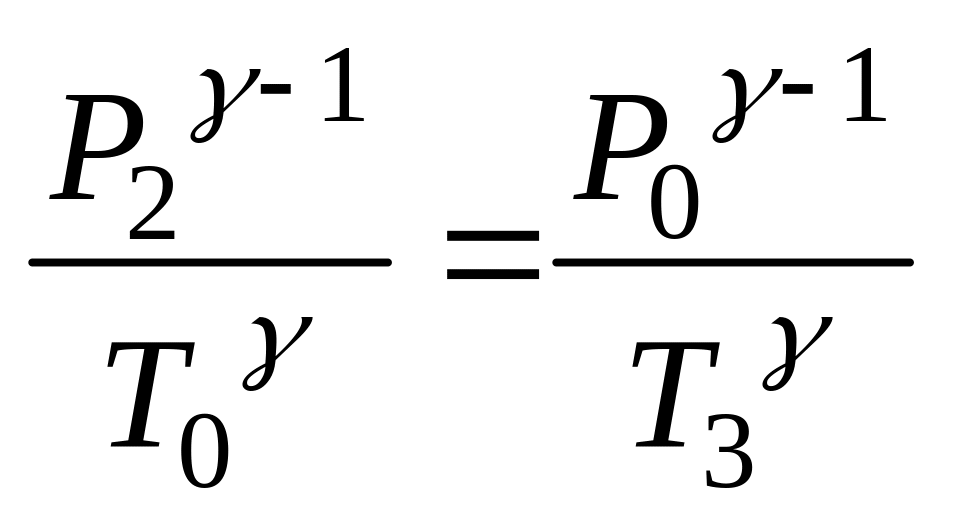 (3.3)
(3.3)
После закрытия крана К1 температура воздуха в баллоне через некоторое время (2-3 мин), определяемое теплопроводностью стенок сосуда cравняется с Т0 = Т4. Процесс 3-4 изохорический. Для него имеем:
![]() (3.4)
(3.4)
Решая совместно (3.3) и (3.4) имеем
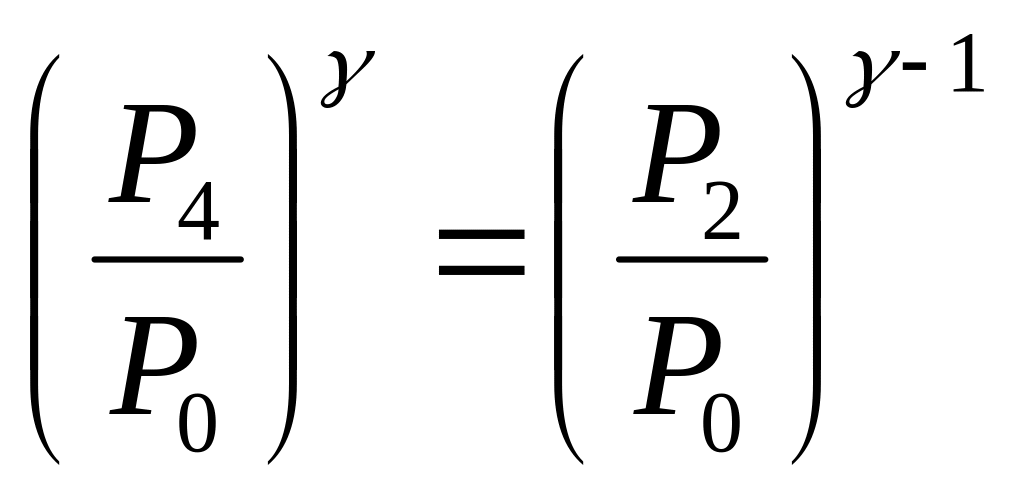 (3.5)
(3.5)
Логарифмируя (3.5), получим:
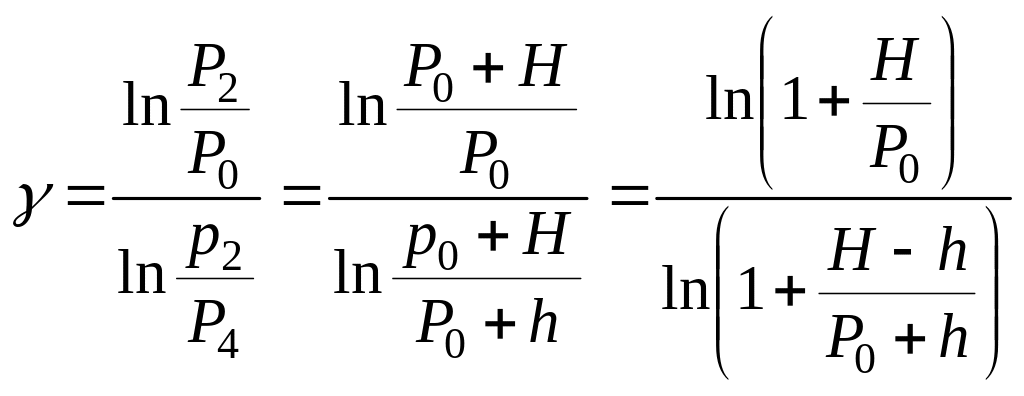 (3.6)
(3.6)
Имея
в виду то, что H,
h
<< p0,
можно воспользоваться разложением
функции ln(1+х)
в ряд, т.е. ln(1+x)
= x
-
![]() - … , если x<<1
и ограничившись первым членом разложения,
получим:
- … , если x<<1
и ограничившись первым членом разложения,
получим:
![]() (3.7)
(3.7)
С ледует
заметить, что величина h
существенно зависит от времени
перекрывания крана К1.
Если перекрывать раньше, то получим
завышенное значение h.
Если перекрывать кран К1
позже
момента выравнивания давления в сосуде,
то получим заниженное значение h.
ледует
заметить, что величина h
существенно зависит от времени
перекрывания крана К1.
Если перекрывать раньше, то получим
завышенное значение h.
Если перекрывать кран К1
позже
момента выравнивания давления в сосуде,
то получим заниженное значение h.
Поскольку, момент окончания адиабатического процесса 2-3 неопределен, найдем значения hi в различные промежутки времени I между открыванием крана К1 и его закрытием.
Опыт показывает, что между hi, h, и выполняется соотношение
![]() , (3.8)
, (3.8)
где А- константа зависящая от многих факторов (установки, условий).
Если
построить график зависимости
![]() ,
то путем экстраполирования можно найти
lg
h
и, следовательно , h
(рис.3.3).
,
то путем экстраполирования можно найти
lg
h
и, следовательно , h
(рис.3.3).
Таблица 3.1
i |
1=2 |
2=3 |
3=4 |
4=5 |
5=6 |
H |
|
|
|
|
|
h’i |
|
|
|
|
|
Lghi |
|
|
|
|
|
