
- •Под редакцией в.В. Колпаковой
- •I. Органические соединения азота
- •Нитросоединения
- •2). Реакции, связанные с подвижностью α-атомов водорода.
- •3). Реакции с минеральными кислотами.
- •3. Перегруппировка амидов карбоновых кислот по Гофману:
- •Физические свойства
- •2. Алкилирование аминов.
- •Реакции аминов с азотистой кислотой.
- •В случае взаимодействия n,n-диметиламинобензола с азотистой кислотой механизм реакции выглядит следующим образом:
- •Реакции аминов с карбонильными соединениями.
- •Изонитрильная проба.
- •Синтезы на основе свойств солей диазония
- •Соли диазония.
- •II. Органические соединения серы введение
- •Соединения двухвалентной серы тиоспирты
- •Синтетические способы получения
- •Физические свойства
- •Химические свойства
- •Сульфиды
- •Способы получения
- •Химические свойства сульфокислот и их функциональных производных
- •Эфиры серной кислоты
- •Контрольные вопросы
- •11.1 Синтез и реакции меркаптанов (тиоспирты)
- •11.2 Способы получения и химические свойства ароматических сульфокислот
Эфиры серной кислоты
Легко образуются при реакции серной кислоты с алкенами и спиртами:
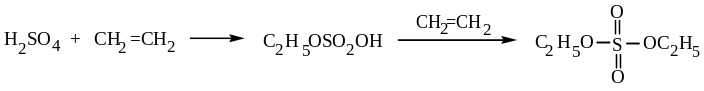 этилсерная
кислота диэтилсульфат
этилсерная
кислота диэтилсульфат
С12H25OH + H2SO4 → C12H25OSO3H
монолаурилсульфат
При кипячении в воде моно- и диэфиры гидролизуются. Так получают сернокислотным методом синтетические этиловый и изопропиловый спирты:

Моноэфиры серной кислоты являются сильными кислотами. С металлами, их оксидами и гидроксидами образуют соли. Лаурилсульфат натрия – эталонное анионное ПАВ. Хорошими поверхностно-активными веществами являются и сульфоэтоксилаты – продукты реакции серного ангидрида с синтанолами:
![]()
Эфиры серной кислоты – хорошие алкилирующие средства:
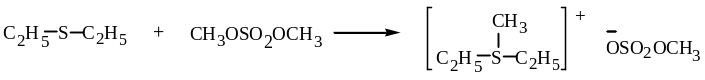 метилдиэтилсульфоний
метилдиэтилсульфоний
метилсульфат
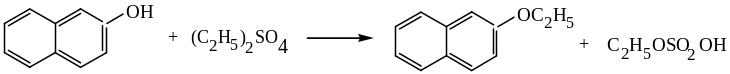
этиловый эфир β-нафтола
Контрольные вопросы
1. а) Какие классы сероорганических веществ Вам известны? Каковы
пути синтеза и основные химические свойства этих соединений?
б) К какому типу реакций относится сульфохлорирование алканов?
Напишите уравнение реакции и механизм реакции сульфохлорирова-
ния пропана.
в) Напишите схему сульфирования бензола олеумом. Приведите
механизм реакции. Сопоставьте механизм сульфирования с
механизмом других реакций электрофильного замещения в ядре
бензола, например галогенирования.
г) Какие сульфирующие реагенты Вам известны?
д) Какое значение имеет обратимость реакции сульфирования для
синтеза α- и β-нафталинсульфокислот?
е) Расположите приведенные ниже соединения в порядке уменьшения
скорости сульфирования: изопропилбензол (1), анизол (метилфени-
ловый эфир) (2), бензол (3), нитробензол (4), м-динитробензол (5).
и) Какой реакцией можно различить два изомерных соединения –
этилмеркаптан (этантиол) и диметилсульфид?
2. При сульфировании толуола при комнатной температуре образуется
75 % пара-, 20 % орто- и 5 % мета-толуолсульфокислот. Рассчитайте,
сколько получится каждого из изомеров (в г), если в реакцию введено
0,5 моль толуола. Какое влияние оказывает метильная группа на
скорость сульфирования (по сравнением с бензолом)?
3. Какие вещества получаются при действии на п-толуолсульфокислоту
cледующих реагентов:
а) перегретого водяного пара;
б) водного раствора гидроксида калия;
в) этанола;
г) анилина;
д) этиламина;
е) при сплавлении с гидроксидом натрия;
ж) при сплавлении с цианистым натрием;
з) пентахлорида фосфора.
4. Напишите уравнения реакций и назовите образующиеся соединения:
а) диметилсульфата с 2-нафтолом;
б) метилэтилсульфида с бромистым изобутилом;
в) окисления п-толилмеркаптана азотной кислотой;
г) бензолсульфокислоты с пентахлоридом фосфора, затем с
п-толуидином;
д) бензилмеркаптана с хлорангидридом пропионовой кислоты;
е) гидролиз изопропилсерной кислоты;
ж) нитрования α-нафталинсульфокислоты;
з) этандитиола-1,2 с уксусным альдегидом;
и) гидролиза диметилсульфата;
к) β-нафталинсульфокислоты с пентахлоридом фосфора, затем с
метанолом.
5. Хлорамин-Т и дихлорамин-Т (эффективные антисептические средства)
получают из толуола по следующей схеме:
ClSO2OH NH3 NaClO
толуол ¾¾¾¾® п-толуолсульфохлорид ¾¾® А ¾¾¾¾®
(1 моль)
NaClO (избыток)
¾¾® хлорамин Т ¾¾¾¾¾¾® дихлорамин-Т
Составьте уравнения реакций и приведите структурные формулы
хлорамина-Т и дихлорамина-Т.
6. Синтезируйте в несколько стадий из бензола, используя только
неорганические реактивы:
а) м-толуолсульфокислоту;
б) тиофенол;
в) ди-п-толилсульфид;
г) 4-бром-3-нитробензолсульфокислоту;
д) 3-хлор-5-нитробензолсульфокислоту;
е) дифенилсульфон;
ж) п-аминобензолсульфамид (амид п-аминобензолсульфокислоты);
з) альбуцид (N-ацетиламид п-аминобензолсульфокислоты).
7. Предскажите продукты сульфирования следующих соединений:
а) бромбензола;
б) п-нитротолуола;
в) м-дихлорбензола;
г) 1,3-диметоксибензола;
д) о-толуиловой кислоты;
е) анисового альдегида (п-метоксибензальдегида);
ж) м-крезола;
з) этилового эфир п-этилбензойной кислоты;
и) м-ксилола (1,3-диметилбензола);
к) о-гидроксибензойной кислоты (салициловой кислоты).
8. Установите строение серусодержащих органических соединений, если
известна молекулярная формула веществ и продукты их превращений
а) С8Н10О3S; при щелочном гидролизе образуется соль С7Н7О3SNa,
которая при сплавлении с NaOH дает п-крезол;
б) С8Н10О3S; при окислении K2Cr2O7 образует сульфобензойную
кислоту, а при щелочном плавлении п-этилфенол;
в) С2Н6S; не реагирует с водным раствором КОН; вступает в
реакции окисления, образуя два типа производных; при алкили-
ровании бромистым этилом дает ионное соединение;
г) С7H7SO2Cl; при гидролизе и последующем окислении
получается м-сульфобензойная кислота;
д) С7H7O3SBr; окисление дает сульфобензойную кислоту, а нитро-
вание __ только одно мононитропроизводное;
е) С7H8O3S; при окислении перманганатом калия превращается в
сульфобензойную кислоту, а при сплавлении с NaOH __ в о-
крезол;
ж) С4Н10SO4; при гидролизе разлагается на спирт и серную кислоту,
с фенолом в щелочной среде дает вератрол (этилфениловый
эфир);
з) C7H7ClO3S; при десульфировании образуется о-хлортолуол
(предложите все варианты ответа);
и) С6H6O4S; с FeCl3 дает фиолетовую окраску; при сплавлении
со щелочью (и последующем подкислении) превращается в
С6Н6О2, при окислении которого образуется бензохинон
(циклогексадиен-2,5-дион-1,4);
к) 1-бромпропан реагирует с избытком гидросульфида калия с
образованием С3Н8S (А). Соединение (А) окисляется конц.HNO3
до вещества С3Н8О3S (Б). Соединение (Б) реагирует c РСl5
давая хлорангидрид (В).Идентифицируйте вещества (А), (Б),(В)
л) С10Н8SO3; в результате окисления образуется 3-сульфофталевая
кислота (3-сульфобензолдикарбоновая-1,2 кислота);
м) С10H13NO4S; нейтрального характера; при нагревании с водным
раствором NaOH образует смесь солей уксусной и сульфанило-
вой (п-аминобензолсульфокислоты) кислот.
9. Осуществите указанные ниже последовательные реакции и назовите все
образующиеся соединения:
Н2SО4 Br2 K2S [ O ]
а) толуол ――→ А ―――→ Б ――→ В ―――→ Г
свет
Br2 2 NaSH 2 CH3MgBr
б) циклопропан ――→ А ―――→ Б ――――――→ В
HCl ? 2 [ O ]
в) пропилен ――→ А ―→ [(CH3)2CH]2S ――――→ Б
( H2O2 )
H2S KOH C2H5Br 2 [ O ]
г) пропанол-2 ――――→ А ――→ Б ―――→ В ――――→ Г
t ; Al2O3 ( H2O2 )
NaOH H2S CH3 MgJ
д) хлорциклогексан ―――→ А ―――→ Б ―――――→ В
t t ; Al2O3
NaOH CH3J [ O ]
е) п-тиокрезол ―――→ А ―――→ Б ―――→ В
SO2 + O2 PСl5 NH3 Cl2
ж) бутан ―――――→ А ―――→ Б ―――→ В ――→ Г
свет
3 [ O ] PСl5 этилат натрия
з) бутантиол-2 ―――→ А ―――→ Б ――――――→ В
3 [ O ] SOCl2 метилат натрия
и) п-метокситиофенол ―――→ А ―――→ Б ―――――――→ В
?
к) 1-нафталинсульфокислота ―→ 2-нафталинсульфокислота ―→
PCl5 NH3
―――→ А ―――→ Б
NaCN ? 2 HOSO2Cl
л) бензолсульфокислый ―――→ А ―→ бензойная ――――→ Б
натрий t кислота
? PСl5 этанол
м) нафталин ―→ 1-нафталинсульфокислота ――→ А ――→ Б
10. Объясните направление реакций электрофильного замещения (нитрова-
ния, бромирования, сульфирования) для α-нафталинсульфокислоты.
Сравните скорости этих реакций с таковыми для незамещенного
нафталина и α-нафтола.
ЛИТЕРАТУРА
основная:
1. Петров А.А. Органическая химия / А.А. Петров, Х.В. Бальян, А.Т. Трощенко: учебник. - СПб.: Иван Федоров, 2002. - 624 с.
2. Ким А.М. Органическая химия / А.М. Ким: учебник. - Новосибирск: Сибирское университетское изд-во, 2001. - 680 с.
дополнительная:
Моррисон Р. Органическая химия / Р. Моррисон, Р. Бойд: учебник. -
- М.: Мир, 1974. - 1132 с.
