
- •Под редакцией в.В. Колпаковой
- •I. Органические соединения азота
- •Нитросоединения
- •2). Реакции, связанные с подвижностью α-атомов водорода.
- •3). Реакции с минеральными кислотами.
- •3. Перегруппировка амидов карбоновых кислот по Гофману:
- •Физические свойства
- •2. Алкилирование аминов.
- •Реакции аминов с азотистой кислотой.
- •В случае взаимодействия n,n-диметиламинобензола с азотистой кислотой механизм реакции выглядит следующим образом:
- •Реакции аминов с карбонильными соединениями.
- •Изонитрильная проба.
- •Синтезы на основе свойств солей диазония
- •Соли диазония.
- •II. Органические соединения серы введение
- •Соединения двухвалентной серы тиоспирты
- •Синтетические способы получения
- •Физические свойства
- •Химические свойства
- •Сульфиды
- •Способы получения
- •Химические свойства сульфокислот и их функциональных производных
- •Эфиры серной кислоты
- •Контрольные вопросы
- •11.1 Синтез и реакции меркаптанов (тиоспирты)
- •11.2 Способы получения и химические свойства ароматических сульфокислот
Сульфиды
Простые тиоэфиры называют сульфидами. Их можно получить из галогеналканов и сульфидов щелочных металлов:
2 CH3CH2Br + K2S → СH3CH2 – S – CH2CH3 + 2 KBr
Сульфиды образуются также при перегонке меркаптидов свинца:
(CH3S) 2Pb → (CH3) 2S + PbS
Низшие тиоэфиры представляют собой жидкости, нерастворимые в воде и кипящие выше, чем меркаптаны. Запах чистых сульфидов не является неприятным, напоминает запах эфира.
К тиоэфирам относится и известное отравляющее вещество «иприт» – β,β'-дихлордиэтилсульфид. Его получали из этилена и однохлористой серы:
2 CH2=CH2 + S2Cl2 → Cl – CH2CH2 – S – CH2CH2 – Cl + S
Химические свойства сульфидов обусловлены склонностью двухвалентной серы к переходу в высшие валентные состояния.
50%-ная азотная кислота окисляет тиоэфиры в сульфоксиды:

Диметилсульфоксид – один из наиболее применяемых высоко-полярных растворителей.
Более сильные окислители (конц. HNO3, КMnO4) окисляют сульфиды и сульфоксиды до сульфонов.
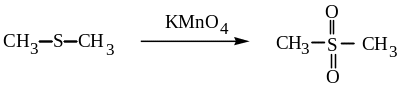
диметилсульфон
Сульфоны – твердые кристаллические вещества. Некоторые сульфоксиды и сульфоны применяются в лекарственных средствах.
Полисульфоны являются негорючими полимерами. Некоторые из них могут быть получены взаимодействием олефинов с оксидом серы (IV):
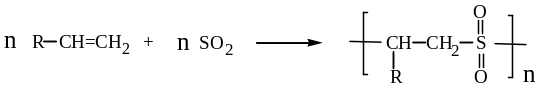
При алкилировании тиоэфиров галогеналканами или эфирами серной кислоты образуются сульфониевые соли:
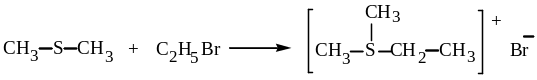
Бромистый диметилэтилсульфоний и другие сульфониевые соли хорошо растворимы в воде. Их физические и химические свойства подобны свойствам четвертичных аммониевых соединений.
Сульфокислоты
Сульфокислоты (или сульфоновые кислоты) – органические соединения, молекулы которых содержат сульфогруппу SO3H, непосредственно связанную с атомом углерода.
Способы получения
1. Прямое сульфирование углеводородов обычно применяется для получения ароматических сульфокислот. Сам бензол и его производные, содержащие в ядре заместители-акцепторы, сульфируются олеумом:
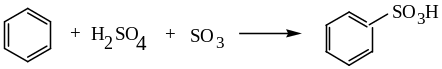
Гомологи бензола и нафталин сульфируются концентрированной серной кислотой:
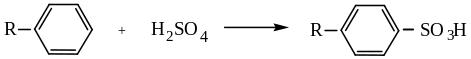
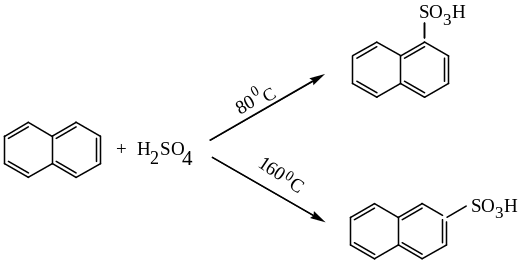
Прямое сульфирование алканов возможно лишь при наличии в молекуле третичного атома углерода:
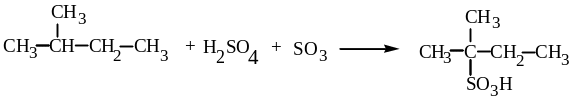
2-метилбутан-2-сульфокислота
Некоторые алифатические сульфокислоты могут быть получены сульфоокислением алканов (на свету), однако эта реакция мало изучена и практического применения пока не нашла:
R – H + SO2 + O2 → R – SO3H
Окисление меркаптанов:
R – SH + [ O ] → R – SO3H
Способ имеет ограниченное применение, так как исходные меркаптаны не дешевы.
Реакция галогеналканов с сульфитом натрия:
CH3CH2Br + Na2SO3 → CH3CH2SO2ONa + NaBr
натрийэтилсульфонат
Присоединение гидросульфита натрия по двойным связям:
R – CH=CH2 + NaHSO3 → R – CH – SO3Na
│
CH3
Таким образом в промышленности получают смеси высших алкилсульфонатов.
Сульфокислоты представляют собой кристаллические вещества, хорошо растворимые в воде, весьма гигроскопичные.
