
- •Введение
- •Виды тепловых машин:
- •По способу подвода теплоты
- •1)Термодинамика
- •2)Теория теплообмена
- •Предмет Термодинамики
- •Достоинства Термодинамического метода исследования:
- •Достоинства статического подхода:
- •Термодинамическая система
- •Термодинамический процесс и равновесное состояние
- •Основные параметры состояния термодинамической системы.
- •Уравнение состояния.
- •Уравнение состояния идеального газа полученное на основе мкт
- •Теплоёмкость
- •Второй закон термодинамики Сущность второго закона термодинамики
- •Цикл Карно
- •Энтропия
- •Термодинамические циклы двигателя внутреннего сгорания
- •Цикл Дизеля
- •Цикл Тринклера
- •Циклы Отто, Дизеля и Тринклера в t-s
- •Сгорание топлива
- •Теплопередача.
Цикл Карно
Цикл Карно – это идеальный термодинамический цикл, тепловая машина работающая по этому циклу обладает максимальным КПД. Цикл Карно состоит из двух адиабатных и двух изотермических процессов. Изотермические и адиабатные процессы являются самыми выгодными для получения работы из определённого количества теплоты, в изотермическом процессе вся теплота, подводимая к рабочему телу превращается в работу, а адиабатный процесс протекает без потерь теплоты так как отсутствует теплообмен с окружающей средой и работа совершается за счёт уменьшения внутренней энергии. Кроме того одним из важных свойств цикла Карно является его обратимость
![]()
11
21
q1
P

31
41
q2
V
Лекция №11
Энтропия
Обмен энергией может происходить в форме работы и в форме теплоты. Работа совершается системой в случае изменения объёма или перемещения всей системы.
![]()
P
L







1
2

V
Работа может быть изображена на графике площадью под линией процесса. Работа зависит от значения давления и объёма.
В случае передачи энергии в форме теплоты значение энергии в некоторых случаях возможно получить по известной формуле однако, измеряя значение температуры не всегда можно определить количество переданной теплоты ( при подводе теплоты к кипящей воде её температура не меняется).
В 1852 году Клаузис предложил параметр, который изменялся только в случае подвода или отвода теплоты (энтропия)
Энтропия – функция состояния термодинамической системы дифференциал которой равен количеству подведённой теплоты отнесённому к температуре процессу
![]()
dQ – элементарное количество теплоты подведённое к системе при постоянной температуре Т.
Данная формула является математической записью второго закона термодинамики для обратимых процессов.
Вывод из второго закона термодинамики: энтропия системы при совершении необратимых процессов возрастает.
Энтропия может быть измерена и определена только только расчётным путём – также как потенциальная энергия тела.
Количество подводимой теплоты к системе из данной формулы можно записать в виде интеграла:
Как следует из формул:
![]()
dQ=TdS
Существует следующая зависимость:
dS>0 dQ>0
dS<0 dQ<0
Тепловая диаграмма T-S.
Тепловая диаграмма T-S – это графическая зависимость между температурой и энтропией, она имеет широкое применение при исследовании и расчёте термодинамических процессов и циклов, значительно упрощает и повышает наглядность термодинамических исследований.
![]()
Изобарный и изохорный процесс в T-S координатах
T
T
2V
2P
1
S
S
dq
S1
S2
q
2


Расчёт КПД цикла Карно с помощью тепловой диаграммы
b
z
T
c
a
q1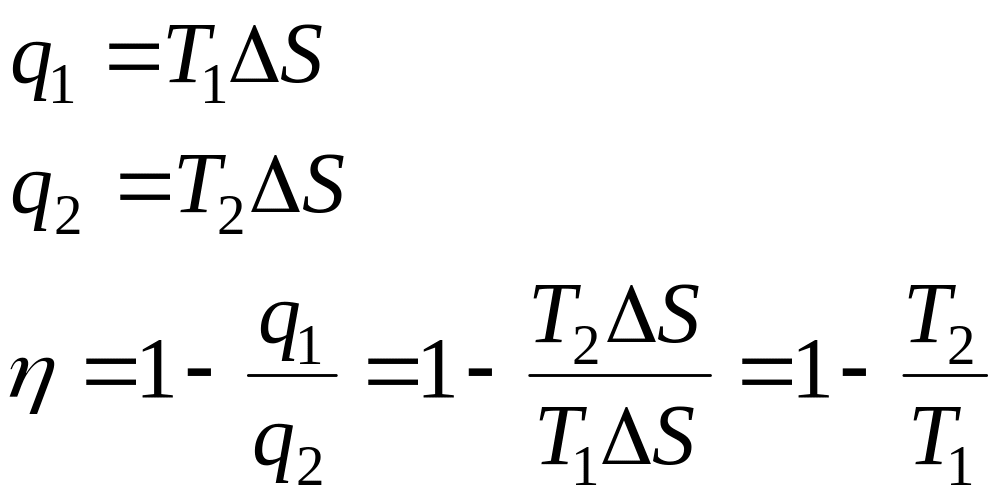
S
Лекция №12
