
Вопрос 8
Внутренняя
энергия идеального газа является только
функцией температуры
(и
не зависит от V,
Р и тому подобным),
поэтому формула справедлива для любого
процесса.
Для произвольной массы
идеального газа:
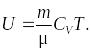
числа степеней свободы: это число независимых переменных (координат), которые полностью определяют положение системы в пространстве. В некоторых задачах молекулу одноатомного газа (рис. 1, а) рассматривают как материальную точку, которой задают три степени свободы поступательного движения. При этом не учитывается энергия вращательного движения.
Итак, средняя энергия приходящаяся на одну степень свободы:
У одноатомной молекулы i = 3, тогда для одноатомных молекул
для двухатомных молекул
для трёхатомных молекул
Таким образом, на среднюю кинетическую энергию молекулы, имеющей i-степеней свободы, приходится
Это и есть закон Больцмана о равномерном распределении средней кинетической энергии по степеням свободы. |
Постулат Максвелла
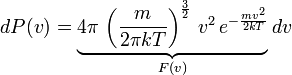
Средняя энергия хаотического движения молекулы
![]() =
3/2 kT (для
одной частицы)
=
3/2 kT (для
одной частицы)
Постоянная Больцмана
![]()
Газовая постоянная
R=k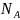 =8,31
=8,31
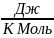
Молярные теплоемкости идеального газа
C = M · c
![]()
Cp = CV + R.
Вопрос 9
Равнове́сный тепловой процесс — тепловой процесс, в котором система проходит непрерывный ряд бесконечно близких равновесных термодинамических состояний.
Равновесный тепловой процесс называется обратимым, если его можно провести обратно и в телах, окружающих систему, не останется никаких изменений.
Реальные процессы изменения состояния системы всегда происходят с конечной скоростью, поэтому не могут быть равновесными. Реальный процесс изменения состояния системы будет тем ближе к равновесному, чем медленнее он совершается, поэтому равновесные процессы называют квазистатическими.
Неравновесный процесс - Называется процесс, при протекании которого система не находится в состоянии равновесия (т.е. при протекании процесса различные части системы имеют разные температуры, давление, плотности,концентрации и т.д.).
Обратимый процесс (то есть равновесный) — термодинамический процесс, который может проходить как в прямом, так и в обратном направлении, проходя через одинаковые промежуточные состояния, причем система возвращается в исходное состояние без затрат энергии, и в окружающей среде не остается макроскопических изменений.
Обратимый процесс можно в любой момент заставить протекать в обратном направлении, изменив какую-либо независимую переменную на бесконечно малую величину.
Обратимые процессы дают наибольшую работу. Бо́льшую работу от системы вообще получить невозможно. Это придает обратимым процессам теоретическую важность. На практике обратимый процесс реализовать невозможно. Он протекает бесконечно медленно, и можно только приблизиться к нему.
Цикл круговые процессы в термодинамике, то есть такие процессы, в которых начальные и конечные параметры, определяющие состояние рабочего тела (давление, объём, температура, энтропия), совпадают.
Теплова́я маши́на — устройство, преобразующее тепловую энергию в механическую работу (тепловой двигатель) или механическую работу в тепло (холодильник). Преобразование осуществляется за счёт изменения внутренней энергии рабочего тела — на практике обычно пара или газа.
В течение цикла рабочее тело теплового двигателя получает от нагревателя количество теплоты Q1, совершает работу А и отдает некоторое количество теплоты Q2 < Q1 холодильнику. Все процессы совершаются квазистатически, что обеспечивает их обратимость.
Цикл Карно́ — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов.
