- •Общая геология
- •Учебное пособие для иностранных студентов
- •Введение
- •Строение и состав земли
- •Фигура и размеры Земли
- •1.2. Геофизические поля и физические свойства Земли
- •1.3. Внутреннее строение Земли
- •1.4. Агрегатное состояние вещества и химический состав геосфер
- •2. Геологические процессы и документы
- •Эндогенные – это внутренние процессы; экзогенные – внешние, поверхностные, для них источник энергии – это энергия Солнца и сила тяжести (гравитационное поле Земли).
- •2.1. Минералы
- •2.1.1. Формы нахождения минералов в природе
- •2.1.2. Классификация минералов
- •2.2. Горные породы
- •2.2.1. Магматические горные породы
- •2.2.2. Осадочные горные породы
- •2.2.3. Метаморфические породы
- •Экзогенные процессы
- •2.3.1. Выветривание
- •2.3.1.1. Физическое выветривание
- •2.3.1.2. Химическое выветривание
- •2.3.1.3. Органическое выветривание
- •2.3.1.4. Элювий и кора выветривания
- •2.3.1.5. Геологическая роль выветривания
- •2.3.2. Геологическая деятельность ветра
- •2.3.2.1. Типы ветров и воздушных потоков
- •Шкала скоростей ветра
- •2.3.2.2. Виды ветров
- •2.3.2.3. Геологическая работа ветра
- •2.3.2.3.1. Разрушительная работа ветра
- •2.3.2.3.2. Перенос материала ветром
- •2.3.2.3.3. Эоловая аккумуляция
- •2.3.2.4. Типы пустынь
- •2.3.3. Геологическая деятельность поверхностных текучих вод
- •2.3.3.1. Продольный профиль динамического равновесия
- •2.3.3.2. Деятельность временных водотоков
- •2.3.3.3. Деятельность постоянных водотоков
- •2.3.3.4. Стадии развития речной долины
- •2.3.3.5. Речные террасы
- •2.3.4. Геологическая деятельность подземных вод
- •2.3.4.1. Формы существования воды в горных породах
- •2.3.4.2. Коллекторские свойства горных пород
- •2.3.4.3. Происхождение и состав подземных вод
- •2.3.4.4. Условия залегания подземных вод. Водоносные горизонты
- •2.3.4.5. Воды нефтяных и газовых месторождений
- •2.3.4.6. Карстовые процессы
- •2.3.4.7. Отложения подземных вод
- •2.3.4.8. Оползни
- •2.3.5. Геологическая деятельность снега, льда
- •2.3.5.1. Образование и типы ледников
- •2.3.5.2. Геологическая работа ледников
- •2.3.5.3. Оледенения в истории Земли
- •2.3.6. Геологическая деятельность моря
- •2.3.6.1. Строение морского дна и отделы моря
- •2.3.6.2. Физические и химические свойства морской воды
- •2.3.6.3. Биономические зоны моря
- •2.3.6.4. Разрушительная работа моря
- •2.3.6.5. Перенос продуктов разрушения
- •2.3.6.6. Накопление осадков
- •2.3.7. Геологическая деятельность озер и болот
- •2.4. Эндогенные процессы
- •2.4.1. Магматизм
- •2.4.1.1. Общая характеристика магматизма
- •2.4.1.2. Типы магм
- •2.4.1.3. Причины многообразия магматических пород
- •Интрузивный магматизм
- •Эффузивный магматизм
- •Тектонические движения и деформации земной коры
- •Дислокации осадочных пород
- •Землетрясения
- •2.4.3. Метаморфизм и метасоматоз
- •2.4.3.1. Термальный метаморфизм
- •2.4.3.2. Динамометаморфизм
- •2.4.3.3. Метасоматоз
- •2.4.3.4. Типы и условия проявления метаморфизма
- •3. Геологическое летоисчисление (геохронология)
- •3.1. Относительное летоисчисление
- •3.2. Абсолютное летоисчисление
- •3.3. Геохронологическая и международная стратиграфическая шкалы
- •Общая стратиграфическая шкала докембрия
- •4. Строение тектоносферы и земной коры
- •4.1. Модели развития тектоносферы и земной коры
- •4.1.1. Тектонический цикл с позиции фиксизма
- •4.1.2. Тектонический цикл с позиции мобилизма
- •4.2. Основные тектонические структуры земной коры
- •4.2.1. Срединно-океанические хребты
- •4.2.2. Геосинклинали и геосинклинальные зоны
- •4.2.3. Платформы
- •4.3. Восстановление тектонического режима развития земной коры
- •5. Краткая история формирования земной коры
- •Список литературы
- •Общая геология Эндогенные и экзогенные процессы
2.3.1.2. Химическое выветривание
При химическом выветривании разрушение горных пород происходит с изменением их химического состава главным образом под воздействием кислорода, углекислого газа и воды, а также активных органических веществ, содержащихся в атмосфере и гидросфере.
Главными реакциями химического выветривания являются окисление, гидратация, растворение и гидролиз.
Окисление – это переход элемента с низкой валентностью в высоковалентное за счет присоединения кислорода. Особенно быстро окислению подвергаются сульфиды, некоторые слюды и другие темноцветные минералы. В результате образуются оксиды и гидроокиси, например:
Fe++S2 + nH2O + mO2 Fe++SO4 Fe2+++ (SO4)3 Fe+++(OH)3 H2SO4
пирит |
|
сульфат |
сульфат |
|
гидроокись |
|
|
|
закиси |
окиси |
|
трехвалентного |
|
|
|
железа |
железа |
|
железа |
в р–р |
Г етит
(мало H2O)
етит
(мало H2O)
F e(OH)3
Fe2O3
nH2O
e(OH)3
Fe2O3
nH2O
Лимонит (много H2O)
Лимонит – это самая устойчивая форма существования железа в поверхностных условиях. Все ржавые пленки и ржаво-бурая окраска пород обусловлены присутствием гидроокислов железа. Так как железо постоянно входит в химический состав многих породообразующих минералов, значит, при химическом выветривании этих минералов Fe++ перейдет в Fe+++, т.е. лимонит. Окисляется не только Fe, но и другие металлы.
В условиях недостатка кислорода протекает процесс восстановления, при котором металлы с высокой валентностью переходят в соединения с более низкой валентностью. Подобный процесс наиболее ярко протекает в зонах окисления сульфидных месторождений (рис.21).
В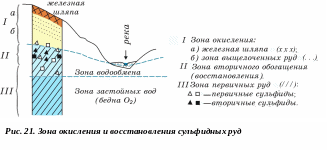 ыше
уровня грунтовых вод располагается
зона обогащения O2,
и
в ней интенсивно протекают процессы
окисления. В результате этого сульфиды
металлов переходят в сульфаты, которые
хорошо растворимы и вместе с водой
перемещаются вниз, ниже уровня грунтовых
вод, в зону, обедненную кислородом. В
этой зоне сульфаты восстанавливаются
и переходят во вторичные сульфиды, в
результате чего возникает зона богатых
руд (зона вторичного обогащения). На
поверхности же рудного тела в результате
окисления и выщелачивания образуется
так называемая железная шляпа, которая
представляет собой каркас кварца,
пропитанного лимонитом. Процессы
окисления и восстановления можно
представить в виде схемы:
ыше
уровня грунтовых вод располагается
зона обогащения O2,
и
в ней интенсивно протекают процессы
окисления. В результате этого сульфиды
металлов переходят в сульфаты, которые
хорошо растворимы и вместе с водой
перемещаются вниз, ниже уровня грунтовых
вод, в зону, обедненную кислородом. В
этой зоне сульфаты восстанавливаются
и переходят во вторичные сульфиды, в
результате чего возникает зона богатых
руд (зона вторичного обогащения). На
поверхности же рудного тела в результате
окисления и выщелачивания образуется
так называемая железная шляпа, которая
представляет собой каркас кварца,
пропитанного лимонитом. Процессы
окисления и восстановления можно
представить в виде схемы:
Первичные сульфиды Ме |
о |
Сульфаты Ме |
в осстановление |
Вторичные сульфиды Ме |
Гидратация – это химическое присоединение воды к минералам горных пород с образованием новых минералов (гидросиликатов и гидроокислов) с другими свойствами.
Fe2O3 + nH2O Fe2O3 nH2O
гематит лимонит
CaSO4 + 2H2O CaSO4 2H2O
ангидрит гипс
превращение ангидрита в гипс всегда сопровождается значительным увеличением объема породы, что приводит к механическому разрушению всей гипсо-ангидритовой толщи.
Растворение – способность молекул одного вещества распространяться вследствие диффузии в другом веществе. Оно происходит с различной скоростью для разных пород и минералов. Наибольшей растворимостью обладают хлориды (галит NaCl, сильвин KCl и др.). Менее растворимы сульфаты, карбонаты.
Гидролиз – наиболее важный процесс химического выветривания, т.к. путем гидролиза разрушаются силикаты и алюмосиликаты, которые слагают половину объема внешней части континентальной коры.
Гидролиз – это обменное разложение вещества под влиянием гидролитической диссоциации воды, которое сопровождается разрушением одних и образованием других минералов. Наиболее характереный пример гидролиза – это гидролиз полевых шпатов:
KAlSi3O8 + nH2O + CO2 K2CO3 + Al4Si4O10(OH)8 + SiO2 nH2O
ортоклаз в раствор каолинит опал
Дальнейший гидролиз каолинита приводит к его разложению и образованию латерита: Al4Si4O10(OH)8 H2Al2O4 + SiO2 nH2O.
латерит
Интенсивность процесса гидролиза, которому сопутствуют растворение и гидратация, зависит от климатических условий: в умеренном климате гидролиз протекает до стадии образования гидрослюд; во влажном теплом климате – до стадии образования каолинита; в субтропическом климате – до стадии образования латерита. Таким образом при гидролизе разрушаются силикаты, алюмосиликаты; на их месте накапливаются глинистые минералы, а за счет вытеснения катионов образуются свободные окислы и гидроокислы алюминия, железа, кремния, марганца.
В целом обобщенную схему гидролиза минералов можно представить в виде последовательных преобразований:
Полевые шпаты |
|
гидрослюды |
|
каолинит |
|
латерит |
A Fe2O3 SiO2 |
nH2O |
|||||
Оливин Роговая обманка Пироксен |
|
Монтмориллонит mMg3Si4O10OH2p(Al,Fe)2Si4O10OH2nH2O Бейделлит Al2Si4O10OH2nH2O |
|
Латерит |
|
||||||||
Латериты являются ценными рудами на алюминий. При перемыве латеритной коры выветривания и переотложении гидроокислов алюминия формируются месторождения бокситов.
Стадии химического выветривания. В соответствии с приведенной последовательностью гидролиза выделяются 4 стадии химического выветривания:
Обломочная, при которой породы превращаются в рыхлые продукты физического выветривания;
Сиаллитная (обызвесткованного элювия), когда начинается разложение силикатов, сопровождаемое удалением хлора, серы, и обогащение пород карбонатами;
Кислая сиаллитная стадия глин, когда продолжается разложение силикатов и происходит отщепление и вынос оснований (Ca, Mg, Na,K), а также образование каолиновых глин на кислых породах и нонтронитовых – на основных;
Аллитная, завершающая стадия химического выветривания, на которой идет дальнейшее разложение минералов (отщепляются и выносятся окислы и гидроокислы алюминия и железа и образуются гетит, гидрогетит и гиббсит, гидраргиллит).

 кисление
кисление


 l2O3
l2O3