
- •Химическая связь
- •Взаимное влияние атомов в органических молекулах
- •Пространственное строение органических молекул
- •Физико-химические методы идентификации
- •Общие закономерности реакционной способности органических соединений
- •Реакционная способность насыщенных углеводородов
- •Непредельные углеводороды
- •Ароматические углеводороды Арены
- •Галогенпроиводные углеводороды
- •Гидроксопроизводные углеводороды
- •Простые эфиры
- •Оксосоединения
- •Овр карбонильныхсоединений
- •Карбоновые кислоты
- •Функциональные производные карбновых кислот
- •Ароматические карбоновые кислоты
Ароматические углеводороды Арены
Это циклические ненасыщенные соединения состава CnH2n-6.
Бензол.Строение:




Все атомы С находятся в sp2 – гибридизации и расположены в одной плоскости в виде правильного шестиугольника. Негибридизованные π-орбитали образуют 3 π-связи, которые являются сопряженными.

Критерии ароматичности:
-
Наличие плосского замкнутого σ-скелета(sp2-гибридизация);
-
Наличие единого сопряженного π-электронного облака;
-
Выполнение правила Хюккеля: (4n + 2)π, где n – целое число.
Моноядерные арены:
CH3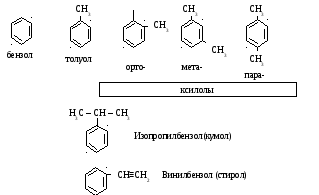
Способы получения бензола и его гомологов:
-
Сухая перегонка каменного угля;
-
Нефть;
-
Тримеризация этина (по Зеинскому);
-
Декарбоксилирование органических кислот:
C6H5COONa (тв.) + NaOH(тв.)→ t С6H6 + Na2CO3
-
Алкилирование по Фриделю-Крафтсу;
-
Синтез по Фиттигу









 Cl
+ 2Na + Cl – R→ R + 2NaCl
Cl
+ 2Na + Cl – R→ R + 2NaCl
Химические свойства:
Наиболее характерны реакции электрофильного замещения SE.









H + Eδ+
- Naδ-→ E
+ H-Na
+ Eδ+
- Naδ-→ E
+ H-Na
Механизм реакции:
- Генерирование электрофильной частицы:
E-Nu + кат.→ Eδ+→ Nuδ-…кат.→E+ +Nu- - кат.
- Электрофильная частица связывается со всеми π-электронами кольца, образуя π-комплекс:












 +
Е+→ Е+ или Е+
+
Е+→ Е+ или Е+
- Образование σ-комплекса:
Е+ забирает два из шести π-электронов, образуя σ-связь с одним из атомов С бензольного кольца.





 Е
Е

 Е+→
Е+→
σ-комплекс неустойчив.
+
- Отщепление протона с возвратом 2х электронов в ароматическую систему.

H+ + Nu- - кат.→H-Nu + кат.
Реакции SE:
- Галогенирование:









 Н + Br2→
FeBr3,
25° Br +HBr
Н + Br2→
FeBr3,
25° Br +HBr
B r-Br
+ FeBr3→Brδ+
- Brδ-
… FeBr3→Br+
+ FeBr4
r-Br
+ FeBr3→Brδ+
- Brδ-
… FeBr3→Br+
+ FeBr4
E+
- Нитрование
Осществляется с помощью нитрующей смеси, представляющей собой смесь HNO3(к.) и H2SO4(к.) в соотношении 1:2.









 Н
+НО – NO2
(к.)→
H2SO4,
60°.
NO2
+ H2O
Н
+НО – NO2
(к.)→
H2SO4,
60°.
NO2
+ H2O
H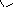 NO3(к.)
+ 2H2SO4(к.)→NO2+
+ H3O+
+ 2HSO4-
NO3(к.)
+ 2H2SO4(к.)→NO2+
+ H3O+
+ 2HSO4-
E+
- Сульфирование









 Н
+ HO – SO3H(к.)→
SO3
SO3H
+ H2O
Н
+ HO – SO3H(к.)→
SO3
SO3H
+ H2O
Электрофил – SO3

- Алкилирование по Фриделю-Крафтсу
а








 )
H + R-Cl
→
AlCl3
R
+ HCl
)
H + R-Cl
→
AlCl3
R
+ HCl
б) алкенами:








 +
CH2 = CH2 →
AlCl3
или Н+
CH2 – CH3
+
CH2 = CH2 →
AlCl3
или Н+
CH2 – CH3
в) спиртами:










H + HO – C2H5→ C2H5 + H2O
R-Cl + AlCl3→Rδ+→Clδ-…AlCl3→R+ AlCl4-
E+







Rδ+ - Clδ-…AlCl3
- Ацилирование по Фриделю-Крафтсу

При введении в бензольное кольцо реакционные способности полученного соединения отличается от реакционных способностей бензола.





Х
Заместители
|
Ориентанты I-ого рода. Это электроно-донорные заместители, которые повышают электронную плотность в кольце, особенно в орто и пара положениях, тем самым активируя реакции с SE и повышая их скорость. OH Вновь входящий заместитель занимает орто и пара положение. |
Ориентанты II-ого рода. Это электроно – акцепторные заестители, которые понижают электронную плотность в кольце, тем самым затрудняя реакции с SE и понижая скорость этих реакций. Вновь входящий заместитель занимает мета положение.
При наличии двух заместителей влияние бывает:
|
Реакции присоединения(связаны с потерей ароматизации):
- Гидрирование:




 + 3Н2→
кат.
+ 3Н2→
кат.
- Хлорирование
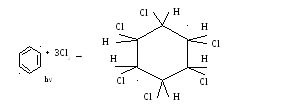
Реакции окисления:
Бензольное кольцо устойчиво к действию обычного окисления.

У гомологов C6H6 легко окисляются боковые цепи

Реакции бокоых цепей:
- Радикальное замещение:

- Окисление.
Конденсированные арены:

Все являются ароматическими, т.к. отвечают критериям ароматичности. Являясь ароматическими, они вступают в реакци SE. У нафталина реакции SE легче идут в α-положении.
- Галогенирование:
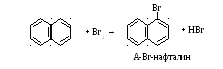
- Сульфирование:

-
α-нафталинсульфокислота менее устойчива из-за отталиквания атомов Н при восьми атомах С. Это кинетический продукт.
-
β-нафталинсульфокислота более устойчива.Термодинамический продукт.
У антроцена и фенантрена подвижны атомы С9 и С10.
- Присоединение:
Гидрирование
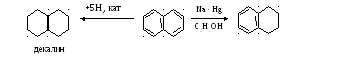
Окисление


Лекция№8


