
- •Химическая связь
- •Взаимное влияние атомов в органических молекулах
- •Пространственное строение органических молекул
- •Физико-химические методы идентификации
- •Общие закономерности реакционной способности органических соединений
- •Реакционная способность насыщенных углеводородов
- •Непредельные углеводороды
- •Ароматические углеводороды Арены
- •Галогенпроиводные углеводороды
- •Гидроксопроизводные углеводороды
- •Простые эфиры
- •Оксосоединения
- •Овр карбонильныхсоединений
- •Карбоновые кислоты
- •Функциональные производные карбновых кислот
- •Ароматические карбоновые кислоты
Физико-химические методы идентификации
Спектральные методы анализа органических соединений:
К ним остносятся:
- Инфракрасные (ИК);
- Ультрафиолетовые( УФ);
- Спектроскопия и спектропия видимой области спектра;
- Спектроскопия комбинационного рассеивания (КР);
- Спектроскопия магнитного резонанса (ЯМР);
- Масспектрометрия;
- Дифракционные методы;
- Рентгенография;
- Электронография;
- Нейтронография;
В основу спектральных методов положено свойство органических молекул поглащать электромагнитное излучение в определенном диапазоне электромагнитного спектра.
Элеткронная спектроскопия
Изучает спектры поглощения в ультрафиаолетовом(≥10-200нм) и видимом диапазонах электромагнитных излучений.
Спектр поглощения в ультрафиалетовой и видимй областях обусловлен электронными переходами в молекулах и поглощенной молекулой энергией, соответствующей ее энергетической разнице.
Электроны образуют σ- и π- связи, а также возбуждаются и переходят на более высокие уровни.
Возможны следующие переходы: σ→σ*, π→π*, n→n*, n→π*
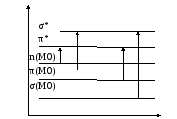
Наряду с энергетческим поглощением электронная спектроскопия характеризует интенсивность поглощения (ε)
ε опеделяет вероятность перехода каждого типа.
С большей вероятностью порисходят электронные переходы между МО одного типа симметрии.
Такие переходы являютсяразрешенными по симметрии и меют большую интенсивность. (σ наσ, π на π).
Переходы типа n на σ* и n на π* являются запрещенными и имеют малую ε.
Этот метод используют для анализа вществ, содержащих кратные связи.
Атомная группировка, содержащая кратные связи, называется хромоформ.
В молекулах с сопряженными хромофоформами поглощение происходит в более длмнной волновой области и с большей интенсивностью, чем в аналдогичной системе с изолированными хромоформами.
К повышению длины волны и εприводит включение в систему хромоформов аутсохромов (групп, содержащащих атом с неподеленной парой электронов).
Для характерных спектральных изменений хромофора используется следующая терминология:
- батохромный сдвиг – смещение полосы в сторону больших длин волн.
- гипсохромный сдвиг – смещение полосы в сторону меньших длин волн.
- гиперхромный эффект – увеличение интенсивности поглощения(ε).
- гипохромный эффект – уменьшение интенсивности поглощения(ε).
Инфракрасная спектроскопия
При действии инфракрасного излучения(4000-400см-1) на органические молекулы происходит возбуждение колебательных движений инфракрасных волн и переход на более высокий колебательный уровень.
Различают два основных типа колбаний:
- валентные (ν);
- дифформационные(δ);
Валентные колебания:
-
Симметричные(νs);
-
Ассимметричные(νas);
Дифформационные колебания:
-
Ножничковые;
-
Маятниковые;
-
Крутильные;
-
Веерные.
В многоатомных молекулах колебания отдельных пар атомов или атомных групп происходит практически независимо от остальных атомов молекулы.
Частота присущая определенной группе и соответствующая ей полоса поглощения называется характеристической.
Интерпритацию к-спектра начинают с начальных частот, которые располагаются в полосах валентных колебаний связей С-Н, >N -,О-Н. Эти полосы обычно интенсивны, а также положение и контур групп, полос или связей С-Н, >N – зависит от наличия или отсутствия водородных связей.
Затем проводят отнесение полос поглощения в область 2500-1900 см-1, которую называют областью спектральных связей.
Важное значение имеет область 1900-1300см-1, т.к. это область двойных связей (С=С, С=О, NО2, Cар=Cар)
Область >1300см-1 содержит много полос, многие из которых трудно отнести к определенному типу колебаний, т.к. они обусловлены колебаниями всего углеродного скелетат в целом.(«Область отпечатков пальцев»)
Спектроскопия ядерного магнитного резонанса
Основано не свойстве ядер некоторых атомов поглощать излучание в диапазоне радио частот. Поглощение энергии радиочастотных излучений характерно только для ядер, обладающих магнитным моментом. К ним относятся ядра с нечетной суммой p+ и n°, т.е. имеющие спиновое квантовое число, неравное 0. (1Н, 12С, 31Р).
Микроскопическический ЯМР 1H называется протоно-магнитным резонансом (ПМР).
При помещение органического вещества в магнитное поле обладающие магнитным моментом ядра атомов Н ориентируются осью вращения вдоль направления силовых линий магнитнго поля.
Две ориентации:
- по направлению поля спин=+1/2;
- против направления поля спин=-1/2.
Первой ориентации соответствует более низкая энергия, чем второй. Следовательно большая часть протонов занимает низшее состояние.
Переход на более высокий энергетический уровень происходит при поглощении радиочастотного излучения с энергией, равной энергетической разности уровней, и переонриентацией спина.
Разные протоны, в зависимости от элктронного окружения, будут резонировать при различных частотах.
Количеством, характеризующим степение ихронизирования ядер, является химический сдвиг(хс/хсб), который представляет собой расстояние между сигналом ядер определенного типа и сигналом ядер эталонного вещества. Эталон – ТМС:тетраметилсилан Si(CH3)4. В нем содержатся 12 эквивалентных сильно экронированных протонов, которые дают интенсивный сигнал сильному полю.
Хс для ТМС=0. Хс исчислятся в миллионных долях и расчитывается по формуле:
![]() , где
, где
ν – резонансная частота протона;
νтмс – резонансная частота ТМС(тетраметилсилана);
ν0 – рабочая частота генератора.
Хс протонов 0-10 м.д.
На значение Хс протонов влияют соседние атомы группы.
Электроно-донорные заместители повышают электронную плотность вокруг и смещают сигнал в сильное поле.
Электроно-акцепторные заместители понижают электронную плотность и смещают сигнал в слабое поле.
Для решения структурных задач важна интенсивность сигналов, которая определяет S подрезонансной кривой и является величиной, пропорциональной количеству протонов определенного типа.
Количество сигналов в спектре ПМР показывает сколько эквивалентных протонов содержится в образце.
Хс указывает на принадлежность протонов к определенной группировке, а интенсивность сигналов определяет количество сигналов в группе.
О строении органического вещества можно судит по форме, структуре сигнала.
Протоны одного типа, достаточно удаленные от протонов другого типа, дают сигнал в виде узкого пика с одним max.
Протоны разного типа дают сигнал, расщепляющихся на ряд линий различной интенсивности, располагающихся на одинаковых расстояниях друг от друга. Такой сигнал называется мультиплетом, а явление спин-спиновым взаимодействием. Оно обусловлено взаимным влиянием магнитных полей соседних протонов и наблюдается в том случае, когда расстояние между неэквивалентными протонами не более 2-3 связей.
Расстояние между ближайшими измеряется в Герцах и носит название константа спин-спинового взаимодействия(J).
(M) – степень расщепления сигнала зависит от количества соседних протонов и определяется по формуле: M=n+1, где n – количество соседних протонов.
Масспектрометрия
Основано на ионизации молек и регистрации спектра масс образовавшихся ионов.
Ионизацию чаще вызвают методом электронного удара. При этом из нейтральной молекулы выбивается 1 ĕ, и образуется положительный ион, молекулярный ион (М+.), который в дальшнейшем претерпевает ряд последовательных распадов с образованием более мелких положительных ионов – форментарных ионов и нейтральных частиц.
М- ĕ→ М+.→ фрагментарные ионы+нейтральные частицы.
Лекция №5
