
- •Раздел 1
- •Глава 1
- •1.1. Предмет аналитической химии
- •1.2. Принцип, метод и методика анализа
- •1.3. Виды анализа
- •1.4. Методы аналитической химии
- •Глава 2
- •Первая аналитическая группа катионов
- •Вторая аналитическая группа катионов
- •Систематический анализ смеси Cl-, Br-, I- - ионов
- •Глава 3
- •3.2. Активность и коэффициент активности
- •Активность (a) - такая концентрация вещества в растворе, при использовании которой свойства данного раствора могут быть описаны теми же уравнениями, что и свойства идеального раствора.
- •0,100 Моль/л
- •0,100 Моль/л
- •3.4. Виды констант химического равновесия, используемые в аналитической химии в аналитической химии используются
- •3.5. Общие принципы расчёта состава равновесных систем
- •Уравнение материального баланса основано на том, что число атомов определённого элемента (или групп атомов определённого вида) в изолированной системе остаётся неизменным.
- •Глава 4
- •4.1. Важнейшие теории кислот и оснований
- •4.3. Влияние растворителя на кислотно-основные свойства растворённого вещества
- •4.4. Нивелирующее и дифференцирующее действие растворителя. Сильные и слабые кислоты и основания
- •Растворы амфолитов
- •4.6. Расчёт состава равновесных смесей протолитов при заданном значении рН
- •4.7. Кислотно-основные буферные растворы
- •Глава 5
- •5.1. Понятие о комплексном соединении
- •5.2. Классификация комплексных соединений
- •5.3. Равновесия в растворах комплексных соединений
- •Природа комплексообразователя и лигандов
- •Концентрация реагентов
- •Ионная сила
- •Температура
- •Побочные реакции
- •Глава 6
- •6.1. Произведение растворимости малорастворимого электролита
- •6.2. Растворимость
- •7,210-4 Моль/л
- •6.3. Влияние различных факторов на растворимость Природа растворяемого вещества и растворителя
- •Температура
- •Ионная сила
- •Общий (одноименный) ион
- •Побочные реакции
- •6.4. Общие принципы растворения осадков малорастворимых электролитов
- •Глава 7
- •Электродные потенциалы
- •Уравнение Нернста
- •7.3. Влияние различных факторов на протекание окислительно-восстановительных реакций Температура
- •Посторонние ионы
- •Влияние рН
- •Образование малорастворимых соединений
- •7.4. Расчёт различных констант с использованием электродного потенциала
- •Глава 8
- •8.1. Отбор пробы
- •8.2. Разложение пробы
- •Глава 9
- •9.2. Жидкость - жидкостная экстракция
- •9.2.2. Экстракционные системы и экстрагенты
- •9.2.4. Влияние различных факторов на процесс экстракции
- •Слабые основания
- •Амфолиты
- •Присутствие сильных электролитов
- •9.2.5 Способы осуществления экстракции
- •9.2.6. Применение экстракции
- •Глава 10
- •10.1. Приближённые вычисления и значащие цифры
- •Сложение и вычитание
- •Деление и умножение
- •Другие операции
- •10.2. Понятие об аналитическом сигнале
- •10.3. Методы расчёта концентрации вещества по величине аналитического сигнала
- •Метод градуировочного графика
- •Метод стандартов
- •10.4. Неопределённость и погрешности измерений
- •10.5. Некоторые основные положения математической статистики, используемые в аналитической химии
- •10.7. Основные характеристики методики анализа
- •Воспроизводимость
- •Правильность
7,210-4 Моль/л
Рис.
6.2.
Равновесия
в системе «осадок малорастворимого
слабого электролита - насыщенный
раствор»
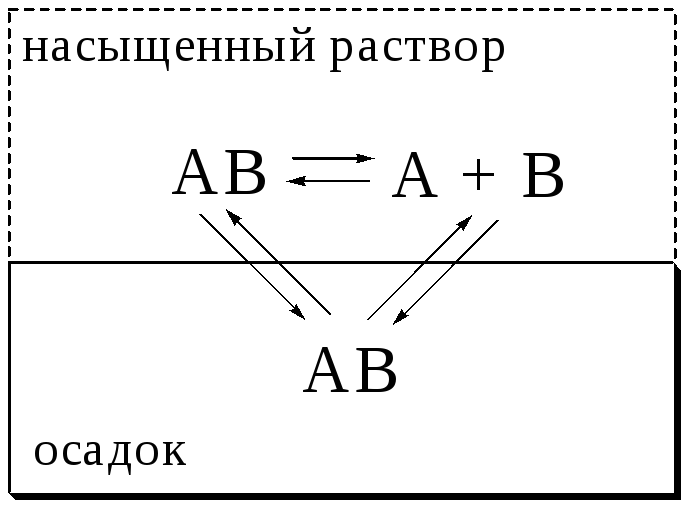
Sобщ = [A] + [AB]
Рассмотрим случай, когда вещество может находиться в растворе в виде незаряженного комплекса.
![]()
![]()
Например, для AgSCN KS = 1,110-12, = 5,6104
![]() моль/л
(около 5% от Sобщ).
моль/л
(около 5% от Sобщ).
Формулу для расчёта S0 слабых кислот можно получить из выражения константы кислотности
![]()
![]()
Например, для бензойной кислоты KS = 1,410-6, Ka = 6,310-5.
![]() моль/л
(около 95% от общей S)
моль/л
(около 95% от общей S)
6.3. Влияние различных факторов на растворимость Природа растворяемого вещества и растворителя
В настоящее время не существует точных правил или каких-то количественных закономерностей, позволяющих предсказать растворимость любого соединения в любом растворителе или хотя бы объяснить возможные случаи растворимости. Поэтому зависимость между химическим строением соединения и его растворимостью в различных растворителях приходится описывать с помощью эмпирических правил, которые обычно носят статистический характер (например, “подобное растворяется в подобном”). На растворимость влияют такие факторы как способность вещества к сольватации данным растворителем, способность растворённого вещества изменять структуру растворителя, кристаллическая модификация осадка, размер частиц осадка и т.д.
Температура
Для большинства малорастворимых электролитов при повышении температуры растворимость в воде увеличивается, что связано с подводом дополнительной энергии, компенсирующей энергию, необходимую для разрушения кристаллической решётки, и действием энтропийного фактора. Исключение составляют некоторые малорастворимые соединения кальция, магния, лития (рис. 6.3). Уменьшение растворимости при повышении температуры может быть связано с разрушением сольватных оболочек и т.д.
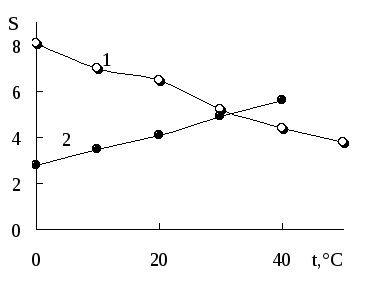
Рис. 6.3. Влияние температуры на растворимость (мг/100 г воды) CaCO3 (1) и PbSO4 (2).
Ионная сила
Увеличение ионной силы раствора приводит к уменьшению коэффициентов активности ионов и к повышению их концентрации в насыщенном растворе над осадком
Явление повышения растворимости малорастворимого электролита при повышении ионной силы раствора называется солевым эффектом.
Пример 6.3. Рассчитать растворимость иодата бария при ионной силе 0,050.
Для расчёта коэффициентов активности ионов при ионной силе 0,050 можно использовать расширенное уравнение Дебая-Хюккеля. Коэффициент а для иона Ba2+ равен 5, а для иона IO3- - 4. В результате расчётов получаем, что у(Ba2+) = 0,46; y(BrO3-) = 0,82.
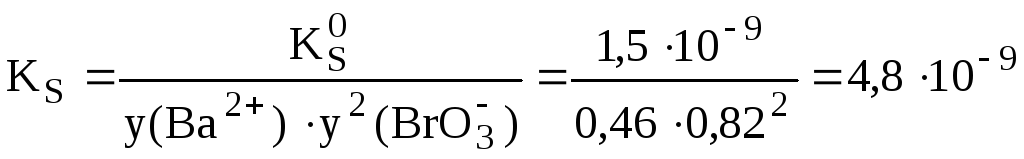
![]() моль/л,
моль/л,
что примерно в 1,5 раза больше, чем при нулевой ионной силе.
Общий (одноименный) ион
Повышение активности в растворе одного иона, образующегося при растворении малорастворимого электролита, должно привести к уменьшению активности второго, так чтобы их произведение осталось неизменным. Если к раствору добавить некоторое количество хорошо растворимого электролита, содержащего такой же ион, что и малорастворимый электролит, то растворимость малорастворимого электролита уменьшится. Такое явление называется эффектом общего (одноименного) иона.
Пример 6.4. Рассчитать растворимость иодата бария в 5,010-2 М NaIO3.
Концентрация
иодат-ионов, образовавшихся при
растворении иодата бария, значительно
меньше, чем 5,010-2
моль/л, поэтому можно принять, что
![]() моль/л. Для расчётов воспользуется
полученным в примере 6.3 концентрационным
произведением растворимости иодата
бария при I = 5,010-2.
моль/л. Для расчётов воспользуется
полученным в примере 6.3 концентрационным
произведением растворимости иодата
бария при I = 5,010-2.
![]() моль/л
моль/л
По сравнению с примером 6.3 растворимость иодата бария уменьшилась примерно на 3 порядка. Таким образом, влияние эффекта общего иона на растворимость сказывается значительно сильнее, чем влияние солевого эффекта.
При увеличении концентрации иона-осадителя растворимость осаждаемого иона уменьшается. Исходя из этого можно сделать неверное заключение о том, что при добавлении бесконечно большого его избытка растворимость интересующего нас соединения станет бесконечно малой. Молекулярная растворимость не зависит от концентрации иона осадителя в растворе. Она представляет собой предел, ниже которого растворимость осаждаемого соединения уменьшить при добавлении избытка иона-осадителя невозможно. В ряде случаев добавление значительного избытка общего иона приводит к повышению растворимости, например, за счёт протекания побочных реакций комплексообразования (рис. 6.4).
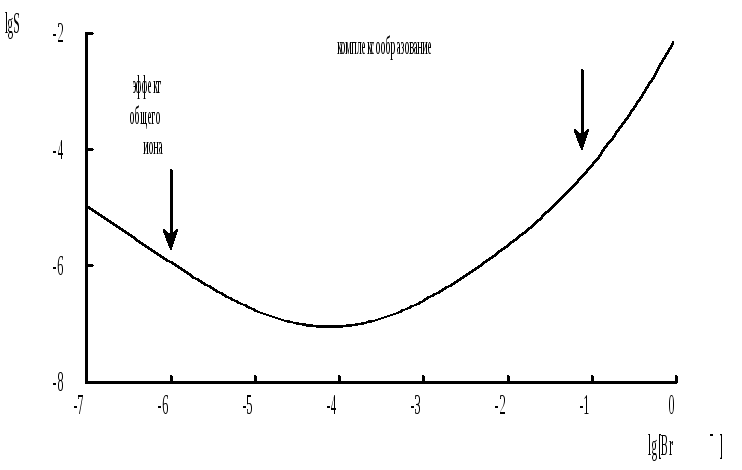
Рис. 6.4 Зависимость растворимости AgBr (размерность S - моль/л) от lg[Br-]
Для малорастворимых кислот и оснований одноименными ионами в водных растворах являются, соответственно, H3O+ и OH-.
Пример 6.5. При каком значении рН начнёт осаждаться Fe(OH)3 (KS = 6,310-38) из раствора с концентрацией Fe3+ 1,010-2 моль/л? При каком значении рН осаждение ионов железа можно считать полным?
Будем считать, что 1,010-2 М - это равновесная концентрация ионов Fe3+.
![]()
![]() моль/л
моль/л
![]()
Осаждение считается полным, если остаточная концентрация осаждаемого иона в растворе становится меньше, чем 110-6 моль/л. Осаждение Fe3+ можно считать полным при рН > 3,6.
