
- •1. Моделі атома Томпсона та Резерфорда. Позитивна сторона моделей і їх недоліки.
- •2.Спектр атома водню. Узагальнена формула Больцмана
- •3. Постулати Бота. Спектр атома водню по Бору
- •4. Гіпотеза Луї де Бройля. Корпускулярно-хвильовий дуалізм матерії;
- •5. Розмір, склад та заряд атомного ядра. Масове та зарядове число
- •6. Дефект маси та енергія зв’язку ядра. Питома енергія зв’язку
- •7 Ядерні сили. Властивості ядерних сил
- •8 Радіоактивне випромінювання та його типи
- •9 Закон Радіоактивного розпаду. Активність нукліда. Правило зміщення
- •10 Гама випромінювання та його властивості
- •11 Ядерні реакції та їх класифікація
- •12 Реакції поділу ядер. Ланцюгові реакції. Поняття про ядерну енергетику
4. Гіпотеза Луї де Бройля. Корпускулярно-хвильовий дуалізм матерії;
Як
показано в розділі 6, світло володіє як
хвильовими, так і корпускулярними
властивостями. Луї де Бройль (1924 рік)
висунув гіпотезу (постулат) про те, що
корпускулярно-хвильовий дуалізм
притаманний не тільки світлу, але матерії
взагалі: усяка частинка, яка має імпульс
![]() і енергію Е,
володіє хвильовими властивостями, її
рух супроводжується хвильовим процесом
з довжиною хвилі де-Бройля
і енергію Е,
володіє хвильовими властивостями, її
рух супроводжується хвильовим процесом
з довжиною хвилі де-Бройля
![]() (7.11)
(7.11)
та частотою
![]() . (7.12)
. (7.12)
В
залежності від величини швидкості v
(кінетичної енергії
![]() )
частинок, їх імпульс розраховується
або за класичною формулою (при
)
частинок, їх імпульс розраховується
або за класичною формулою (при
![]() )
)
![]() ,
(7.13)
,
(7.13)
або
за релятивістською формулою (при
![]() ,
Еk
співмірна з Е0)
,
Еk
співмірна з Е0)
![]() , (7.14)
, (7.14)
де
m
– маса частинки (таблична величина),
![]() – її енергія спокою.
– її енергія спокою.
Зокрема, вільна частинка, що рухається вздовж осі х, описується плоскою хвилею де Бройля
![]() , (7.15)
, (7.15)
де
![]() – амплітуда хвилі де Бройля,
– амплітуда хвилі де Бройля,
![]() – її циклічна частота,
– її циклічна частота,
![]() – її хвильове число. Фазова швидкість
хвиль де Бройля
– її хвильове число. Фазова швидкість
хвиль де Бройля
![]()
![]() , (7.16)
, (7.16)
а групова швидкість
![]() (7.17)
(7.17)
Борівське квантування моменту імпульсу орбітального руху електрона набуває нового змісту з врахуванням хвильових властивостей електрона. Зокрема, довжина стаціонарної орбіти
![]() ,
,
тобто в межах орбіти вкладається ціле число хвиль де Бройля.
Оцінимо
довжину хвилі де Бройля електрона, який
прискорився електричним полем
![]() .
Саме такі напруги використовуються у
вакуумних електронних приладах
(радіолампи, ЕПТ, рентгенівські трубки
тощо). Підставляючи в формулу (7.13) значення
кінетичної енергії електронів
.
Саме такі напруги використовуються у
вакуумних електронних приладах
(радіолампи, ЕПТ, рентгенівські трубки
тощо). Підставляючи в формулу (7.13) значення
кінетичної енергії електронів
![]() еВ,
отримаємо за (7.11) для довжин хвиль де
Бройля
еВ,
отримаємо за (7.11) для довжин хвиль де
Бройля
![]() нм.
нм.
Відомо, що найбільш чітко хвильові властивості світла проявляються в явищі дифракції. І тому прояв хвильових властивостей електронних (нейтронних, атомних тощо) пучків слід очікувати в цьому ж явищі. При цьому чітка дифракційна гратка спостерігається тоді, коли довжини хвиль співмірні з розміром дифракційної неоднорідності (отвори, щілини тощо).
Розміри
макроприладів значно перевищують
довжини хвиль де Бройля електронів, і
тому в цьому випадку хвильові властивості
електронів явно не відслідковуються.
В цей же час розраховані значення
співмірні з розміром (![]() нм)
кристалічної гратки твердих тіл. І тому
така гратка повинна бути дифракційним
пристроєм для електронних пучків.
Дійсно, при проходженні електронних
пучків через тонкі полікристалічні
плівки та при їх відбиванні від
монокристалів спостерігається така ж
дифракційна картина, як і при взаємодії
рентгенівських променів з твердими
кристалічними тілами. Зокрема, виконується
закон Вульфа-Бреггів (див. розділ 6),
встановлений для рентгенівських
променів. Дифракція нейтронних пучків
також виявлена експериментально і
використовується для наукових досліджень.
нм)
кристалічної гратки твердих тіл. І тому
така гратка повинна бути дифракційним
пристроєм для електронних пучків.
Дійсно, при проходженні електронних
пучків через тонкі полікристалічні
плівки та при їх відбиванні від
монокристалів спостерігається така ж
дифракційна картина, як і при взаємодії
рентгенівських променів з твердими
кристалічними тілами. Зокрема, виконується
закон Вульфа-Бреггів (див. розділ 6),
встановлений для рентгенівських
променів. Дифракція нейтронних пучків
також виявлена експериментально і
використовується для наукових досліджень.
В
Рис. 7.5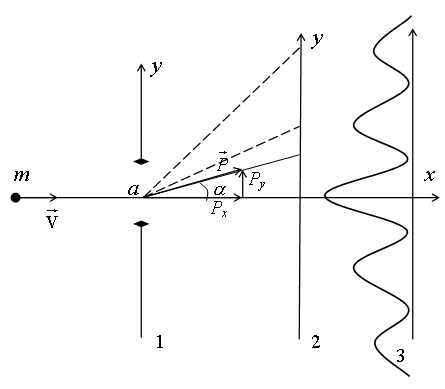
5. Розмір, склад та заряд атомного ядра. Масове та зарядове число
Поняття про ядро атома як центральну позитивно заряджену масивну частину атома, навколо якої рухаються електрони, ввів Е.Резерфорд (1911 р.) на основі своїх дослідів по розсіянню -частинок речовиною. Позитивний заряд ядра чисельно рівний сумі негативних зарядів електронів нейтрального атома. За обрахунками Резерфорда радіус ядра rя ~ 10-15м (радіус атома rа ~ 10-10м). Плідність ядерної моделі атома проілюструвала теорія атома водню Н.Бора (1913 р.). Після того як Г. Мозлі (1913 р.) експериментально показав, що позитивний заряд ядра
![]() , (8.1)
, (8.1)
де Z – порядковий номер елемента в таблиці Менделєєва, а е – елементарний електричний заряд, чисельно рівний зарядові електрона (е = 1,6·10-19 Кл.), уявлення про ядро атома стало загальноприйнятим.
В
ядерній фізиці за одиницю заряду
приймають елементарний заряд е,
а за одиницю маси – атомну одиницю маси
(а. о. м.). 1 а. о. м. рівна
![]() маси нукліда вуглецю
маси нукліда вуглецю
![]() .
Очевидно,
.
Очевидно,
![]() ,
,
де
![]() – число Авогадро. В таких одиницях Q = Z
(Z
називають зарядовим
числом ядра), а маси атомів різних
елементів виражаються числами, близькими
до цілих. Заокруглена до найближчого
цілого маса атома даного елемента,
виражена в а. о. м., називається масовим
числом елемента А.
– число Авогадро. В таких одиницях Q = Z
(Z
називають зарядовим
числом ядра), а маси атомів різних
елементів виражаються числами, близькими
до цілих. Заокруглена до найближчого
цілого маса атома даного елемента,
виражена в а. о. м., називається масовим
числом елемента А.
Зарядове
число Z
і
масове число А
є основними характеристиками будь-якого
ядра, тому ядро даного елемента
позначається хімічним символом цього
елемента з індексами Z
та А
(![]() ).
Наприклад, ядро атома водню позначається
).
Наприклад, ядро атома водню позначається
![]() .
Цю частинку Резерфорд (1919 р.) назвав
протоном (
.
Цю частинку Резерфорд (1919 р.) назвав
протоном (![]() або
або
![]() ).
Оскільки маса електрона
).
Оскільки маса електрона
![]() ,
електрон позначають
,
електрон позначають
![]() .
.
Спочатку
була запропонована протонно-електронна
модель будови ядра, згідно з якою ядро
![]() складається з А
протонів і А – Z
електронів. Однак ця гіпотеза зустрілась
з труднощами, однією з яких виявилась
так звана «азотна катастрофа» –
неможливість пояснити в рамках цієї
гіпотези одиничний спін ядра азоту
складається з А
протонів і А – Z
електронів. Однак ця гіпотеза зустрілась
з труднощами, однією з яких виявилась
так звана «азотна катастрофа» –
неможливість пояснити в рамках цієї
гіпотези одиничний спін ядра азоту
![]() (в одиницях ).
Спін цього ядра, яке містило б непарне
число протонів і електронів (21), мав би
бути напівцілим. Крім того, зі співвідношення
невизначеностей випливає, що електрони
не можуть входити до складу ядра, бо їх
швидкість там була б більшою від с.
(в одиницях ).
Спін цього ядра, яке містило б непарне
число протонів і електронів (21), мав би
бути напівцілим. Крім того, зі співвідношення
невизначеностей випливає, що електрони
не можуть входити до складу ядра, бо їх
швидкість там була б більшою від с.
У
1932 р. Дж. Чедвік відкрив нову нейтральну
елементарну частинку – нейтрон (n
або
![]() ).
Д.Д. Іваненко і С.М. Гапон (1932 р.)
висунули гіпотезу, що ядро атома
складається з нуклонів – протонів і
нейтронів. Ця гіпотеза була розвинена
В. Гейзенбергом і дістала пряме
дослідне підтвердження по розщепленню
ядер на протони і нейтрони.
).
Д.Д. Іваненко і С.М. Гапон (1932 р.)
висунули гіпотезу, що ядро атома
складається з нуклонів – протонів і
нейтронів. Ця гіпотеза була розвинена
В. Гейзенбергом і дістала пряме
дослідне підтвердження по розщепленню
ядер на протони і нейтрони.
Детальне
вивчення нуклонів показало, що протон
– стабільна елементарна частинка з
зарядом +1 і масою
![]() Він має спін
Він має спін
![]() (в одиницях )
і магнітний момент
(в одиницях )
і магнітний момент
![]() ,
де
,
де
![]() – так званий ядерний магнетон. Нейтрон
– нейтральна частинка з масою
– так званий ядерний магнетон. Нейтрон
– нейтральна частинка з масою
![]() ,
спіном
,
спіном
![]() і магнітним моментом
і магнітним моментом
![]() (знак мінус вказує, що магнітний і
спіновий моменти нейтрона антипаралельні);
(знак мінус вказує, що магнітний і
спіновий моменти нейтрона антипаралельні);
![]() ,
причому
,
причому
![]() .
У вільному стані нейтрон нестабільний,
його середній час життя 15
хв.
.
У вільному стані нейтрон нестабільний,
його середній час життя 15
хв.
У
відповідності з нуклонною моделлю ядро
![]() містить А
нуклонів, в тому числі Z
протонів і N = A – Z
нейтронів. Отже, зарядове число Z,
яке співпадає з порядковим номером
елемента в таблиці Менделєєва, визначає
кількість протонів у ядрі і кількість
електронів у атомі. Масове число А
визначає загальну кількість нуклонів
у ядрі.
містить А
нуклонів, в тому числі Z
протонів і N = A – Z
нейтронів. Отже, зарядове число Z,
яке співпадає з порядковим номером
елемента в таблиці Менделєєва, визначає
кількість протонів у ядрі і кількість
електронів у атомі. Масове число А
визначає загальну кількість нуклонів
у ядрі.
Ядра
з однаковими Z
називаються ізотопами, з однаковим А
– ізобарами, з однаковими N
– ізотонами, з однаковими Z
і А
(але різними періодами піврозпаду) –
ізомерами. Наприклад, протій
![]() ,
дейтерій
,
дейтерій
![]() ,
тритій
,
тритій
![]() є ізотопами водню; ядра
є ізотопами водню; ядра
![]() ,
,
![]() є ізобарами. Всього відомо понад 1500
різних ядер, які чим-небудь відрізняються;
приблизно
є ізобарами. Всього відомо понад 1500
різних ядер, які чим-небудь відрізняються;
приблизно
![]() з них стабільні, решта – радіоактивні.
з них стабільні, решта – радіоактивні.
В
природі зустрічаються елементи з атомним
номером Z
від 1 до 92 (крім
![]() і
і
![]() ).
Трансуранові елементи, починаючи з
Z = 93,
були одержані штучно шляхом різних
ядерних реакцій. Згідно з сучасними
уявленнями хімічні елементи виникли в
процесі нуклеосинтезу на етапі зоряної
еволюції Всесвіту. За час існування
Землі (5·109
р.) трансуранові елементи із-за відносно
малого часу життя не збереглися в земній
корі. Елементи з 93-го по 101-й були одержані
в основному реакторним шляхом. Елементи
зі 102-го по 118-й були одержані шляхом
бомбардування важких ядер іншими важкими
ядрами. Межу періодичної системи
елементів повинна визначати нестабільність
відносно спонтанного поділу надважких
ядер.
).
Трансуранові елементи, починаючи з
Z = 93,
були одержані штучно шляхом різних
ядерних реакцій. Згідно з сучасними
уявленнями хімічні елементи виникли в
процесі нуклеосинтезу на етапі зоряної
еволюції Всесвіту. За час існування
Землі (5·109
р.) трансуранові елементи із-за відносно
малого часу життя не збереглися в земній
корі. Елементи з 93-го по 101-й були одержані
в основному реакторним шляхом. Елементи
зі 102-го по 118-й були одержані шляхом
бомбардування важких ядер іншими важкими
ядрами. Межу періодичної системи
елементів повинна визначати нестабільність
відносно спонтанного поділу надважких
ядер.
Слід
враховувати, що сукупність А
нуклонів ядра не є класичною статичною
системою, це – суто квантова динамічна
система. Кожний нуклон, крім спіну
![]() ,
внаслідок руху має орбітальний момент
імпульсу
,
внаслідок руху має орбітальний момент
імпульсу
![]() ,
отже, – і повний момент імпульсу
,
отже, – і повний момент імпульсу
![]() ,
тому повний момент імпульсу (спін) ядра
,
тому повний момент імпульсу (спін) ядра
![]() .
Ця величина квантується за законом
.
Ця величина квантується за законом
![]() ,
де
,
де
![]() – спінове ядерне квантове число, що
пробігає значення
– спінове ядерне квантове число, що
пробігає значення
![]() При парному А
спін ядра цілий, при непарному А
– напівцілий. Спіни ядер не перевищують
декількох одиниць: це свідчить, що спіни
більшості нуклонів ядра компенсуються.
При парному А
спін ядра цілий, при непарному А
– напівцілий. Спіни ядер не перевищують
декількох одиниць: це свідчить, що спіни
більшості нуклонів ядра компенсуються.
Зі
спіном ядра зв’язаний його магнітний
момент
![]() співвідношенням
співвідношенням
![]() ,
де
,
де
![]() – гіромагнітний множник для ядра.
Магнітні моменти ядер зумовлені власними
магнітними моментами нуклонів і
орбітальним рухом протонів. Суттєво,
що власні магнітні моменти нуклонів
ядра не адитивні. Оскільки L
квантується, μ
також квантується, тому енергія магнітної
взаємодії електрона з ядром набуває
дискретних значень. Це приводить до
виникнення надтонкої структури спектрів
атомів, вивчення якої дає можливість
визначати магнітні моменти ядер.
– гіромагнітний множник для ядра.
Магнітні моменти ядер зумовлені власними
магнітними моментами нуклонів і
орбітальним рухом протонів. Суттєво,
що власні магнітні моменти нуклонів
ядра не адитивні. Оскільки L
квантується, μ
також квантується, тому енергія магнітної
взаємодії електрона з ядром набуває
дискретних значень. Це приводить до
виникнення надтонкої структури спектрів
атомів, вивчення якої дає можливість
визначати магнітні моменти ядер.
Крім магнітного моменту ядро має також електричний квадрупольний момент eQ, який характеризує відхилення розподілу заряду в ядрі від сферично-симетричного; Q – коефіцієнт, що має розмірність площі. Для сферично-симетричного ядра Q = 0; якщо Q > 0, ядро витягнуте, якщо Q < 0 – сплюснуте.
Ефективний радіус ядра виражається емпіричною формулою
![]() , (8.2)
, (8.2)
де
r0 = (1,3 – 1,7) фермі (Ф);
1Ф = 10-15м.
Це – розміри тієї області, де проявляється
дія ядерних сил. Як видно, об’єм ядра
пропорційний до кількості його нуклонів;
тому густина ядерної речовини для всіх
ядер однакова і є величиною
![]() .
.
