
- •Физические методы качественного химического анализа. Метод газовой хроматографии. Молекулярный анализ. Идентификация компонентов в пробе вещества
- •Тема: «физические методы качественного химического анализа. Метод газовой хроматографии. Молекулярный анализ. Идентификация компонентов в пробе вещества» Введение
- •Принцип метода
- •Средства измерений
- •Характеристики удерживания
- •Экспериментальная часть
Принцип метода
Хроматографические методы химического анализа относятся к группе физических методов по способу сравнения с эталоном количества компонента.
Физические методы качественного химического анализа вещества основаны на обнаружении наличия определённого физического свойства у определяемого компонента и отсутствующего у сопутствующих компонентов при одном и том же физическом воздействии на вещество объекта анализа. Результат качественного анализа – это принятие решения о наличии или отсутствии искомого компонента в веществе объекта анализа (обнаружение и идентификация компонента).
Физические методы количественного химического анализа вещества основаны на градуировке средства измерения соответствующего физического свойства по определяемому компоненту, построении градуировочного графика в координатах «интенсивность измеренного физического свойства – содержание компонента», измерении интенсивности физического свойства анализируемой аналитической пробы вещества, нахождении содержания компонента в анализируемой пробе из градуировочного графика.
Аналитическая хроматография – это метод, позволяющий идентифицировать и определить компонентный состав пробы многокомпонентного вещества из одной навески. Это возможно вследствие того, что в приборах – хроматографах совмещены два блока – блок подготовки пробы вещества к измерению физического свойства, в котором происходит разделение компонентов, и измерительный блок, в котором измеряется физическое свойство отдельно для каждого компонента и его измерительный сигнал регистрируется также отдельно.
Разделение компонентов многокомпонентного вещества основано на их распределении между двумя несмешивающимися фазами – неподвижной и подвижной, за счет процессов сорбции. Подвижную фазу под давлением с постоянной скоростью пропускают через хроматографическую колонку, заполненную неподвижной фазой (сорбентом).
В газовой хроматографии подвижная фаза представляет собой поток инертного газа, а в жидкостной хроматографии – поток инертного жидкого растворителя или раствора.
Неподвижная фаза представляет собой либо твердое пористое вещество, либо пленку жидкости, нанесенную на твердое вещество. В первом случае твердое вещество является сорбентом, во втором – твердым носителем, а сорбентом будет служить пленка жидкости.
Пробу в объеме 2-5 см3 (газовая), 1 мкм3 – 10 мм3 (жидкая) с помощью шприца-дозатора или инжектора вводят в подвижную фазу.
Разделение пробы многокомпонентного вещества на составляющие его компоненты А, Б и В и т.д. происходит вследствие различий в скорости перемещения компонентов вдоль хроматографической колонки. Это различие связано с различием в силе физического взаимодействия химических компонентов пробы с неподвижной фазой (явление адсорбции и абсорбции). На поверхности твердого сорбента (адсорбция) или в объёме жидкой плёнки (абсорбция) в каждый момент времени совершается элементарный акт сорбции и следом десорбции за счет движения подвижной фазы. Длительность этого момента времени зависит от химической природы компонента и сорбента. Многократное повторение элементарных актов сорбции и десорбции приводят к тому, что при достаточно большом времени движения вдоль хроматографической колонки с сорбентом компоненты пробы вещества разделяются.
Другими словами, через колонку быстрее движется тот компонент, сорбционные свойства которого слабее. Например, сильно адсорбирующиеся на полярном сорбенте полярные молекулы определить либо не удается, либо анализ длится несколько часов. Скорость перемещения вдоль колонки больше также у тех компонентов, у которых выше летучесть, меньше температура кипения и меньше растворимость в жидкой неподвижной фазе сорбента. В результате этих эффектов одни компоненты при передвижении подвижной фазы вдоль хроматографической колонки с сорбентом останутся в верхнем слое сорбента, другие, из-за меньшей степени взаимодействия с сорбентом, окажутся в нижней части колонки, не сорбируемые компонеты покинут колонку вместе с фиксированной дозой подвижной фазы.
Аналитический сигнал компонентов вещества формируется и регистрируется в блоке хроматографа, который называется детектором. Детектор присоединяется к хроматографической колонке. В оптимальных условиях произойдет разделение компонентов пробы вещества и каждый компонент поступит в детектор в потоке подвижного носителя отдельно от других компонентов в определенной последовательности. Регистрирующее устройство запишет сформированные в детекторе аналитические сигналы компонентов на диаграммной ленте самописца или на экране компьютера в координатах «интенсивность выходного сигнала – время». Отсчет времени ведется от времени вводы пробы вещества в хроматограф.
Аналитический сигнал каждого компонента имеет форму пика. Совокупность пиков всех компонентов пробы, представляющих собой непрерывную кривую, называют хроматограммой, рис.1.
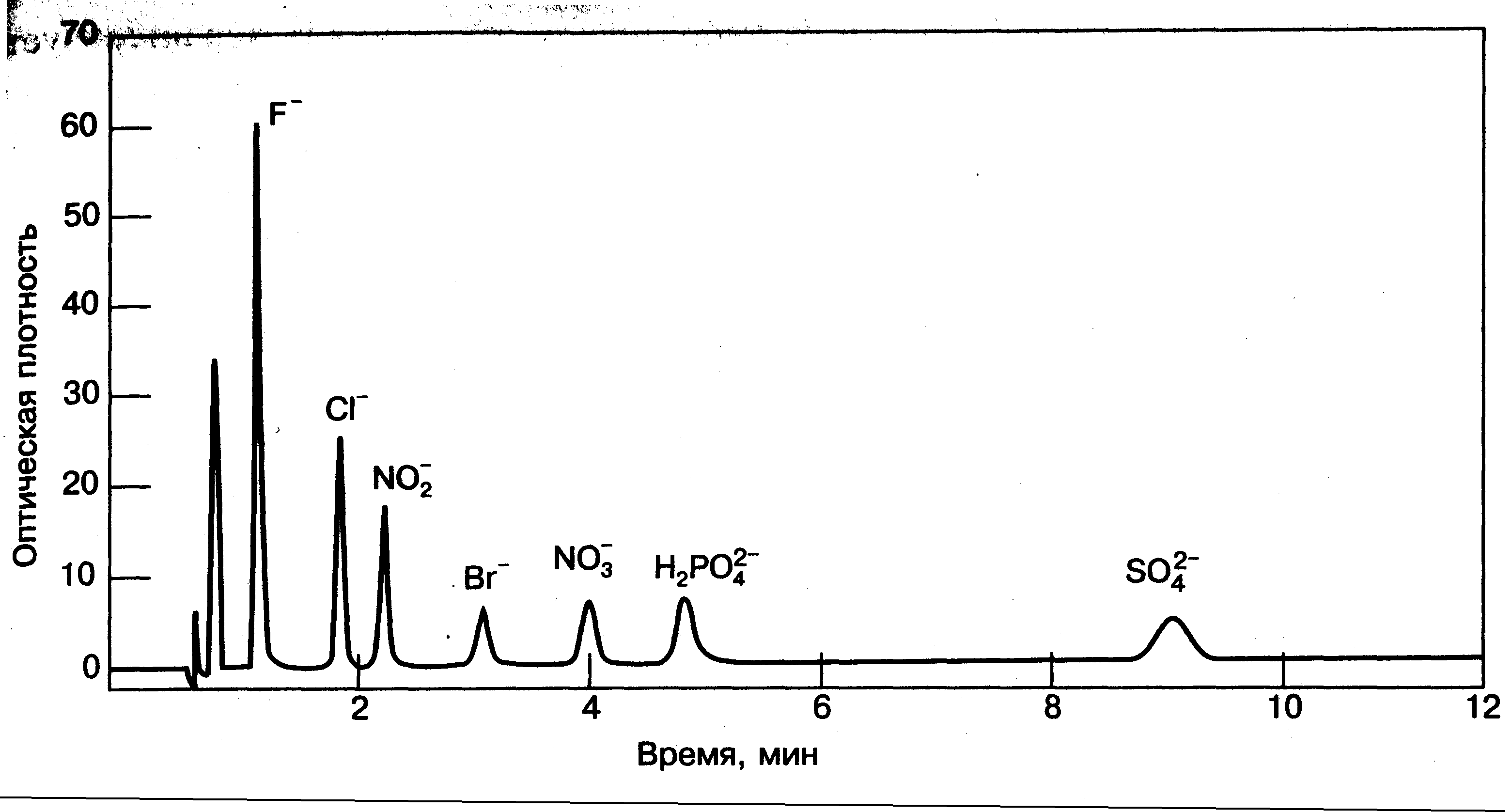
Рис. 1. Аналитические сигналы (хроматограмма) анионов, разделённых в жидкостном ионном хроматографе [Кристиан Г. Аналитическая химия: в 2 т. – Т. 2 – М.: БИНОМ. Лаборатория знаний, 2009. – 504 с. – Рис.21.16, С. 233.]
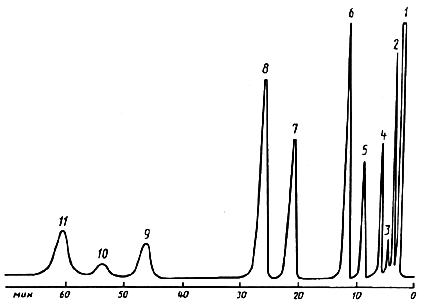
На рисунке 2 представлена типичная хроматограмма пробы вещества природного газа, измеренная на газовом хроматографе с детектором по теплопроводности. Компоненты вещества природного газа разделены на хроматографической колонке с эфиром ТЭГМ, нанесенным на сорбент сферохром.
Время
Рис. 2 Аналитические сигналы (хроматограмма) молекул природного газа, разделённых в газовом хроматографе [ГОСТ 23781-87 Государственный стандарт Союза ССР. Газы горючие природные. Хроматографический метод определения компонентного состава]
1 – метан + неуглеводородные газы; 2 – этан; 3 - диоксид углерода; 4 – пропан; 5 –и-бутан; 6 – н-бутан; 7 – и-пентан; 8 – н-пентан; 9 – 2-метилпентан + 2,3-диметилбутан; 10 – 3-метилпентан; 11 – н-гексан
Подбирая экспериментально химическую природу сорбента, размер его гранул, размеры колонки, температуру колонки, химическую природу подвижного носителя и скорость его движения вдоль колонки, можно разделить довольно сложные многокомпонентные вещества, например, нефти, нефтепродукта, руды редкоземельных элементов и идентифицировать их компоненты, рис.3.
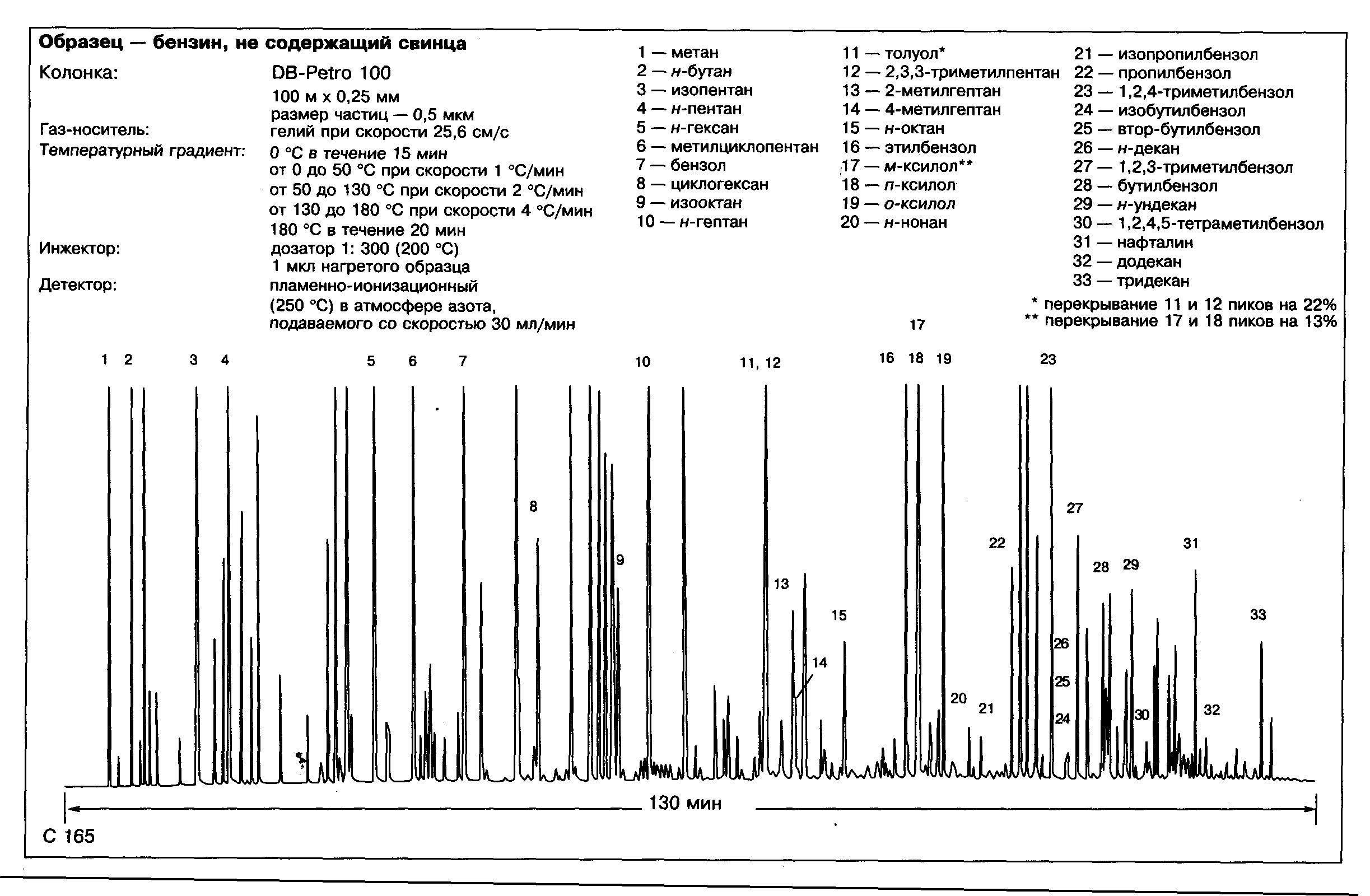 Рис.
3. Пример хроматограммы бензина
(многокомпонентное вещество), разделённой
на капиллярной колонке газового
хроматографа
[Кристиан
Г. Аналитическая
химия: в 2 т. – Т. 2 – М.: БИНОМ. Лаборатория
знаний, 2009. – 504 с. – Рис.20.3, С. 162.]
Рис.
3. Пример хроматограммы бензина
(многокомпонентное вещество), разделённой
на капиллярной колонке газового
хроматографа
[Кристиан
Г. Аналитическая
химия: в 2 т. – Т. 2 – М.: БИНОМ. Лаборатория
знаний, 2009. – 504 с. – Рис.20.3, С. 162.]
Так как аналитический сигнал компонента регистрируется в форме пика, то интенсивность любого измеренного физического свойства этого компонента пропорционально высоте пика или его площади. Поэтому градуировочный график в количественном анализе методом аналитической хроматографии строят в координатах «высота пика, мм (или площадь пика, мм2 ) – содержание компонента», рис.4.
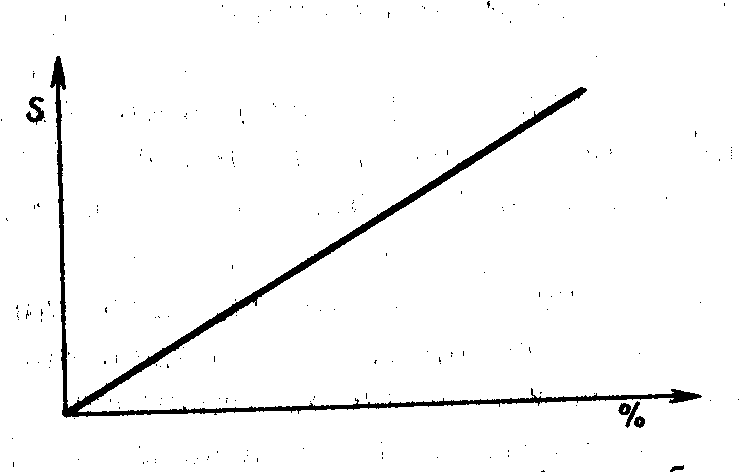
Рис. 4. Общий вид градуировочного графика в аналитической хроматографии [Пецев Н., Коцев Н. Справочник по газовой хроматографии: Пер. с болг. – М.: Мир, 1987. – 260 с. – Рис.12.14, с.125]
Время, соответствующее максимальному значению интенсивности аналитического сигнала компонента (высоте пика), называют временем удерживания компонента (tR), рис.5.
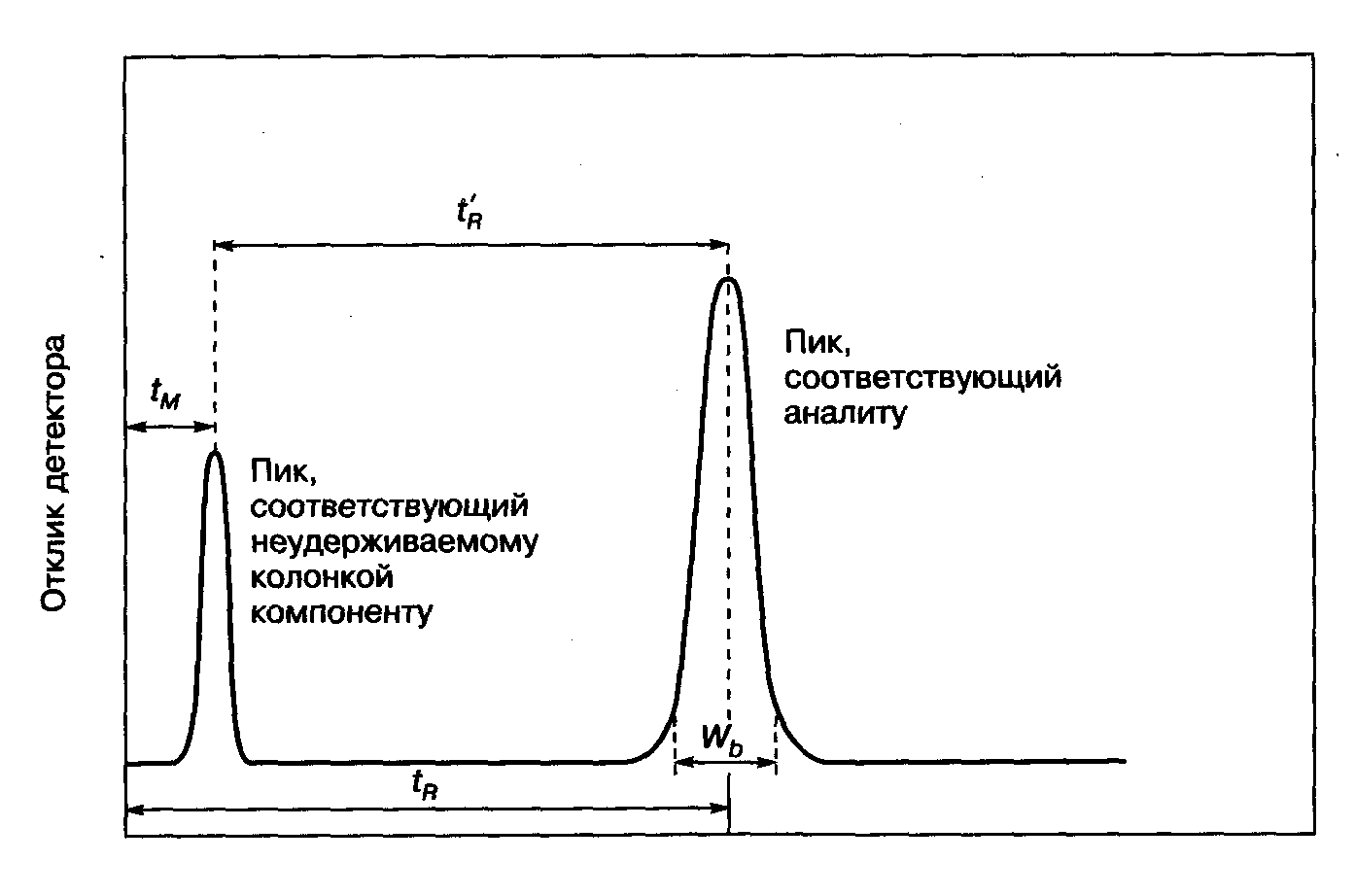
Рис. 5. Время удерживания – параметр удерживания, используемый для проведения качественного анализа в колоночной хроматографии [Кристиан Г. Аналитическая химия: в 2 т. – Т. 2 – М.: БИНОМ. Лаборатория знаний, 2009. – 504 с. – Рис.19.3, С. 139.]
Параметр «время удерживания» используют для идентификации химической природы компонента. Оказывается, если проводить измерения в одних и тех же условиях, то всегда можно зафиксировать сигнал одного и того же компонента в пробе вещества через одно и тоже время после ввода пробы в хроматограф.
