
- •Задачи и вопросы по неорганической химии
- •Издательство тпу
- •Кафедра
- •Введение
- •Общие закономерности неорганической химии
- •1.1. Распространенность химических элементов
- •1.2. Закономерности изменения свойств элементов и соединений в периодической системе
- •1.3. Общие закономерности окислительно-восстановительных реакций
- •1.4. Общие закономерности гидролиза
- •1.5. Взаимодействие металлов и неметаллов с кислотами, щелочами, водой
- •Водород и галогены
- •2.1. Водород и его соединения
- •2.2. Фтор и его соединения
- •2.3. Хлор, бром, иод - элементы, простые вещества и межгалогенные соединения
- •2.4. Галогеноводородные соединения и галогениды
- •2.5. Кислородосодержащие соединения галогенов
- •3.1. Кислород, воздух, озон
- •3.2. Бинарные соединения кислорода
- •3.3. Сера и её бинарные бескислородные соединения
- •3.4. Кислородосодержащие соединения серы
- •3.5. Селен, теллур, полоний
- •Глава четвертая. Главная подгруппа пятой группы
- •4.1. Азот и его водородосодержащие соединения
- •4.2. Соединения азота с кислородом и галогенами
- •4.3. Фосфор и его соединения
- •1) Р(бел) ® р(кр) 2) р(кр) ® р(чер) 3) р(бел) ® р(черн)
- •4.4. Мышьяк, сурьма, висмут
- •Главная подгруппа четвертой группы
- •5.1. Углерод и соединения углерода
- •5.3. Германий, олово, свинец
- •Главная подгуппа третьей группы
- •6.1. Бор и его соединения
- •6.2. Алюминий и его соединения
- •6.3. Галлий, индий, таллий
- •Химия s-элементов
- •7.1. Щелочные элементы
- •Переходные элементы
- •8.1. Общие закономерности
- •8.2. Подгруппа скандия
- •8.3. Подгруппа титана
- •8.4. Подгруппа ванадия
- •8.5. Подгруппа хрома
- •8.6. Подгруппа марганца
- •8.7. Железо, кобальт, никель
- •8.8. Платиновые элементы
- •8.9. Подгруппа меди
- •8.10. Подгруппа цинка
- •8.11. Лантаноиды и актиноиды
- •Ответы к расчётным задачам и рекомендации по выполнению заданий
- •Общие закономерности неорганической химии
- •Индивидуальное домашнее задание Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Вариант 31
- •Вариант 32
- •Вариант 33
- •Вариант 34
- •Вариант 35
- •Вариант 36
- •Вариант 37
- •Вариант 38
- •Вариант 39
- •Вариант 40
- •Вариант 41
- •Вариант 42
- •Вариант 43
- •Вариант 44
- •Вариант 45
- •Вариант 46
- •Вариант 47
- •Вариант 48
- •Вариант 49
- •Вариант 50
- •Вариант 51
- •Вариант 52
- •Вариант 53
- •Вариант 54
- •Вариант 55
- •Вариант 56
- •Вариант 57
- •Вариант 58
- •Вариант 59
- •Вариант 60
- •Вариант 61
- •Вариант 62
- •Вариант 63
- •Вариант 64
- •Вариант 65
- •Вариант 66
- •Вариант 67
- •Вариант 68
- •Вариант 69
- •Вариант 70
- •Вариант 71
- •Вариант 72
- •Вариант 73
- •Вариант 74
- •Вариант 75
- •Вариант 76
- •Вариант 77
- •Вариант 78
- •Вариант 79
- •Вариант 80
- •Вариант 81
- •Вариант 82
- •Вариант 83
- •Вариант 84
- •Вариант 85
- •Вариант 86
- •Вариант 87
- •Вариант 88
- •Вариант 89
- •Вариант 90
- •Вариант 91
- •Вариант 92
- •Вариант 93
- •Вариант 94
- •Вариант 95
- •Вариант 96
- •Вариант 97
- •Вариант 98
- •Вариант 99
- •Вариант 100
- •Вариант 101
- •Вариант 102
- •Вариант 103
- •Вариант 104
- •Вариант 105
- •Вариант 106
- •Вариант 107
- •Вариант 108
- •Вариант 109
- •Вариант 110
- •Вариант 111
- •Вариант 112
- •Вариант 113
- •Вариант 114
- •Вариант 115
- •Вариант 116
- •Вариант 117
- •Вариант 118
- •Вариант 119
- •Вариант 120
- •Вариант 121
- •Вариант 122
- •Вариант 123
- •Вариант 124
- •Вариант 125
- •Вариант 126
- •Вариант 127
- •Вариант 128
- •Вариант 129
- •Вариант 130
- •Вариант 131
- •Вариант 132
- •Вариант 133
- •Вариант 134
- •Вариант 135
- •Вариант 136
- •Вариант 137
- •Вариант 138
- •Вариант 139
- •Вариант 140
- •Вариант 141
- •Вариант 142
- •Вариант 143
- •Вариант 144
- •Вариант 145
- •Вариант 146
- •Вариант 147
- •Вариант 148
- •Вариант 149
- •Вариант 150
- •Задачи и вопросы по неорганической химии
2.5. Кислородосодержащие соединения галогенов
253. Объясните существование оксидов хлора, брома и иода в нечетных степенях окисления галогенов. То же самое выполните для оксидов, содержащих галогены в четных степенях окисления. Почему оксид ClO3 образует димеры Cl2O6, а оксид ClO2 димеров не образует? Относятся ли оксиды галогенов к термодинамически устойчивым соединениям?
254. Установите формулу вещества (плотность которого по водороду равна 43,5), содержащего 81,6 % хлора и 18,4 % кислорода. Опишите свойства этого вещества, его получение и применение. Выполните такое же задание для соединения, содержащего 47,42 % кислорода (остальное хлор), плотность которого в газообразном состоянии по водороду равна 33,73.
255. Напишите молекулярные и структурные формулы следующих соединений: а) хлорная кислота, б) хлористая кислота, в) гипохлорит кальция, г) хлорат калия, д) перхлорат магния. Каковы тривиальные названия двух последних веществ и с чем эти названия связаны?
256. Напишите формулы всех оксидов хлора, брома, иода и соответствующих им кислот. Как называются эти кислоты и как называются их соли? Какие кислоты и соли имеют наибольшее практическое значение?
257. Напишите формулы и названия всех оксокислот хлора и их солей. Какая из кислот существует в очень разбавленных растворах, какая - в разбавленных, какая - до 40 %-й концентрации и какая - в растворе любой концентрации и в свободном состоянии? Почему соли этих кислот более устойчивы, чем сами кислоты?
258.
Опишите химическую связь и строение
ионов ClO-,
ClO![]() ,
ClO
,
ClO![]() ,
ClO
,
ClO![]() .
Сделайте вывод об их устойчивости и
окислительных свойствах. Как и
почему изменяются эти свойства ионов
в составе кислот и в составе солей?
.
Сделайте вывод об их устойчивости и
окислительных свойствах. Как и
почему изменяются эти свойства ионов
в составе кислот и в составе солей?
259. Как взаимодействуют с водой и щелочами оксиды Cl2O, ClO2, Cl2O6, Cl2O7, I2O5? Напишите уравнения реакций и названия их продуктов.
260. Приведите справочные данные, свидетельствующие о том, что сила кислот в ряду HClO - HClO2 - HClO3 - HClO4 увеличивается, а окислительная способность уменьшается. Объясните эти закономерности.
261. Приведите данные о том, что сила и окислительные свойства кислот в ряду HClO - HВrО - HIO уменьшаются. Объясните эту закономерность.
262. Определите pH децимолярных растворов HCl, HClO, HClO2, HClO3 и HClO4. Почему для пяти данных кислот достаточно провести только три расчета?
263. При каких условиях происходит распад хлорноватистой кислоты соответственно следующим схемам:
1) HClO ® HCl + O2; 2) HClO ® Cl2O + H2O; 3)HClO ® HCl + HClO3?
Определите стехиометрические коэффициенты и тип каждой реакции. Какое из уравнений объясняет дезинфицирующее и отбеливающее свойства этой кислоты?
264. Напишите уравнение взаимодействия хлора с холодным раствором гидроксида калия. Укажите тип реакции и названия продуктов. Вычислите массы хлора и KOH, теоретически необходимые для получения 100 кг гипохлорита калия. Какая часть хлора и KOH расходуется на образование KClO, а какая часть - на образование хлорида калия?
265. Через холодный раствор гидроксида калия пропустили 280 л хлора (н.у.), который на 80 % провзаимодействовал с KOH. Какие массы KCl и KСlO образовались в результате реакции? Какой объем хлора пошел на образование хлорида калия и какой - на образование гипохлорита калия?
266. Опишите состав и строение, получение и применение хлорной извести, определите коэффициенты в уравнениях реакций с её участием:
1) CaOCl2 + HCl = CaCl2 + Cl2 + H2O
2) CaOCl2 + CO2 + H2O = CaCO3 + CaCl2 + HClO
3) CaOCl2 + CO2 + H2O = CaCO3 + HClO3 + HCl
Какая из этих реакций объясняет резкий запах, дезинфицирующие и отбеливающие свойства хлорной извести?
267. На химический завод поступают карбонат кальция, хлорид натрия и вода, а выпускает завод хлорную известь, хлор и гидроксид натрия. Какие химические реакции проводятся в заводских цехах?
268. Для получения хлорной извести заготовили 100 кг гашеной извести. Какой объем хлора (н.у.) потребуется теоретически для превращения её в хлорную известь и какая масса хлорной извести будет получена?
269. При взаимодействии оксида хлора (IV) с водой образуются две кислоты. Напишите уравнение реакции, названия кислот, опишите их свойства. При каких условиях и на какие продукты эти кислоты разлагаются? Почему их соли более устойчивы к разложению?
270. Хлорноватую кислоту в лабораториях получают взаимодействием раствора хлората бария с разбавленной H2SO4. Вычислите объем 20%-й H2SO4 (r = 1,14), который необходимо прибавить к 500 г 20 %-го раствора Ba(ClO3)2. По результатам реакции найдите массу осадка BaSO4, массу раствора и массу HClO3 в чистом виде, массовую долю HClO3 в растворе.
271. В результате взаимодействия 100 г раствора хлорноватой кислоты с избытком соляной кислоты образовалось 15,9 л хлора (н.у.). Вычислите массовую долю HClO3 в растворе.
272. Хлорноватая кислота - сильный окислитель. По значениям стандартных окислительно-восстановительных потенциалов определите возможность ее восстановления до Cl–-ионов, Cl2, HClO и ClO2. Напишите уравнения её наиболее вероятных реакций с магнием и с серой.
273. Один из лабораторных методов получения хлората калия состоит в пропускании хлора через горячий раствор гидроксида калия. Какой объем хлора (н.у.) теоретически необходимо пропустить через 700 г 40 %-ного раствора KOH? Какая масса хлората калия будет получена? Как отделяют хлорат калия от хлорида калия, также образующегося в этом процессе?
274. Один из лабораторных методов получения хлората калия состоит в пропускании хлора через горячий раствор K2CO3. Какой объем хлора (н.у.) теоретически необходимо пропустить через 400 г 35 %-го раствора K2CO3? Какая масса KClO3 будет получена? Какой объем CO2 (н.у.) выделится и какой будет масса побочного продукта - хлорида калия?
275. В промышленности используется известковый метод получения хлората калия, схему которого можно записать так:
CaCO3 ® CaO ® Ca(OH)2 ® Ca(ClO3)2 ® KClO3
Напишите уравнения реакций для каждой стадии, укажите условия их проведения.
276. В промышленности используется известковый метод получения хлората калия, по которому известковое молоко - Ca(OH)2 сначала хлорируют, а затем прибавляют KCl для перевода хлората кальция в хлорат калия. Вычислите расход негашеной извести, хлора и хлорида калия на получение одной тонны KClO3, выход которого составляет 80 %.
277. При действии на кристаллический хлорат калия концентрированной серной кислоты он взаимодействует с ней с образованием хлора и диоксида хлора. Какие другие продукты образуются в этой реакции? Напишите её уравнение, определите её тип.
278. При действии на 59 г бертолетовой соли избытка концентрированной соляной кислоты выделился газ желто-зеленого цвета. Какой это газ и чему равен его объем после приведения к нормальным условиям?
279. Какими уравнениями описывается разложение бертолетовой соли при 400 ºС, при 550–600 ºС и при 200–250 ºС в присутствии катализатора? Какой максимальный объем кислорода, приведенный к н.у., можно получить при полном разложении одного килограмма этого вещества?
280. Какую массу бертолетовой соли, содержащей 2 % KCl, необходимо нагреть для того, чтобы выделившемся кислородом заполнить газометр емкостью 20 л, в котором кислород находится при 20 ºС и 105 кПа?
281. Хлораты калия и натрия используются в качестве окислителей при сплавлении с твердыми веществами, например:
![]()
Задание: а) объясните высокую окислительную активность KClO3 при сплавлении; б) определите стехиометрические коэффициенты; в) вычислите массы KClO3 и KOH, необходимые для окисления 1 кг Cr2O3; д) какой массой хлората натрия NaClO3 можно заменить хлорат калия в этой реакции?
282. Бертолетова соль используется в качестве окислителя при вскрытии минералов. Напишите уравнение реакции, проходящей при сплавлении хлората калия с пиролюзитом в присутствии KOH, в которой образуется K2MnO4. Объясните высокую окислительную активность KClO3 при сплавлении, определите стехиометрические коэффициенты, вычислите массы KClO3 и KOH, необходимые для окисления 1 кг MnO2.
283. Бертолетова соль взаимодействует с красным фосфором по схеме:
KClO3(к) + P(красный) ® KCl(к) + P2O5(к)
Определите стехиометрические коэффициенты и вычислите энтальпию реакции. Объясните причины взрыва, который происходит при растирании или при ударе смеси бертолетовой соли с фосфором.
284. Смесь хлората калия с сахаром вспыхивает от капли концентрированной серной кислоты. Объясните этот процесс, напишите уравнения реакций этого стадийного процесса.
285. Напишите уравнения реакций в подкисленном растворе с участием хлората калия:
|
1) KClO3 + HCl =
2) KClO3 + KI + H2SO4 = |
3) KClO3 + NaNO2 + H2SO4 =
4) KClO3 + FeSO4 + H2SO4= |
286. При взаимодействии хлората калия с аммиаком в щелочной среде хлорат калия восстанавливается максимально, а аммиак окисляется максимально. Какой объем газообразного аммиака, взятого при н.у., взаимодействует с 1 моль KClO3?
287. В лаборатории имеются кристаллический иод, серная кислота, хлорид натрия, диоксид марганца и вода. Как получить из этих веществ иодноватую кислоту? Напишите уравнения реакций. Вычислите объем 35%-й HIO3 (r = 1,19), получаемой из 20 г иода.
288. Исходя из полуреакций
IO![]() + 6H+
+ 6e = I–
+ 3H2O; jº
= 1,08 В
+ 6H+
+ 6e = I–
+ 3H2O; jº
= 1,08 В
IO![]() + 6H+
+ 5e = 1/2I2
+ 3H2O; j0º
= 1,19 В
+ 6H+
+ 5e = 1/2I2
+ 3H2O; j0º
= 1,19 В
IO![]() + 5H+
+ 4e
=
HIO + 2H2O; jº
= 1,14 В
+ 5H+
+ 4e
=
HIO + 2H2O; jº
= 1,14 В
SO![]() + 4H+
+ 2e
=
H2SO4
+ H2O; jº
= 0,17 В
+ 4H+
+ 2e
=
H2SO4
+ H2O; jº
= 0,17 В
определите наиболее вероятный продукт восстановления иодат-ионов сернистой кислотой в кислой среде и напишите уравнение реакции.
289. Какой объем 5%-го раствора HIO3 (r = 1,02) требуется для окисления 40 мл 8%-го раствора HI (r = 1,06) и какая масса иода образуется при этом?
290. Раствор KIO3 с плотностью 1,072 объемом 20 мл провзаимодействовал с избытком иодида калия в присутствии серной кислоты. Образовалось 4,634 г иода. Вычислите массовую долю KIO3 в растворе.
291. Опытные данные свидетельствуют о том, что в окислительно-восстановительных реакциях хлораты восстанавливаются почти всегда до хлоридов, иодиды - до иода, а броматы - до бромидов или до брома в зависимости от того, с какими восстановителями они взаимодействуют. Объясните эти опытные данные.
292. Какой объем 6%-го раствора KBrO3 (r = 1,04) потребуется для окисления в сернокислом растворе 100 мл 0,5 М раствора FeSO4, если восстановление бромата калия происходит до бромида?
293. При нагревании гипобромита натрия образуется бромид и бромат натрия. Напишите уравнение реакции, определите ее тип.
294. Взаимодействие бромида калия с хлоратом калия в кислой среде можно выразить схемой, включающей несколько параллельных реакций:
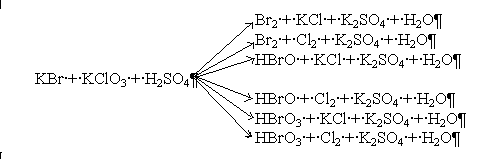
Используя значения jº, определите наиболее вероятные продукты реакции и стехиометрические коэффициенты в её уравнении.
295. При пропускании хлора через раствор иодида калия раствор сначала желтеет, а потом обесцвечивается. Напишите уравнения реакций.
296. Почему хлорную кислоту считают самой сильной кислотой? Почему константа и степень её диссоциации в справочниках отсутствуют? Напишите формулу этой кислоты, объясните химическую связь в молекуле и её строение. Как получают эту кислоту? Как называются ее соли?
297. Какая из оксокислот хлора в безводном состоянии взрывается при 92 ºС, воспламеняет бумагу, дерево, уголь? Что представляет собой бесцветная маслянистая жидкость, образующаяся при взаимодействии этой кислоты с фосфорным ангидридом?
298. По значениям окислительно-восстановительных потенциалов определите возможность восстановления при стандартных условиях хлорной кислоты до HCl, Cl2, HClO3. При взаимодействии хлорной кислоты с иодом выделяется хлор и образуется метаиодная кислота, которая при хранении самопроизвольно превращается в ортоиодную. Напишите уравнения соответствующих реакций.
299. В одном литре раствора содержится 10,05 г хлорной кислоты. Определите молярную концентрацию и молярную концентрацию эквивалента HClO4 как окислителя в реакции: HClO4 + SO4 + H2O ® HCl + H2SO4
300. Напишите уравнения реакций с участием хлорной кислоты и определите в них стехиометрические коэффициенты:
|
1) HClO4 + H2SO3 = |
2) HClO4 + C = |
3) HClO4 + Mg = |
301. Принято считать, что существование соединений INO3, I(NO3)3, I2SO4, I(CH3COO) и I(CH3COO)3, получаемых в неводных растворителях, свидетельствует о металлических свойствах иода. В чем состоит сходство этих соединений с солями металлов и чем они отличаются от солей?
302. Объясните, как и почему изменяется гидролизуемость солей в рядах NaClO - NaClO2 - NaClO3 - NaClO4 и NaClO - NaBrO - NaIO. Для тех солей, которые подвергаются гидролизу, напишите уравнения реакций гидролиза в молекулярном и ионном виде.
303. Вычислите константу гидролиза гипохлорит-иона. Чему равна его степень гидролиза в децимолярном растворе? Добавлением каких веществ можно уменьшить гидролиз гипохлорита калия?
304. Выпадет ли осадок хлората серебра, (произведение растворимости равно 5∙10-2), если смешать одинаковые объемы растворов AgNO3 и KClO3, молярные концентрации которых в растворах равны 0,1 М?
305. Напишите уравнения реакций для осуществления следующей цепочки превращений:
NaCl ® HCl ® Cl2 ® NaClO ® NaClO3 ® HClO3 ® HClO4 ® Cl2 ® HCl ® NaCl
306. Задание в № 303:
NaCl ® HCl ® Cl2 ® KClO3 ® ClO2 ® KClO2 ® HClO2 ® HCl ® Cl2 ® NaCl
307. Задание в № 303:
NaCl ® HCl ® Cl2 ® Ba(ClO)2 ® Ba(ClO3)2 ® HClO3 ® HClO4 ® Cl2 ® HCl ® NaCl
308. Задание в № 303:
NaBr ® HBr ® КBr ® Br2 ® Ba(BrO3)2 ® HBrO3 ® Br2
309. Задание в № 303:
NaI ® I2 ® HI ® HIO3 ® I2O5 ® I2
310. Природное соединение хлорид натрия фактически является исходным веществом для получения всех соединений хлора. Покажите в виде наглядной схемы получение из хлорида натрия следующих соединений: HCl, HClO3, HClO4, KClO, KClO3 и CaOCl2. Укажите названия этих соединений.
Глава третья. ХАЛЬКОГЕНЫ
Кислород, воздух, озон. Бинарные соединения кислорода. Сера и её бинарные бескислородные соединения. Кислородосодержащие соединения серы. Селен, теллур, полоний.
