
- •Введение
- •Глава 1. Основные положения координационной теории
- •1.1. Определение комплексных соединений
- •1.2. Основные понятия
- •1.3. Номенклатура комплексных соединений
- •1.4. Классификация комплексных соединений
- •1.5. Изомерия комплексных соединений
- •Глава 2. Природа химической связи в комплексных соединениях
- •2.1. Электростатическая теория
- •2.2. Метод валентных связей
- •2.3. Теория кристаллического поля
- •2.4. Теория поля лигандов
- •Глава 3. Свойства комплексных соединений
- •3.1. Окраска комплексных соединений
- •Периода в водном растворе
- •3.2. Магнитные свойства комплексных соединений
- •3.3. Равновесия в растворах комплексных соединений
- •3.4. Устойчивость комплексных соединений
- •3.4.1. Природа центрального атома и лигандов
- •3.4.2. Хелатный эффект
- •3.4.3. Стерические факторы
- •3.5. Кинетика и механизм реакций обмена лигандов
- •3.6. Кислотно - основные свойства комплексных соединений
- •3.7. Окислительно-восстановительные свойства комплексных соединений
- •Глава 4. Координационные соединения металлов
- •4.1. Подгруппа железа
- •4.1.1. Железо
- •4.1.2. Кобальт
- •4.1.3. Никель
- •В комплексных соединениях металлов подгруппы железа
- •4.2. Платиновые металлы
- •В комплексных соединениях платиновых металлов
- •4.3. Подгруппа марганца
- •В комплексных соединениях металлов подгруппы марганца
- •4.4. Подгруппа хрома
- •Комплексных соединениях металлов подгруппы хрома
- •4.5. Подгруппа ванадия
- •В комплексных соединениях металлов подгруппы ванадия
- •4.6. Подгруппа титана
- •В комплексных соединениях металлов подгруппы титана
- •4.7. Подгруппа цинка
- •В комплексных соединениях металлов подгруппы цинка
- •4.8. Подгруппа меди
- •В комплексных соединениях металлов подгруппы меди
- •4.9. Подгруппа алюминия
- •4.10. Комплексные соединения s-элементов
- •Катионов подгрупп iАи iiа при 25оС
- •Глава 5. Координационные соединения и медицина
- •5.1.Основные биолиганды
- •5.2. Некоторые основные биометаллы
- •5.3. Избыток и недостаток металлов-микроэлементов
- •5.4. Хелатотерапия
- •5.5. Лекарственные препараты в качестве лигандов
- •5.6. Координационные соединения металлов как противоопухолевые средства
- •Приложение
- •Им окраски
- •Литература
- •Оглавление
- •Глава1.
- •Глава2.
- •Глава3.
- •Глава 4
- •Глава5. Координационные соединения
- •Учебное пособие
- •117997, Москва, ул. Островитянова, д.1.
5.4. Хелатотерапия
Ионы металлов, имеющие биологическое значение (Na+,K+,Fe3+,Fe2+,Cu2+,Zn2+ и др.), являются, в основном, жёсткими кислотами Льюиса или примыкают к жёстким. Важнейшие компоненты клетки и те группы в них, которые выступают как потенциально связывающие группы, относятся к жёстким основаниям. Таким образом, живая система является жёсткой. Наоборот, токсичные ионы металлов окружающей среды чаще всего являются ионами мягких тяжёлых металлов и металлоидов, играющих весьма скромные биологические роли. Попадание их в организм зачастую грозит серьёзными неприятностями, так как они очень прочно связываются с биологическими макромолекулами. Среди токсичных веществ можно отметить соединения мышьяка, кадмия, ртути и свинца. Хотя ион цинка является одним из важнейших биометаллов, слишком высокое содержание его в тканях оказывает канцерогенное действие. Ионы мягких металлов способны образовывать прочные связи с различными биологически активными центрами, предпочтительно с серосодержащими лигандами. Часто они вытесняют естественные ионы и ингибируют металлоферменты.
Большинство способов лечения отравлений металлами подразумевает использование хелатирующих агентов с целью образования и быстрого выведения растворимых и нетоксичных комплексов. Хелатирующий агент металла должен достаточно прочно связывать металл, чтобы конкурировать с биологическими лигандами, и обладать селективностью. В случае недостаточной селективности или её отсутствия могут быть вредные побочные эффекты, заключающиеся в выведении других металлов, в частности, кальция и цинка. Кроме того, лиганд сам по себе не должен быть токсичным.
Для
лечения отравления люизитом ClCH=CHAsCl2
во время первой мировой войны был создан
лиганд БАЛ (британский антилюизит)
(рис.49).  Действие
люизита основывается на связывании
–SH-
групп ферментов, но БАЛ ещё прочнее
связывает мышьяк и поэтому может
выводить его.
Действие
люизита основывается на связывании
–SH-
групп ферментов, но БАЛ ещё прочнее
связывает мышьяк и поэтому может
выводить его.
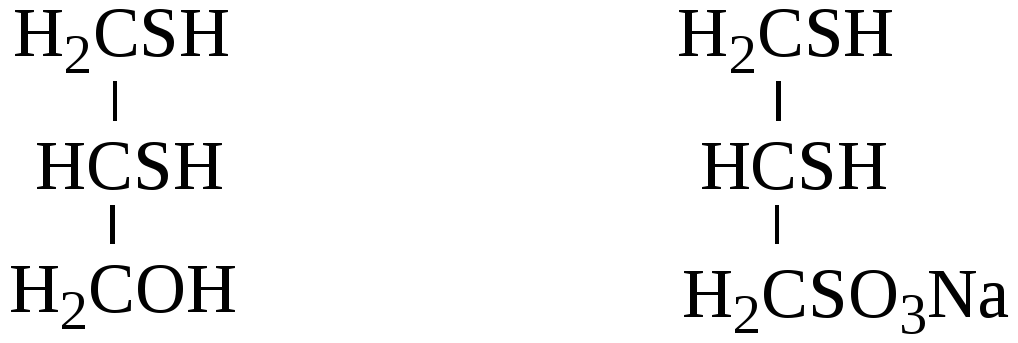
а) б)
Рис.49. БАЛ (а) и «унитиол» (б).
В нашей стране используется похожий препарат «унитиол»(рис.49).«Унитиол» является хорошо растворимой солью и с успехом применяется при отравлениях мышьяком, ртутью, кадмием, титаном, таллием, висмутом и другими металлами, относящимися к так называемым тиоловым ядам, т.е. веществам, способным вступать во взаимодействие с сульфгидрильными (тиоловыми) группами ферментных белков. Например, с кадмием «унитиол» образует комплекс, в котором у кадмия реализуется координационное число 4:
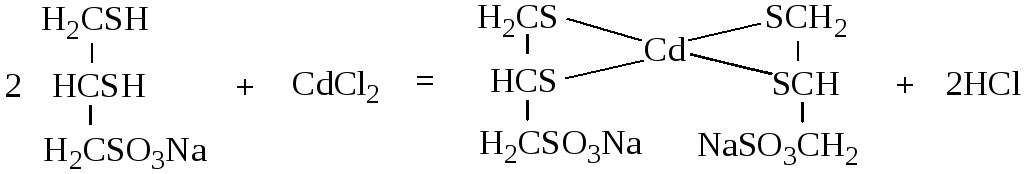
БАЛ и унитиол применяются также и при лечении гепатоцеребральной дистрофии, связанной с нарушением обмена меди в организме. Сравнительно с БАЛ унитиол менее токсичен, лучше растворим в воде, что создаёт большие удобства для применения и обеспечивает более быстрое всасывание.
При лечении отравлений металлами, в особенности, свинцом, широко используется ЭДТА- этилендиаминтетрауксусную кислоту, чаще всего в виде натриевой соли Na2ЭДТА (рис.50):

Рис.50. Na2ЭДТА.
Соли ЭДТА-комплексонаты образуются за счёт взаимодействия ионов металлов и протонов СООН-групп, а также за счёт донорно-акцепторного взаимодействия азота комплексона и ионов металлов. Комплексонаты в большинстве своём хорошо растворимы в воде и характеризуются большими константами устойчивости. Высокая устойчивость комплексонатов объясняется тем, что при их образовании замыкаются два, три или более хелатных цикла, как, например, в случае комплекса меди (рис.51):
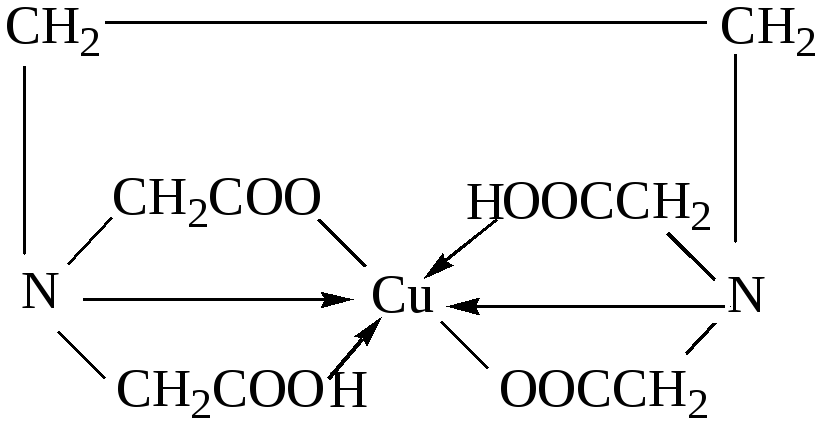
Рис.51. Комплексонат меди.
Динатриевая соль ЭДТА (трилон Б) способна образовывать комплексонаты с различными металлами, в том числе с ионом кальция. Это даёт возможность применять её при заболеваниях, связанных с избыточным отложением солей кальция (мочекаменная болезнь, катаракта).
При острых и хронических отравлениях тяжёлыми и редкоземельными металлами и их соединениями (свинцом, кадмием, ртутью, кобальтом, ураном, иттрием, церием и др.) используют тетацин-кальций (кальций динатриевую соль этилендиамино-
тетрауксусной кислоты), которую используют для предотвращения вымывания кальция из скелета. Комплексонат кальция образует более прочные комплексы с ионами этих металлов, чем комплексы этих ионов с серосодержащими группами белков, ферментов. Ионы этих элементов вытесняют кальций, так как образуют более прочные связи с кислородом и азотом комплексона, чем кальций:
Hg2+ + [CaЭДТА] = Ca2+ + [HgЭДТА].
Высокую комплексообразующую активность в отношении ионов металлов (главным образом, меди, ртути, свинца и железа) проявляет пеницилламин (D-3,3-диметилцистеин):
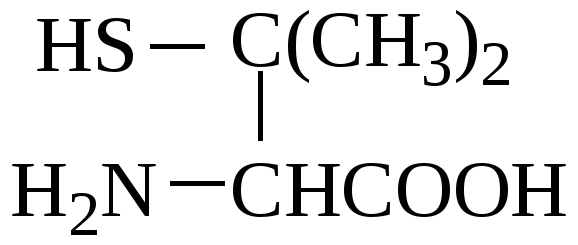
Образующиеся комплексы растворимы в воде и выводятся почками. Пеницилламин особенно эффективно удаляет избыток ионов меди - более эффективно, чем унитиол. Пеницилламин широко используют при лечении заболеваний, связанных с увеличением концентрации меди в организме, в частности, болезни Вильсона, при которой содержание меди увеличивается в 100 раз по сравнению с нормой.
Некоторые криптанды демонстрируют исключительно высокую селективность к определённым катионам. Так, криптанд:
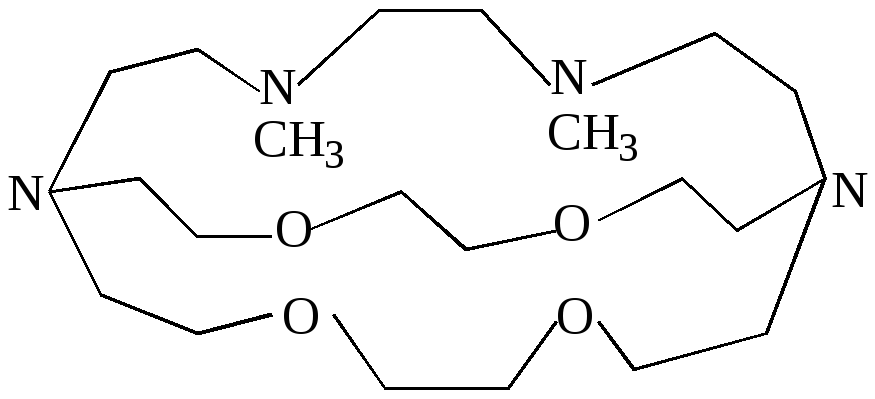
способен в присутствии Zn2+и Ca2+ с очень высокой селективностью(~106) связывать Cd2+ . Этот криптанд эффективно удаляет также свинец, радионуклиды стронция и радия.
При остром отравлении препаратами железа, гемохроматозе и гемосидерозе используют дефероксамин:
(N-[5-{-[(5-аминопентил)оксикарбамоил]пропионамидо}пентил]-3-{N-оксиацетамидо)пентил]карбамоил}–пропионгидроксамовая кислота) N, который образует комплексное соединение с железом (рис.52).
Дефероксамин способствует удалению железа из железосодержащих белков (ферритина и гемосидерина), но не из гемоглобина и железосодержащих ферментов.

Рис.52. Комплекс железа с дефероксамином.
