
- •Башкирский государственный аграрный университет
- •Р.И. Галеева, е.В. Тальвинский, и.А. Сагитдинов
- •Практикум
- •По органической химии
- •Оглавление
- •Введение
- •Методика тушения некоторых видов пожаров в химических лабораториях
- •1 Предельные и непредельные углеводороды Алканы
- •Вопросы для контроля
- •Упражнения по теме «Алканы»
- •Вопросы для контроля
- •Упражнения по теме «Алкены»
- •Опыт 1.4 Получение этина и изучение его свойств
- •Вопросы для контроля
- •Упражнения по теме «Алкины»
- •2 Ароматические углеводороды Арены
- •Лабораторная работа
- •Опыт 2.1 Растворимость бензола в воде
- •Опыт 2.2 Окисление боковых цепей гомологов бензола
- •Вопросы для контроля
- •Упражнения по теме «Ароматические углеводороды»
- •3 ГалогенОпроизводные углеводородов
- •Лабораторная работа
- •Опыт 3.1 Получение хлорэтана из этанола
- •Опыт 3.2 Получение хлороформа из хлоральгидрата
- •Опыт 3.3 Получение иодоформа из этанола
- •И в боковой цепи
- •Вопросы для контроля
- •Упражнения по теме «Галогенопроизводные углеводородов»
- •4 Спирты
- •Лабораторная работа
- •Опыт 4.1 Получение этилата натрия
- •Опыт 4.2 Реакция глицерина с гидратом окиси меди в щелочной среде
- •Опыт 4.4 Получение диэтилового эфира
- •Опыт 4.5 Получение этилового эфира этановой кислоты
- •Вопросы для контроля
- •Упражнения по теме «Спирты»
- •5 Фенолы
- •Опыт 5.3 Образование трибромфенола
- •Опыт 5.4 Доказательство кислотного характера фенола
- •Опыт 5.5 Цветные реакции фенолов с хлорным железом
- •Вопросы для контроля
- •Упражнения по теме: «Фенолы»
- •6 Оксосоединения Альдегиды и кетоны
- •Лабораторная работа
- •Опыт 6.1 Окисление метаналя аммиачным раствором окиси
- •Опыт 6.3 Получение ацетона из ацетата натрия
- •Опыт 6.4 Открытие пропанона в виде 2,4-динитрофенилгидрозона
- •Вопросы для контроля
- •Упражнения по теме «Альдегиды и кетоны»
- •7 Карбоновые кислоты и их производные
- •Лабораторная работа №
- •Опыт 7.2 Окисление муравьиной кислоты марганцевокислым калием
- •Опыт 7.4 Получение натриевой соли щавелевой кислоты
- •Образование биурета и циануровой кислоты
- •Вопросы для контроля
- •Упражнения по теме: «Карбоновые кислоты и их производные»
- •8 Амины
- •Лабораторная работа
- •Опыт 8.1 Реакция первичного амина с азотистой кислотой (пример дезаминирования)
- •Вопросы для контроля
- •Упражнения по теме: «Амины»
- •9 Оксикислоты
- •Виннокаменной кислоте.
- •Вопросы для контроля
- •Упражнения по теме «Оксикислоты»
- •10 Углеводы
- •Моносахариды
- •Лабораторная работа
- •В присутствии щелочи
- •Вопросы для контроля
- •Упражнения по теме «Простые сахара»
- •Дисахариды и полисахариды
- •Лабораторная работа
- •(Тростниковом сахаре)
- •Вопросы для контроля.
- •Упражнения по теме «Дисахариды и полисахариды»
- •11 Аминокислоты, белки
- •Лабораторная работа
- •Принцип формольного титрования
- •(Цистин, цистеин)
- •Вопросы для контроля
- •Упражнения по теме «Аминокислоты. Белки»
- •12 Гетероциклические соединения
- •Лабораторная работа
- •С хлоридом железа (III)
- •Натриевой соли в воде
- •(Выделение кристаллической мочевой кислоты)
- •Вопросы для контроля
- •Упражнения по теме «Гетероциклические соединения»
И в боковой цепи
а). Помещают в пробирку 1 каплю хлорбензола (С6H5Cl) и 5 капель воды. Содержимое пробирки нагревают до кипения и к горячему раствору прибавляют 1 каплю 0,2н AgNO3. Что при этом наблюдается?
б) Помещают в пробирку 1 каплю хлористого бензила (С6H5СН2Cl) и 5 капель воды. Содержимое пробирки нагревают до кипения и к горячему раствору прибавляют 1 каплю 0,2н AgNO3. Что при этом происходит? Описать в журнале.
Вопросы для контроля
-
Изомерия и номенклатура галогенпроизводных углеводородов.
-
Полярность связи углерод – галоген, индуктивный эффект.
-
Реакция нуклеофильного замещения. Механизм реакции.
-
Сравнительная подвижность атома галогена в зависимости от типа радикала.
-
Методы получения галогенопроизводных углеводородов.
Упражнения по теме «Галогенопроизводные углеводородов»
1. Напишите структурные формулы всех галогенозамещенных с формулой С5Н11Cl. Назовите эти соединения по номенклатуре ИЮПАК.
2. Напишите уравнения реакций взаимодействия 2-бромбутана со следующими соединениями:
а) магнием; б) аммиаком;
в) цианистым калием; в) водным и спиртовым раствором щелочи.
3. Из пропина получите 1-хлорпропен-2.
4. Из этина получите 2-хлорбутадиен-1,3-хлоропрен.
5. Из метана получите этановую кислоту, используя реактив Гриньяра.
6. Получите хлорэтен (CH2 = CH – Cl), исходя из этена и этина.
7. Из бензола получите 2,4-динитрохлорбензол и 2,5-дихлорнитробензол.
8. Напишите схемы реакций полимеризации:
а) хлористого винила; б) 2-хлор-1,3-бутадиена.
9. Из этаналя получите бромоформ (CHBr3).
10. Напишите схему следующих превращений:
СН3 – СН2 – СН2 –
СН3![]() А
А![]() Б
Б![]() В
В![]() Г
Г![]()
Назовите соединения А, Б, В, Г, Д.
11. Из этана получите хлорэтен (CH2 = CH – Cl).
12. Из дибромэтана получите 1,2-дибромбензол.
13. Из этина получите 1-бром-4-хлорбензол.
14. Как осуществить следующие превращения:





 СН3
– С СН
СН3
– С СН
СН3 – СН = СН2
СН3-СН2 – СН2 - Br СН3 – (СН2)4 – СН3
СН3 – СН2 – СН2 – СН3
СН3 – СН2 – СН3
1 5.
С помощью каких реакций можно различить
изомерные соединения:
5.
С помощью каких реакций можно различить
изомерные соединения:
n-хлортолуол и хлористый бензил?
4 Спирты
Спирты или алкоголи-производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на соответствующее число гидроксильных групп.
Химические свойства спиртов определяются реакционноспособной гидроксильной группой и строением связанного с ней радикала.
Реакции, в которые вступают спирты, можно разбить на следующие группы:
I. Реакции идущие с участием только атома водорода гидроксильной группы (разрыв связи О – Н).
II. Реакции, происходящие с замещением или отщеплением всей гидроксильной группы (разрыв связи С – О)
III Реакции окисления, в которых одновременно принимают участие гидроксильная группа, -водородные атомы или соседние связи углерод – углерод.
Спирты – практически нейтральные вещества. Однако, атом водорода гидроксильной группы, обладая некоторой подвижностью, способен вступать в реакции замещения.
Кислород как более электроотрицательный элемент, оттягивая электронную плотность в свою сторону, способствует поляризации связи О – Н:
- +
R – O H
В результате происходит замещение атома водорода на щелочные или, при соответствующих условиях, на другие металлы (Ca, Al, Mg).
По способности отщепления водорода спирты можно расположить в такой ряд: первичные вторичные третичные.
При окислении спиртов образуются различные продукты. Первичные спирты при этом переходят в альдегиды, а вторичные – в кетоны:
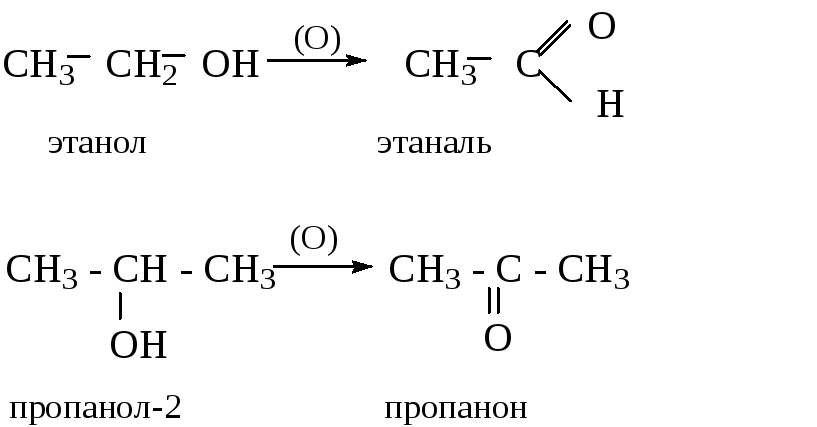
Третичные спирты наиболее стойки к действию окислителей. Поэтому при их окислении в жестких условиях происходит расщепление молекулы с образованием смеси кислот.
