
- •Введение
- •1.Охрана окружающей среды от вредных выбросов и способы их подавления
- •1.1 Характеристика выбросов от тэс и котельных и проблема охраны окружающей среды.
- •Обезвреживание вредных выбросов
- •Постановка задачи исследования
- •2. Основы рабочего процесса в противоточном полом скруббере-абсорбере
- •2.1 Процессы взаимодействия твердых частиц с каплями жидкости
- •2.2. Повышение степени очистки от диоксида серы при использовании щелочных свойств золы.
- •Процессы, происходящие в жидкой фазе.
2.2. Повышение степени очистки от диоксида серы при использовании щелочных свойств золы.
Для расчета абсорбции сернистого ангидрида из дымовых газов очень важным является определение основных физико-химических процессов, протекающих в системах МЗУ и ГЗУ. В работах /13, 21/ показано, что в настоящее время большое внимание разработчиков привлекают скрубберные способы очистки дымовых газов совместно от окислов серы и золы. Такие схемы обладают тем свойством, что не требуются значительные капитальные затраты на сооружение специальных узлов сероочистки, т.к. имеющееся оборудование при незначительной реконструкции позволяет решить, в большинстве случаев, поставленную задачу - соблюдение санитарных норм. Кроме того, особенности технологического процесса - сжигание топлива в топках паровых и водогрейных котлов - не позволяет применять традиционные способы извлечения серы из газа, т.к. концентрация двуокиси серы в газовой фазе не превышает 0,3-0,4% по объему /21, 22/.
Весьма перспективным является повышение реакционной способности поглотителя в орошающей воде путем увеличения щелочности раствора при использовании традиционной оборотной схемы. Исследования, проведенные в работах /13, 23/, показали, что одной из действенных мер
Совершенствования эффективности сероулавливания является повышение растворимости соединений кальция, входящих в состав зол, в присутствии CO2. Это достигается продувкой через емкость с пульпой некоторой части дымовых газов, содержащих в большинстве случаев около 8% CO2. Растворимость, например, известняка CaCO3 в присутствии CO2 резко повышается из-за образования легко растворимой углекислой соли Ca(HCO3)2:
CaCO3+ CO2+H2O→Ca(HCO3)2 (2.2.1)
На рис. 2.2.1 представлена схема золоуловителя с принудительной продувкой в контуре оборотного водоснабжения.
Поясним принцип формирования щелочных свойств золы, поступающей в полый скруббер.
РИСУНОК
При сжигании твердого топлива происходит термическая обработка материала, что сопровождается определенными физико-химическими процессами в его структуре.
Согласно дифференциально-термическому, химическому и рентгенографическому анализам ряда проб летучей золы различных топлив /21/ в ее состав входят такие соединения, как: CaO, SiO2, Al2O3, CaSO3, CaCO3 и некоторые другие. CaO является из основных компонентов золы (его содержание составляет 8-43% на бессульфатную массу). Часть окислов содержится в золе в связанном между собой состоянии, часть - в химически свободном. Свободная окись кальция образуется в топке в зоне высоких температур вследствие разложения карбоната и органических соединений кальция, содержащихся в топливе. Часть окиси кальция спекается с окислами кремния, железа и алюминия. Некоторая ее часть при снижении темперы газов до 800°С связывается с окислами серы, содержащимися в дымовых газах, образуя сульфит и сульфат кальция.
CaO+SO2→ CaSO3
CaO+SO3→ CaSO4 (2.2.2)
Оставшаяся часть окиси кальция остается свободной – CaOсв. С увеличением общего содержания окиси кальция в золе растет и содержание в ней CaOсв, причем быстрее, чем по линейному закону, т.к. при этом уменьшается содержание в золе SiO2, Al2O3 и, следовательно, уменьшается доля связанной с ними окиси кальция.
Процентное содержание свободной окиси кальция в летучей золе личных типов можно приближенно определить по полуэмпирической формуле CaOсв=0,0074 CaO2общ /21/, где CaOобщ – общее содержание CaO в золе топлива, определяется по табличным данным, %.
Наряду со свободной окисью, сульфитом и сульфатом кальция в золе присутствуют окислы и соли других щелочных металлов (например, K2O, Na2O и т.д.), но в меньших количествах, поэтому их влияние на процессы, протекающие в системе МЗУ проявляется в значительно меньшей степени.
Определение состава общей щелочности орошающей воды
Для расчета процессов абсорбции SO2 растворенными поглотителями большое значение имеет качественный состав исходной общей щелочности орошающей воды. Проведенный выше анализ показывает, что наиболее вероятными поглотителями являются соединения кальция, обуславливающие гидратную, карбонатную и бикарбонатную щелочности. Роль других поглотителей из-за малой их концентрации незначительна.
Согласно схеме (см. рис.2.2.1), можно выделить четыре способа подачи воды на орошение:
-
разомкнутая схема (подача технической воды);
-
традиционная оборотная схема (подача осветленной воды после золоотвала);
-
подача воды после бака-выщелачивателя;
-
совместная подача первых трех потоков воды.
При разомкнутой схеме водоснабжения, на орошение подается техническая вода. Как следует из опыта эксплуатации, концентрация щелочи в такой воде незначительна, до 2-2,5 мг-экв/л при рН< 7 /21/. Наличие такой щелочности, как правило, слабо влияет на хемобсорбцию, и процесс абсорбции двуокиси серы можно считать физическим. Таким образом, общая щелочность Щоб принимается равной нулю.
В тех случаях, когда рН менее 7 можно считать, что общая щелочность орошающей воды обусловлена исключительно присутствием гидроксид-ионов, т.е. Щоб= Щон-.
Следует заметить, что превышение рН более 7, в условиях, характерных для рассматриваемого случая, наблюдается очень редко /21/. Данное обстоятельство подтверждается тем, что вследствие незначительной, как правило, щелочности степень очистки от SO2 не превышает 3-5% /13,21/.
Опыт эксплуатации системы МЗУ при оборотном водоснабжении показывает, что в зависимости от наличия в золе свободной окиси кальция /21/, степень очистки может колебаться в достаточно широком диапазоне и в благоприятном случае достигать 25-30%. Так, например, при содержании CaOсв>20% (общая щелочность до 50 мг-экв/л (при рН до 12-13) в Канско-Ачинских углях и торфе, показатели степени очистки достигали данной величины, но при этом наблюдались интенсивные отложения в системах МЗУ и ГЗУ, что резко ухудшало условия работы аппарата. Для большинства сжигаемых углей общая щелочность, как правило, не превышала 10 мг-экв/л, при степени очистки порядка 5-10%.
Согласно данным /13, 21/ в случае традиционного оборотного водоснабжения компонентами общей щелочности будут гидратная и карбонатная. Возникновение гидратной щелочности в системе ГЗУ обусловлено взаимодействием свободной окиси кальция с водой:
CaOсв+H2O→Ca(OH)2 (2.2.3)
Наличие карбонатной щелочности обусловлено как содержанием карбоната кальция в уловленной золе, так и вследствие реакции
CaOсв+CO2→CaCH3 (2.2.4)
Составные части общей щелочности можно определить следующим
образом:
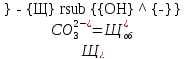 ,
(2.2.5)
,
(2.2.5)
где
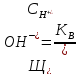 ; КВ
– ионное произведение воды;
; КВ
– ионное произведение воды;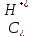 - концентрация ионов водорода, определяемая
из выражения
- концентрация ионов водорода, определяемая
из выражения
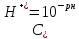 ;
;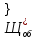 - задаваемая общая щелочность орошающей
воды.
- задаваемая общая щелочность орошающей
воды.
В третьем случае (после бака - выщелачивателя) определение составных частей общей щелочности можно осуществить, исходя из следующих соображений. Согласно исследованиям, приведенным в /13/, возникновение бикарбонатной щелочности определяется уравнением (2.2.1). При этом образование гидрокарбоната кальция Ca(HCO3)2 происходит за счет потребления карбоната кальция CaCO3, как из жидкой фазы, так и за счет улучшения растворимости его из золовых частиц в присутствии CO2. Это приводит к резкому уменьшению содержания карбонатной щелочности в воде. Поэтому, в дальнейшем карбонатной щелочностью можно пренебречь.
Следует заметить, что применение принудительного выщелачивателя является не только мерой повышения поглотительной способности раствора исключительно за счет использования щелочных свойств золы, но и эффективным средством предотвращения отложений карбоната кальция в системе оборотного водоснабжения.
Определение состава, общей щелочности производится аналогично предыдущему:
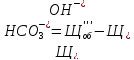 (2.2.6)
(2.2.6)
Для случая смешения потоков воды, подаваемой на орошение скруббера, общую щелочность следует определять по формуле:
Щоб=m’Щ’об+ m’’Щ’’об+ m’’’Щ’’’об, (2.2.7)
где m’ - массовая доля технической воды; m” – массовая доля потока воды осветленной после золоотвала; m”’ – массовая доля потока воды после бака-выщелачивателя.
Суммарный расход воды будет определен из соотношения:
m’+m”+m”’=1 (2,2.8)
