- •Механическое движение. Системы отсчета.
- •2. Основные кинематические характеристики.
- •3. Равномерное прямолинейное движение.
- •4. Равнопеременное движение.
- •6. Угловые скорость и ускорение и их связь с параметрами поступательного движения.
- •9. Равновесие твердого тела.
- •10. Работа и кинетическая энергия.
- •11. Законы сохранения в механике
- •12. Упругие силы.
- •17. Уравнение состояния идеального газа.
- •18. Теплота и работа.
- •19. Внутренняя энергия идеального газа.
- •20. Теплоемкость.
- •22. Работа при основных изопроцессах.
- •23. Фазовые переходы.
- •25. Взаимодействие зарядов. Закон Кулона.
- •27. Закон Гаусса.
- •29. Связь потенциала с напряженностью электрического поля.
- •33. Электрический ток в жидкостях. Закон электролиза фарадея.
- •35. Индукция и напряженность магнитного поля. Закон Био-Савара-Лапласа.
- •38. Магнитное поле в вещ-ве. Понятие о диа-, пара- и ферромагнетизме.
- •39. Электромгнитные колебания.
- •43. Интерференция монохроматических волн. Когерентность.
- •48. Атом водорода.
- •49. Волновая функция и ее смысл.
- •51. Зонная теория электропроводности.
- •53. Естественная радиоактивность. Закон радиоактивного распада.
- •Законы радиоактивного распада ядер
- •55. Тепловые машины.
- •56. Переменный ток.
20. Теплоемкость.
Удельная
теплоемкость — это количество теплоты,
необходимое для нагревания 1 кг вещества
на 1 К:
![]() .
Молярная
теплоемкость — количество теплоты,
необходимое для нагревания 1 моль
вещества на 1 К:
.
Молярная
теплоемкость — количество теплоты,
необходимое для нагревания 1 моль
вещества на 1 К:
![]() .
Удельная
и молярная теплоемкости связаны
соотношением:
.
Удельная
и молярная теплоемкости связаны
соотношением:
![]() ,
где
М — молярная масса (масса одного
моля вещества).
,
где
М — молярная масса (масса одного
моля вещества).
При
постоянном объеме работа газа равна
нулю (А=0) и все полученное тепло идет на
увеличение внутренней энергии газа
(![]() ).
Молярная
теплоемкость газа при постоянном
объеме:
).
Молярная
теплоемкость газа при постоянном
объеме: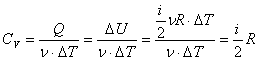 .
.
При
постоянном давлении тепло Q,
полученное газом, идет на увеличение
внутренней энергии газа ![]() и
совершение работы A над
внешними телами:
и
совершение работы A над
внешними телами: ![]() .
Молярная
теплоемкость газа при постоянном
давлении:
.
Молярная
теплоемкость газа при постоянном
давлении:
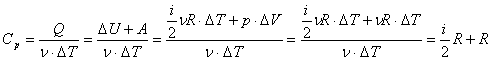 .
.
Таким
образом, теплоемкость газа при постоянном
давлении связана с теплоемкостью газа
при постоянном объеме соотношениями:
![]() ,
,![]() .
.
22. Работа при основных изопроцессах.
ИЗОПРОЦЕССЫ
Изопроцессы — равновесные процессы, в которых один из основных параметров сохраняется.
ИЗОБАРНЫЙ
ПРОЦЕСС (![]() )
Для
изобарного процесса в идеальном газе
справедлив закон Гей-Люссака:
при
постоянном давлении объем данной массы
газа прямо пропорционален его
термодинамической температуре:
)
Для
изобарного процесса в идеальном газе
справедлив закон Гей-Люссака:
при
постоянном давлении объем данной массы
газа прямо пропорционален его
термодинамической температуре:![]() или
или ![]() .
.
 Работа
газа при изобарном расширении:
Работа
газа при изобарном расширении:
![]() .
Изменение
внутренней энергии:
.
Изменение
внутренней энергии:![]() Количество
полученного тепла в соответствии с
первым началом термодинамики:
Количество
полученного тепла в соответствии с
первым началом термодинамики:![]() .
Молярная
теплоемкость при изобарном процессе:
.
Молярная
теплоемкость при изобарном процессе:![]() .
.
ИЗОХОРНЫЙ
ПРОЦЕСС (![]() )
Изохорный
процесс в идеальном газе описывается
законом Шарля:
при постоянном объеме
давление данной массы газа прямо
пропорционально его термодинамической
температуре:
)
Изохорный
процесс в идеальном газе описывается
законом Шарля:
при постоянном объеме
давление данной массы газа прямо
пропорционально его термодинамической
температуре:![]() или
или ![]() .
.
 Работа
газа при изохорном процессе равна
нулю:
Работа
газа при изохорном процессе равна
нулю: ![]() .
Все
полученное тепло идет на изменение
внутренней энергии в соответствии с
первым началом термодинамики:
.
Все
полученное тепло идет на изменение
внутренней энергии в соответствии с
первым началом термодинамики:
![]() .
Молярная
теплоемкость при изохорном процессе:
.
Молярная
теплоемкость при изохорном процессе:![]() .
.
ИЗОТЕРМИЧЕСКИЙ
ПРОЦЕСС (![]() )
Изотермический
процесс в идеальном газе подчиняется
закону Бойля - Мариотта:
для данной
массы газа при неизменной температуре
произведение значений давления и объема
есть величина постоянная:
)
Изотермический
процесс в идеальном газе подчиняется
закону Бойля - Мариотта:
для данной
массы газа при неизменной температуре
произведение значений давления и объема
есть величина постоянная:![]() или
или ![]() .
.
 Работа
газа при изотермическом расширении:
Работа
газа при изотермическом расширении:
 .
Изменение
внутренней энергии при изотермическом
процессе равно нулю:
.
Изменение
внутренней энергии при изотермическом
процессе равно нулю:![]() .
Все
полученное тепло идет на совершение
работы в соответствии с первым началом
термодинамики:
.
Все
полученное тепло идет на совершение
работы в соответствии с первым началом
термодинамики:![]() .
.
23. Фазовые переходы.
В зависимости от условий тела могут находиться в различных агрегатных состояниях. Переход из одного агрегатного состояния в другое называетсяфазовым переходом.
Количество теплоты, выделяемое при кристаллизации тела и поглощаемое телом при плавлении, отнесенное к единице массы тела, называется удельной теплотой плавления (кристаллизации) λ:
|
Q = λm. |
При отвердевании (кристаллизации) выделяется такое же количество теплоты, какое поглощается при плавлении.
Количество теплоты, необходимое для парообразования (выделяющееся при конденсации):
|
Q = Lm, |
где L – удельная теплота парообразования (конденсации).
Если прочие параметры внешней среды (в частности, давление) остаются постоянными, то температура тела в процессе плавления (кристаллизации) и кипения не изменяется.
|
|
|
Плавление льда и кипение воды.(p = 1 атм, m = 4 кг). |
Модель идеального газа не предполагает превращения газа в жидкость при постоянной температуре. Однако, реальные газы, в которых взаимодействием между молекулами пренебречь нельзя, способны при изменении давления превращаться в жидкость, если их температура ниже некоторой критическойTкр.
|
|
|
|
Если количество молекул, покидающих жидкость, равно количеству молекул, возвращающихся в жидкость, то говорят, что наступило динамическое равновесие между жидкостью и ее паром. Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным.
Абсолютная влажность воздуха ρ показывает плотность водяного пара. Относительной влажностью воздуха φ называют отношение абсолютной влажности воздуха ρ к плотности ρ0 насыщенного водяного пара при той же температуре, выраженное в процентах:
|
|
Температура, при которой пар, находящийся в воздухе, становится насыщенным, называется точкой росы.