
- •Теоретический материал,
- •Вынесенный на самостоятельную проработку студентам
- •К теме : Химический состав природной воды
- •Органическое вещество в воде
- •Тема 2: Факторы, влияющие на химический состав воды
- •Тема 3: Источники и характер загрязнения природных водоемов
- •Тема 4: Классификация природных вод
Тема 4: Классификация природных вод
Существуют несколько способов классификации природных вод, в основу которых положены те или иные характеристики химического состава воды.
Классификация вод по степени жесткости (табл.1). Жесткость воды – свойство, обусловленное содержанием в воде катионов двухвалентных металлов, прежде всего кальция и магния. Общая жесткость воды характеризуется содержанием в ней (мэкв/л) катионов жесткости. Величина общей жесткости может быть рассчитана по формуле
Ж (мэкв/л) = [Ca2+]/20,04 + [Mg2+]/12,16.
В общей жесткости воды выделяют карбонатную и некарбонатную жесткость. Карбонатная жесткость жесткость воды представляет собой ту часть общей жесткости, которая эквивалентна содержанию в воде карбонат- и гидрокарбонат-ионов. Также различают жесткость временную (устраняемую кипячением) и постоянную (неустраняемую кипячением). Временная жесткость соответствует содержанию в воде гидрокарбонатов кальция и магния. При кипячении воды происходит удаление катионов этих металлов в составе образующихся малорастворимых карбонатов:
Ca(HCO3)2= СaCO3 ↓+H2O +CO2
Mg(HCO3)2= MgCO3 ↓+H2O + CO2
Постоянная жесткость воды равна разности между общей и временной жесткостью, ее можно устранить только химическими реагентами.
В качестве единицы измерения жесткости воды используется моль (жесткости) на кубический метр, численно равный 1 мг-экв/л.
Таблица 1
Классификация природных вод по величине общей жесткости
|
Общая жесткость , моль/м3 |
Вода |
|
Меньше 1,5 |
Очень мягкая |
|
1,5 – 3,0 |
Мягкая |
|
3,0 – 5,4 |
Средней жесткости |
|
5,4 – 10,7 |
Жесткая |
|
Больше 10,7 |
Очень жесткая |
|
|
|
Классификации по величине общей минерализации воды. Эта классификация (табл. 2) является одной из наиболее распространенных. Величина общей минерализации воды (М) определяется по массе сухого остатка предварительно отфильтрованной и выпаренной пробы воды после высушивания до постоянной массы при температуре 105 °С.
Таблица 2
Классификация природных вод по величине общей минерализации
|
Минерализация, г/л |
Наименование вод |
|
Меньше 0,2 |
Ультрапресные |
|
0,2– 0,5 |
Пресные |
|
0,5 – 1,0 |
С повышенной минерализацией |
|
1 – 3 |
Солоноватые |
|
3 – 10 |
Соленые |
|
10 – 35 |
С повышенной соленостью |
|
35 – 50 |
Переходные к рассолам |
|
50 – 400 |
Рассолы |
Классификация вод по химическому составу. В подавляющем большинстве случаев солевой состав природных вод определяется катионами Са2+, Мg2+, Nа+, К+ и анионами НСO3-, Сl-, SO42-. Эти ионы называются главными ионами воды; они определяют химический тип воды. Остальные ионы присутствуют в значительно меньших количествах, они не определяют химический тип воды.
Классификация природных вод по химическому составу, предложенная О. А. Алекиным (рис. 1), считается наиболее приемлемой для вод, используемых в питьевых и хозяйственно-бытовых целях. В ее основу положены два принципа: преобладающих ионов и соотношения между ними.
Согласно этой классификации природные воды делятся по преобладающему анионуна три класса:
1) гидрокарбонатные и карбонатные (большинство маломинерализованных водрек, озер, водохранилищ и некоторые подземныеводы);
2) сульфатные воды(промежуточные между гидрокарбонатными и хлориднымиводами, генетически связаны с различными осадочнымипородами);
3) хлоридные воды(высокоминерализованныеводыокеана, морей, соленых озер, подземныеводысолончаковых районов).
Каждый класс вод подразделяется по преобладающему катиону на три группы: кальциевую, натриевую, магниевую.
Каждая группа в свою очередь подразделяетсяна четыре типаводпо соотношению содержащихся в воде ионов (в эквивалентах):
I. HCO3-> Ca2+ + Mg2+. Воды этого типа маломинерализованы и характеризуются избытком ионов HCO3-, образуются в процессе химического выщелачиванияизверженныхпород.
II. HCO3- < Ca2+ + Mg2+< HCO3- + SO2-4. К этому типу относятся подземные воды, воды рек и озёр с малой и средней минерализацией.
III. HCO3- + SO2-4< Ca2+ + Mg2+ или Cl-> Na+. Воды этого типа сильно минерализованы, это воды океанов и морей. К этому типу относятся водыокеанов, морей , морских лиманов.
IV. HCO3-= 0. Характеризуется отсутствием гидрокарбонат-ионов. Воды этого типа являются кислыми и присутствуют только в хлоридном и сульфатном классах. Это болотные, шахтные, вулканические воды иливодысильно загрязненные промышленными стоками.
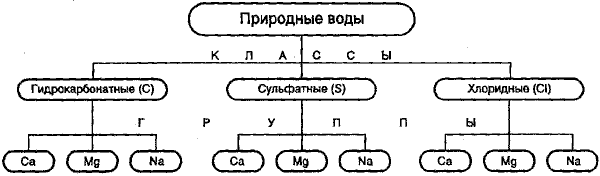
Рис. 1. Схема классификации природных вод по О.А. Алекину
Обозначения.
Класс природных вод обозначается символом соответствующего аниона:
С — НСО3-, S — SO42-, Сl — Сl-;
группа: символом катиона: К+, Na+, Са2+, Мg2+;
тип - римской цифрой.
Формула водызаписывается следующим образом. К символу класса добавляется нижний индекс - значение минерализации (с точностью до 0,1 г/л ), к символу группы - верхний индекс - значение общего катионного состава (с точностью до целых единиц вещества в ммоль/л).
Например: С1,2 Nа0,5 - гидрокарбонатно-натриевая вода с общей минерализацией 1,2 г/л и преобладающей концентрацией гидрокарбонатных ионов и ионов натрия.
Воды большинства рек принадлежат к гидрокарбонатному классу. По составу катионов эта вода имеет почти исключительно преобладание кальция; гидрокарбонатные воды с преобладанием магния и натрия - крайне редкое явление. Из природных вод гидрокарбонатного класса наиболее распространены воды малой минерализации (суммарное содержание солей до 200 мг/л). Они приурочены к подзолистым почвам северных районов лесной зоны и к почвам тундр (включая зону многолетней мерзлоты), которые бедны растворенными солями и обогащают воду органическими веществами. Значительно меньше рек с гидрокарбонатными водами средней минерализации. Это реки средней полосы Европы. Еще меньшую площадь занимают реки с повышенной минерализацией, которые распространены в лесостепной и степной зонах (междуречья Днестра, Южного Буга, Днепра, некоторые притоки Дона и Урала).
Реки с водой, относящейся к сульфатному классу, сравнительно малочисленны и встречаются в засушливых степях Донбасса, Приазовья, Северного Кавказа, в полупустынях Средней Азии и Казахстана. Минерализация их обычно превышает 1000 мг/л. В составе катионов природных вод сульфатного класса, так же как и в водах гидрокарбонатного класса, преобладает кальций. Однако ряд рек сульфатного класса имеет преобладание натрия. По минерализации воды сульфатного класса значительно превосходят воды гидрокарбонатного класса. Речные сульфатные воды с малой (общее количество солей до 200 мг/л) и средней (общее количество солей с 200 до 500 мг/л) минерализацией встречаются сравнительно редко. Наиболее характерна для этих рек повышенная (общее количество солей с 500 до 1000 мг/л), а иногда и высокая (общее количество солей более 1000 мг/л) минерализация воды.
Речные воды хлоридного класса встречаются почти так же редко, как и реки, в воде которых преобладают сульфаты. Это воды преимущественно степных районов и полупустынь (полупустыни Прикаспийской низменности, Западно-Сибирской равнины и Казахстана). Преобладающими катионами природных вод хлоридного класса являются главным образом ионы натрия. Воды хлоридного класса отличаются высокой минерализацией, свыше 1000 мг/л, достигающей в отдельных случаях 19000 мг/л (р. Тургай).
