
- •Федеральное агентство по образованию
- •Программа по дисциплине «химия»
- •Перечень лабораторных работ
- •Вопросы к экзамену
- •Контрольные задания
- •Тема 1. Строение атома и периодическая система элементов д.И.Менделеева
- •Задачи 1 20
- •Тема 2. Химическая связь
- •Теоретические основы
- •Задачи 21 40
- •Тема 3. Химическая термодинамика
- •Теоретические основы
- •Задачи 41 60
- •Тема 4. Химическая кинетика и равновесие
- •Теоретические основы
- •Задачи 61 80
- •Тема 5. Растворы
- •Теоретические основы
- •Задачи 81-100
- •Тема 6. Окислительно-восстановительные реакции
- •Задачи 101 120
- •Тема 7. Электродные потенциалы и электродвижущие силы
- •Тема 8. Коррозия металлов и способы защиты от неё
- •Задачи 141 160
- •Тема 9. Электролиз Теоретические основы
- •Задачи 141 160
- •Тема 10. Химические свойства элементов и их соединений
- •Теоретические основы
- •Задачи 161 180
- •Приложения
Задачи 101 120
Для реакций, схемы которых указаны ниже, составьте уравнения методом электронного баланса. Укажите типы реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем и почему.
С х е м ы р е а к ц и й
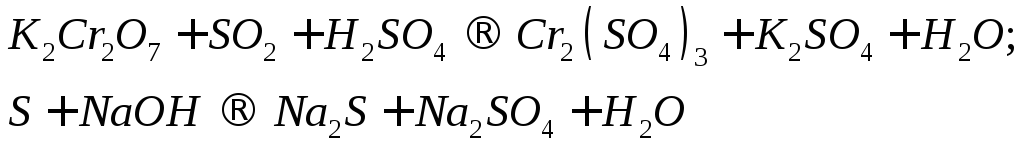
101.
![]()
102.
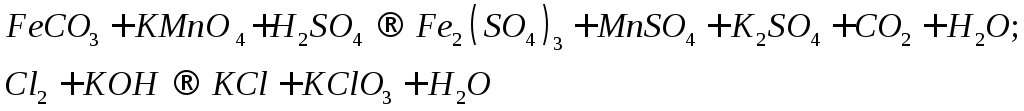
103.
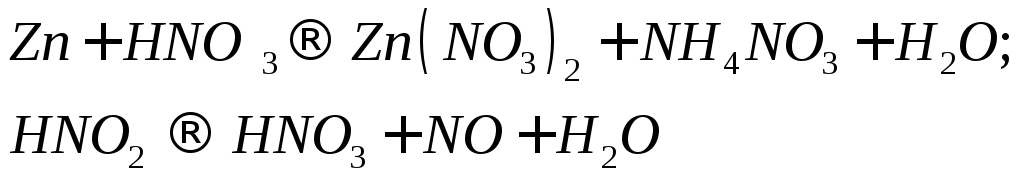
104.
1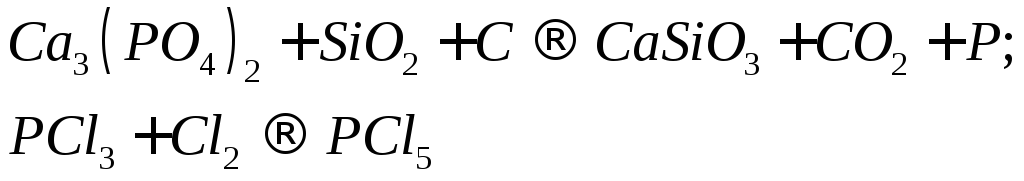 05.
05.
![]()
106.
![]()
107.
![]()
108.
1![]() 09.
09.
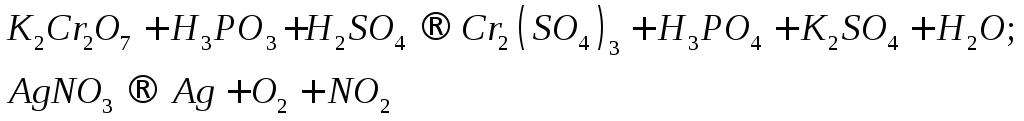
110.
![]()
111.
1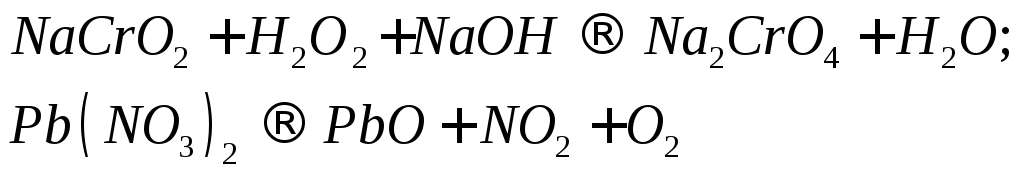 12.
12.
1![]() 13.
13.
![]()
114.
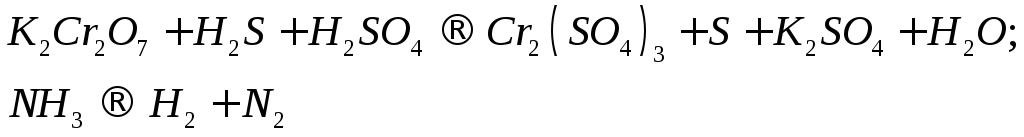
115.
1![]() 16.
16.
![]()
117.
1![]() 18.
18.
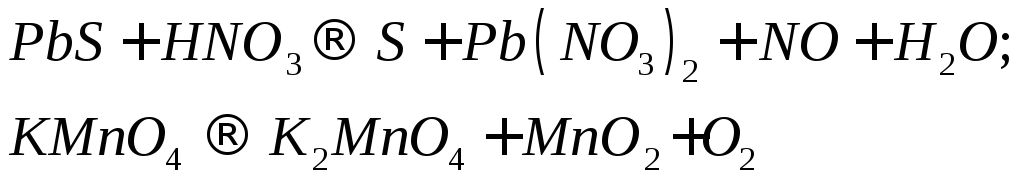
119.
1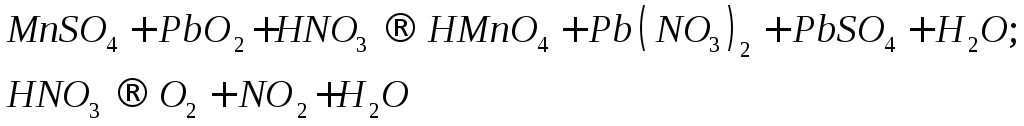 20.
20.
Тема 7. Электродные потенциалы и электродвижущие силы
Литература: [1] c. 260-278, 300-310; [2] с. 272-293; [3] c.219-224
Теоретические основы
При контакте поверхности металла с водным раствором соли определённая часть катионов металла под действием полярных молекул воды в гидратированном виде переходит из металлической фазы в раствор. На границе раздела фаз «металл ─ раствор» устанавливается динамическое равновесие:

При этом металл заряжается отрицательно, если преобладал процесс перехода ионов металла в раствор, или положительно, если преобладал процесс осаждения этих ионов на поверхности металла. Металлический проводник, погружённый в раствор электролита, называется электродом. Разность потенциалов, которая возникает на границе между металлом и водным раствором в состоянии равновесия, называется равновесным электродным потенциалом.
Абсолютные значения электродных потенциалов измерить нельзя. Обычно определяют относительные потенциалы металлов, принимая условно за нуль значение потенциала водородного электрода. Разность потенциалов между металлом, погружённым в раствор своей соли с концентрацией ионов металла 1 моль/л, и стандартным водородным электродом, называется стандартным электродным потенциалом металла (о).
Если расположить металлы в порядке возрастания их стандартных электродных потенциалов, то получим ряд напряжений металлов. Положение металла в ряду напряжений характеризует его восстановительную способность, а также окислительные свойства его ионов в водных растворах при стандартных условиях. Из ряда напряжений металлов (приложение 3) вытекают следствия:
1. Каждый предыдущий металл в ряду напряжений вытесняет расположенный за ним металл из растворов солей.
2. Только металлы с отрицательными значениями потенциалов способны вытеснять водород из его соединений.
3. Чем левее (раньше) в ряду напряжений находится металл, тем легче он отдаёт электроны (электрохимически активнее) и тем труднее восстанавливаются его ионы до атомов.
4. В гальваническом элементе анодом служит тот металл, который в ряду напряжений характеризуется наиболее отрицательным потенциалом, т.е. более активный металл.
Величина электродного потенциала зависит от природы металла, температуры и концентрации раствора электролита. Эта зависимость выражается уравнением Нернста:
![]() ,
где
,
где
– электродный потенциал металла, В;
о – стандартный электродный потенциал металла, В;
R
– универсальная газовая постоянная
(![]() );
);
Т – температура, К;
n – валентность иона металла;
F
– число Фарадея (![]() );
);
С – концентрация ионов металла в растворе, моль/л (моль/л ≡ M).
При подстановке в формулу Нернста всех констант и стандартной температуры (298 К) она приобретает вид:
![]()
При С = 1 моль/л равновесный потенциал становится равным стандартному: = о. Формулу Нернста можно применять только к металлам, погружённым в растворы своих солей.
Гальваническим элементом (ГЭ) называется устройство, в котором химическая энергия окислительно-восстановительной реакции превращается в энергию электрического тока. Гальванический элемент представляет собой систему из двух электродов, растворы электролитов которых сообщаются. На границах металлов и растворов устанавливаются разные электродные потенциалы. При замыкании цепи электроны перемещаются по внешнему её участку от электрода с меньшим потенциалом к электроду с большим потенциалом. На первом электроде идёт процесс окисления:
![]() .
.
Этот электрод, который в процессе работы ГЭ окисляется и посылает электроны во внешнюю цепь, называется анодом.
На втором электроде, называемом катодом, происходит восстановление катионов, присутствующих в растворе электролита:
![]() .
.
Металл Me2 осаждается на катоде. Анод в гальванических элементах имеет знак минус, катод - плюс.
Электродвижущая сила (ЭДС, или Е) рассчитывают по формуле:
ЭДС = К - А,
где К и А - электродные потенциалы катода и анода, соответственно.
Пример. Рассмотрим работу гальванического элемента, составленного из медного и цинкового электродов, погруженных в раствор соответствующих сульфатов с концентрациями:
С(CuSO4) = 0,01 моль/л и С(ZnSO4) = 0,1 моль/л.
Решение. Краткая схема данного гальванического элемента:
![]()
Вертикальная часть обозначает поверхность раздела между металлом и раствором, а две черты - границу раздела двух жидких фаз - пористую перегородку (или соединительную трубку, заполненную раствором электролита, которую называют солевым мостиком). Значения стандартных электродных потенциалов меди и цинка:
оСu = + 0,34 B, оZn = - 0,76 B (см. приложение 3).
Следовательно, цинковый электрод вданном ГЭ является анодом, а медный – катодом. Цинк отдаёт электроны, то есть окисляется, и его ионы переходят в раствор. На катоде происходит восстановление ионов меди. Уравнения электродных процессов:
А)
![]()
К)
![]()
Суммарное
уравнение реакции, которое служит
источником электрической энергии в
медно-цинковом гальваническом элементе,
имеет вид:
![]() .
.
Подобного рода источники тока называются гальваническими элементами Якоби-Даниэля. Полная схема рассматриваемого ГЭ записывается следующим образом:
















 е-
е-
V
A- SO42- K+
Zn Cu


раствор ZnSO4 раствор CuSO4
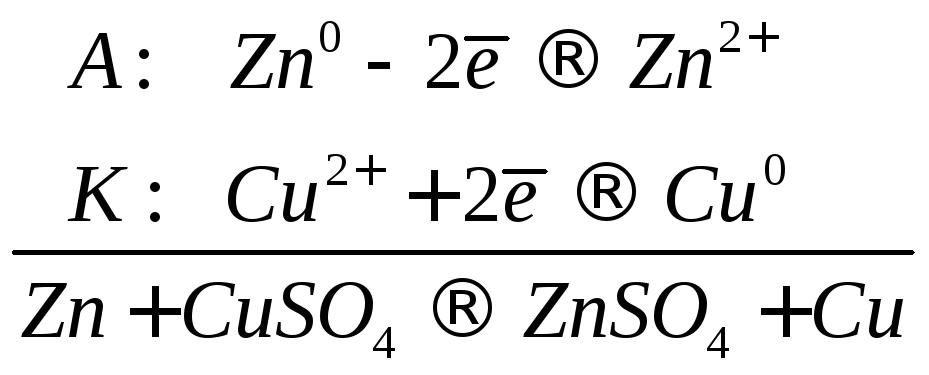
Для определения электродвижущей силы вычислим сначала электродные потенциалы меди и цинка по уравнению Нернста:
![]()
![]()
Электродвижущая сила:
![]() .
.
Задачи 101 120
Составьте полную схему гальванического элемента, напишите уравнения электродных процессов и вычислите ЭДС. Необходимые для решения данные приведены в табл. 6.
Таблица 6
|
N задачи
|
Металл 1 |
Металл 2 |
Электро-лит 1 |
Концентра ция электролита 1 |
Электро-лит 2 |
Концентра-ция электролита 2 | |
|
121 |
Ag |
Ag |
|
1,0 M |
|
0,001 M | |
|
122 |
Cu |
Mg |
|
0,1 M |
|
0,1 M | |
|
123 |
Zn |
Ni |
|
0,1 M |
|
0,1 M | |
|
124 |
Zn |
Zn |
|
1,0 M |
|
0,01 M | |
|
125 |
Cr |
Cu |
|
0,1 M |
|
0,1 M | |
|
126 |
Mg |
Cu |
|
0,1 M |
|
0,1 M | |
|
127 |
Zn |
Pb |
|
0,01 M |
|
0,01 M | |
|
128 |
Cd |
Ni |
|
0,1 M |
|
0,1 M | |
|
129 |
Ni |
Pb |
|
0,1 M |
|
1,0 M | |
|
130 |
Cu |
Cu |
|
0,1 M |
|
0,001 M | |
|
131 |
Zn |
Fe |
|
0,1 M |
|
0,1 M | |
|
132 |
Mg |
Cd |
|
0,01 M |
|
0,1 M | |
|
133 |
Fe |
Ag |
|
0,1 M |
|
0,1 M | |
|
134 |
Co |
Cu |
|
0,01 M |
|
0,001 M | |
|
135 |
Fe |
Ni |
|
0,1 M |
|
0,1 M | |
|
136 |
Zn |
Ag |
|
0,1 M |
|
0,01 M | |
|
137 |
Cu |
Ni |
|
0,1 M |
|
1,0 M | |
|
138 |
Fe |
Cu |
|
0,01 M |
|
0,1 M | |
|
139 |
Pb |
Mg |
|
0,1 M |
|
0,1 M | |
|
140 |
Ni |
Co |
|
1,0 M |
|
0,1 M | |
