
- •Основы строения органических соединений
- •Классификация органических соединений. Функциональная группа и строение углеродного скелета как классификационные признаки органических соединений, Главные классы органических соединений.
- •Электронное строение атомов углерода. Виды гибридизации.
- •Сопряжение (, и р,). Энергия сопряжения. Сопряженные системы с открытой и замкнутой цепью сопряжения (вопр. 6): строение, устойчивость, примеры.
- •Ароматическое строение; энергия резонанса (сопряжения) на примерах: бензол, нафталин, гетероциклические соединения.
- •Взаимное влияние атомов в молекулах органических соединений: индуктивный и мезомерный эффекты. Примеры.
- •Электронодонорные и электроноакцепторные заместители. Распределение электронной плотности в молекуле. Примеры.
- •Пространственное строение органических соединений: конфигурация, конформация; способы изображения; примеры.
- •Хиральные и ахиральные молекулы. Асимметрический атом углерода. Примеры. Оптическая активность.
- •Виды конфигурационной стереоизомерии. Энантиомерия и диастереомерия. Относительная и абсолютная конфигурация. D,l– и r,s–системы стереохимической номенклатуры. Рацематы. Примеры.
- •Конфигурационная стереоизомерия молекул с двумя и более центрами хиральности. ,–диастереомерия. Свойства энантиомеров и диастереомеров.
- •Конформации ациклических углеводородов (этан, бутан); виды напряжений в молекуле; изображение конформаций; их энергетическая характеристика.
- •Конформации циклогексана; виды напряжений, энергетическая характеристика конформаций; аксиальные и экваториальные связи; инверсия цикла у производных циклогексана (метилциклогексан).
- •Кислотные и основные свойства органических молекул; теории Бренстеда и Льюиса. Примеры.
- •Типы органических кислот. Факторы, определяющие кислотность. Примеры.
- •Типы органических оснований. Факторы, определяющие основность. Примеры.
- •Классификация органических реакций и реагентов. Примеры.
-
Электронодонорные и электроноакцепторные заместители. Распределение электронной плотности в молекуле. Примеры.
Графически I-эффект обозначается стрелкой на конце валентной черты, направленной в сторону более электроотрицательного атома. Направление I-эффекта заместителя качественно оценивают, сравнивая с практически неполярной связью С—Н и полагая I-эффект водорода равным нулю. Заместители, смещающие электронную плотность σ-связи сильнее, чем водород, проявляют отрицательный I-эффект (-I-эффект). Такие электронооттягивающие заместители снижают электронную плотность в системе σ-связей, их называют электроноакцепторными. Эффект тем сильнее, чем больше электроотрицательность гетероатома.
![]()
![]()
Электроноподающие заместители повышают электронную плотность в цепи σ-связей по сравнению с водородом, т. е. проявляют +I-эффект и являются электронодонорными. К ним относятся атомы с низкой электроотрицательностью, а также отрицательно заряженные атомы или группы, обладающие избытком электронной плотности, которую стремятся перераспределить на соседние связи.
Алкильные группы, связанные с атомами углерода в sp2- или sp-гибридном состоянии, проявляют +I-эффект. Например, в молекуле пропена 12С метальной группы в sp3-гибридном состоянии, менее электроотрицателен, чем гибридизованные 12С двойной связи. Поэтому метальная группа выступает в роли электронодонора и ее влияние в первую очередь испытывает π-связь. Смещение электронной плотности π-связи обозначают изогнутой стрелкой:
![]()
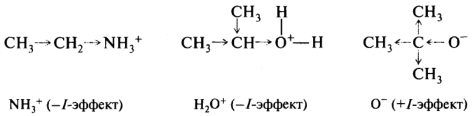
Алкильные группы проявляют +I-эффект только в растворе, в газовой фазе они могут обнаруживать и -I-эффект. Наибольшего значения индуктивные эффекты достигают в том случае, когда на атоме или группе атомов имеется полный заряд. Ионы индуцируют особенно сильное смещение электронной плотности, которое распространяется далеко по цепи.
Заместитель может вносить в систему сопряжения π-связь (π,π-сопряжение) или р-АО, которая может быть либо вакантной, либо занятой 1 электроном или неподеленной парой электронов (p,π-сопряжение). М-эффект отражает тот факт, что р-орбитали заместителя, перекрываясь с орбиталями π-связей, образуют делокализованную орбиталь более низкой энергии. М-эффект передается по сопряженной системе без затухания.
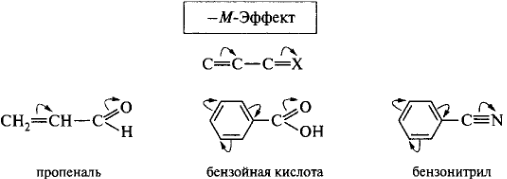
Заместители, понижающие электронную плотность в сопряженной системе (смещающие электронную плотность в свою сторону), проявляют отрицательный мезомерный эффект (-М-эффект) и являются электроноакцепторными. К ним относятся заместители, содержащие кратные связи атома углерода с более электроотрицательным гетероатомом.
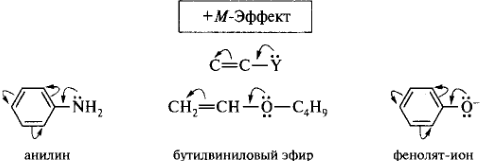
Заместители, повышающие электронную плотность в сопряженной системе (смещающие электронную плотность от себя в сторону сопряженной системы), проявляют положительный мезомерный эффект (+М-эффект). К ним относятся заместители, содержащие гетероатом с неподеленной парой электронов или имеющие отрицательный заряд. Эти заместители являются электронодонорными и за счет включения в состав сопряженной системы своей пары электронов создают избыточность электронной плотности в цепи сопряжения.
