
- •Г. Н. Роганов органическая химия Учебно-методическое пособие
- •Часть 1
- •Содержание
- •Часть 1
- •Часть 2
- •Предисловие
- •Введение
- •1 Углеводороды
- •1.2 Алкены (этиленовые углеводороды или олефины)
- •1.3 Диеновые углеводороды (алкадиены)
- •1.4 Алкины (ацетиленовые углеводороды)
- •1.5 Алициклические углеводороды
- •1.6 Ароматические углеводороды
- •2 Гидроксисоединения
- •2.1 Спирты
- •2.1.1 Одноатомные спирты
- •2.1.1.1 Насыщенные одноатомные спирты
- •2.1.1.2 Ненасыщенные одноатомные спирты
- •2.1.2 Многоатомные спирты
- •2.1.2.1 Гликоли
- •2.1.2.2 Глицерин
- •2.2 Фенолы и ароматические спирты
- •2.2.1 Фенолы
- •2.2.2 Ароматические спирты
- •3 Простые эфиры
- •3.1 Алифатические простые эфиры
- •3.2 Циклические простые эфиры или органические окиси (эпоксисоединения)
- •4 Карбонильные соединения (альдегиды и кетоны, оксосоединения )
- •4.1 Насыщенные карбонильные соединения
- •4.2 Ненасыщенные карбонильные соединения
- •4.3 Ароматические карбонильные соединения
- •Список использованной литературы
- •Приложение а учебно-методические материалы для самостоятельной работы студентов
- •Продолжение приложения а
- •Продолжение приложения а
- •Приложение б
- •Часть 1
4.2 Ненасыщенные карбонильные соединения
Акролеин

Акролеин получают кротоновой конденсацией формальдегида с ацетальдегидом
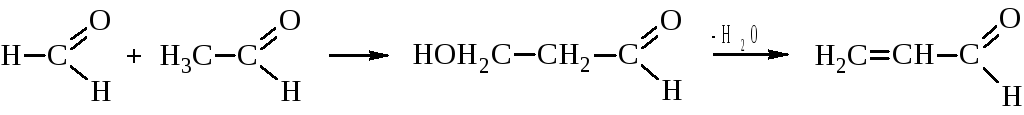
и каталитическим окислением пропилена.

Он получается также дегидратацией глицерина (смотри реакции многоатомных спиртов), образующегося гидролизом растительных масел при длительном нагревании их на открытом воздухе (приготовление чипсов, жарка и т. п.) и является вредным для здоровья человека компонентом пищи.
Акролеин проявляет свойства алкена и альдегида одновременно. Он имеет сопряжённую систему двойных связей.

Присоединение HBr протекает по типу 1,4 в соответствии с распределением зарядов. Получающийся нестойкий енол благодаря таутомерному превращению переходит в устойчивую карбонильную форму. В результате HBr оказывается присоединенным по двойной связи вопреки правилу Марковникова.

Используется акролеин для получения пластмасс.
Кротоновый альдегид

Получается кротоновой конденсацией ацетальдегида. Используется в производстве масляного альдегида, масляной кислоты, малеинового ангидрида.
Метилвинилкетон (бутенон-2)

Используется в производстве полимеров.
4.3 Ароматические карбонильные соединения
Ароматические альдегиды и кетоны имеют карбонильную группу >С=О, непосредственно связанную с углеродом ароматического цикла или находящуюся в боковой цепи. Соединения с карбонильной группой в боковой цепи проявляют свойства, аналогичные свойствам альдегидов и кетонов алифатического или алициклического рядов.
Названия альдегидов первого типа даются по названиям соответствующих им ароматических кислот, второго типа – называются как арилзамещённые альдегидов жирного ряда.

Кетоны называют по радикалам или как «производные» кислот.

Способы получения
Для получения ароматических альдегидов и кетонов в большинстве случаев могут использоваться обычные методы синтеза кетонов и альдегидов, рассмотренные ранее. Однако имеются и оригинальные методы получения этих соединений
– Окисление ароматических углеводородов с боковой цепью (преимущественно для альдегидов).
Реакция в жидкой фазе идёт в присутствии смеси MnO2 + 60 % H2SO4 , в газовой фазе окисление приводят кислородом воздуха в присутствии катализатора V2O5.

– Гидролиз геминальных дигалогенпроизводных в присутствии железа в качестве катализатора.

– Прямое введение альдегидной группы в ядро (реакция Гаттермана-Коха). Реакция протекает при пропускании оксида углерода и хлористого водорода во взвесь углеводорода и AlCl3. Предполагается, что промежуточным продуктом является хлористый формил.


Таким образом из гваякола получают ванилин

– Подобную реакцию используют и для получения кетонов. При этом на ароматический углеводород действуют галогенангидридами или ангидридами кислот в присутствии безводного хлористого алюминия (реакция Фриделя-Крафтса)

Химические свойства
Ароматическим альдегидам и кетонам свойственно большинство реакций альдегидов и кетонов алифатического ряда. Они присоединяют синильную кислоту, реагируют с гидразином и его производными. Оксидом серебра альдегиды окисляются до кислот. Однако они вступают и в специфические реакции, не характерные для карбонильных соединений алифатического ряда.
– При хранении ароматические альдегиды интенсивно самопроизвольно окисляются кислородом воздуха до кислот.
Реакция ускоряется светом и катализаторами – солями металлов. Фенол и амины ингибируют окисление.
– Реакция Канниццаро
Протекает в водных или спиртовых растворах щелочей. При этом одна молекула ароматических альдегидов окисляется до кислоты, другая – восстанавливается до спирта.
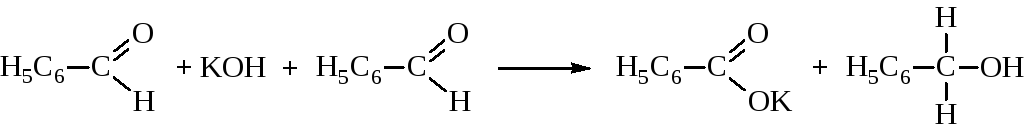
Большинство алифатических альдегидов в условиях реакции Канниццаро подвергаются осмолению (полимеризации).
– При электрофильном замещении альдегидная группа ориетирует в мета-положение.

– Ароматические альдегиды весьма реакционноспособные соединения и легко вступают в различные реакции конденсации с альдегидами, кетонами, эфирами и ангидридами кислот алифатического ряда и между собой.
– Ароматические кетоны менее реакционноспособны по сравнению с алифатическими. Они, например, не присоединяют гидросульфит натрия.
Отдельные представители
Бензойный альдегид – жидкость с запахом горького миндаля Кипит при температуре 179 °С. Легко окисляется на воздухе до бензойной кислоты. Используется в производстве красителей и душистых веществ.
Ацетофенон. tплав= 20 °С, tкип= 202 °С. Имеет запах цветов черёмухи. Применяется в парфюмерии.
Бензофенон применяется в парфюмерной промышленности.
