
- •Содержание
- •Общие методические указания
- •Модуль 1. Особенности силикатных материалов и процессов их синтеза
- •Задание 1. Термодинамика реакций в силикатных системах
- •Лабораторная работа № 1
- •Изучение химического равновесия в гетерогенной системе
- •(Расчет термодинамических характеристик реакции
- •Разложения карбоната кальция)
- •Лабораторная работа № 2 Кинетика гетерогенной химической реакции (расчет кинетических характеристик реакции разложения карбоната кальция)
- •Модуль 2. Фазовые равновесия в силикатных системах и диаграммы состояния
- •Задание 2. Диаграммы состояния двухкомпонентных систем Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Задание 3. Диаграммы состояния трехкомпонентных систем
- •Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 11
- •Расчет термодинамических характеристик кристаллизующихся веществ по данным термического анализа
- •Список литературы
Вариант 11
Твердая смесь, содержащая 20% Na2O, 10% CaO и 70% SiO2, нагрета до 900ºС. Будет ли при этой температуре существовать твердая фаза, какая и в каком количестве?
Опишите процесс кристаллизации расплавов следующих составов: а) 5% Na2O, 35% CaO, 60% SiO2; б) 20% Na2O, 10% CaO, 70% SiO2. Определите температуру завершения кристаллизации расплавов указанных составов.
Вариант 12
Определите, при какой температуре полностью расплавится стекло, в состав которго входит 14% Na2O, 13% CaO и 73% SiO2. На сколько градусов изменится температура плавления стекла при замене 3% Na2O на 3% SiO2.
Опишите процесс кристаллизации расплавов системы Na2O – CaO – SiO2, если изображающие их состав точки находятся: а) на изотерме 1000ºС в поле кристаллизации соединения Na2O·3CaO·6SiO2; б) на изотерме 1300ºС в поле кристаллизации соединения CaO·SiO2.
Лабораторная работа № 3
Построение диаграммы состояния
двухкомпонентной системы (термический анализ)
Цель работы: освоить метод термического анализа, построить диаграмму состояния двухкомпонентной системы, рассчитать термодинамические характеристики кристаллизующихся компонентов.
Приборы и реактивы
Учебно-лабораторный комплекс «Химия» в следующей комплектации:
– центральный контроллер;
– модуль «Термический анализ» в комплекте с одиннадцатью ампулами, содержащими смеси различных составов (от 10 до 90 мас.%), и ампулы с чистыми компонентами.
Термический анализ
Изучение многокомпонентных систем, образующих несколько фаз, производится при помощи физико-химического анализа, в основе которого лежит изучение функциональной зависимости между физическими свойствами системы и факторами, определяющими ее равновесие. В качестве изучаемых свойств могут быть выбраны: тепловые, электрические, механические и др. Найденные из опыта зависимости изображают в виде диаграмм состав – свойство.
Частным случаем физико-химического анализа является термический анализ, заключающийся в определении температуры, при которой в равновесной системе изменяется число фаз. Анализ основан на изучении изменения температуры системы в зависимости от времени охлаждения. В результате получаются так называемые кривые охлаждения, вид которых зависит от состава и типа смеси.
Кривые охлаждения
При охлаждении системы скорость понижения температуры пропорциональна разности температур системы и окружающей среды:
![]() .
.
Из этого уравнения следует, что кривые охлаждения должны быть вогнуты к оси времени t. При большей разности температур они близки к прямой линии.
Кристаллизация расплавленного индивидуального вещества, подвергнутого медленному охлаждению, вызывает температурную остановку (рис. 17, кривая 1), так как состав жидкой фазы остается неизменным и выделяющаяся теплота кристаллизации полностью компенсирует отвод тепла в окружающую среду. На кривой охлаждения 1 моменту выпадения первого кристалла отвечает точка b. Длительность температурной остановки, и тем самым размер горизонтального участка на кривой охлаждения, зависят от количества вещества и от скорости отвода тепла. При исчезновении последней капли жидкости (точка c на кривой 1) температура вновь начинает понижаться, поскольку с этого момента потеря тепла в окружающую среду уже ничем не компенсируется.

Рис. 17 Кривые охлаждения расплавов индивидуальных веществ
(Тк – температура кристаллизации)
При охлаждении расплава двухкомпонентной системы (рис. 18) сначала кристаллизуется тот компонент, относительно которого жидкий расплав становится насыщенным. Кривая охлаждения (рис. 18, кривая 2) в точке b имеет излом, т.к. скорость охлаждения понижается вследствие выделения теплоты кристаллизации. Отсутствие температурной остановки объясняется тем, что состав жидкой фазы при кристаллизации меняется. При достижении температуры, при которой жидкий раствор становится насыщенным относительно и второго компонента, происходит одновременная кристаллизация обоих компонентов. Раствор, насыщенный обоими компонентами и имеющий наименьшую температуру кристаллизации, называется эвтектическим. Состав жидкой фазы остается постоянным. Поэтому на кривой охлаждения 2 наблюдается температурная остановка cd. После отвердевания всей смеси (точка d на кривой 2) температура снова понижается.
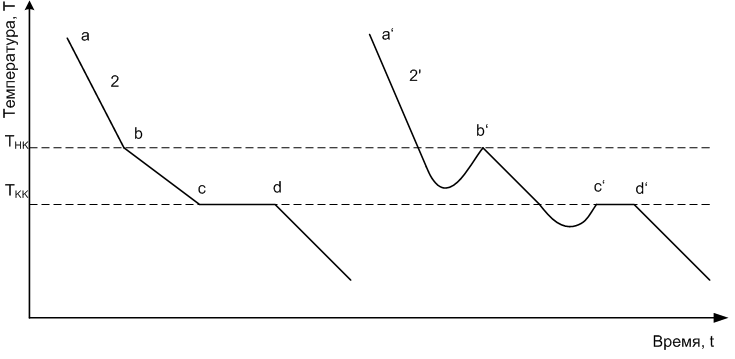 Рис.
18 Кривых охлаждения расплавов
двухкомпонентной системы
Рис.
18 Кривых охлаждения расплавов
двухкомпонентной системы
(Тнк – температура начала кристаллизации;
Ткк – температура конца кристаллизации)
Кривые 1 и 2 (рис. 17,6) представляют собой идеальные кривые охлаждения, которые наблюдаются при кристаллизации простых веществ. Сложные вещества и их смеси, в частности органические, как правило, кристаллизуются с переохлаждением, величина которого зависит от чистоты вещества и условий охлаждения. Это приводит к более сложной форме кривых охлаждения (кривые 1' и 2' на рис. 17, 18).
В качестве температуры начала кристаллизации в этих случаях следует взять температуру в точке b', а в качестве температуры конца кристаллизации – температуру в точке c'.
Построение диаграммы состояния
Ординаты точек b и c, т.е. температуры начала и конца кристаллизации, зависят от состава каждой смеси. Эта зависимость, выраженная графически в координатах температура – состав, носит название диаграммы плавкости (рис. 19).
Точки ТА и ТВ соответствуют температурам кристаллизации чистых компонентов, точки Т1– 4 – температурам начала кристаллизации смесей различных составов (x1 – x4). Линия, соединяющая все точки с температурами начала кристаллизации, называется линией ликвидуса. Поле диаграммы выше линии ликвидуса отвечает области условий существования системы в жидком состоянии. Линия, соединяющая все точки с температурами конца кристаллизации, называется линией солидуса. В области диаграммы ниже линии солидуса вся система находится в твердом состоянии.
 Рис.
19 Вид диаграммы плавкости и принцип её
построения
Рис.
19 Вид диаграммы плавкости и принцип её
построения
Точные координаты эвтектической точки можно определить с помощью треугольника Таммана. Тамманом было замечено, что длительность температурной остановки на кривой охлаждения пропорциональна количеству эвтектики в исходной смеси. Максимальную температурную остановку при кристаллизации имеет смесь эвтектического состава. Отложив длины отрезков cd (температурных остановок) как функцию состава смеси, Тамман получил две прямые, пересекающиеся при составе, имеющем наибольшую длительность температурной остановки, т.е. при составе эвтектики. Получившаяся фигура имеет вид треугольника.
Методика выполнения работы и ее обоснование
Для получения диаграммы состояния двухкомпонентной системы методом термического анализа необходимо построить кривые охлаждения как чистых компонентов, так и их смесей в различных соотношениях. Для этого используют несколько смесей, составленных через 10 мас.% во всем возможном диапазоне изменения концентраций. Все смеси для выполнения работы приготовлены заранее и находятся в герметичных ампулах, выполненных из нержавеющей стали.
Каждую смесь необходимо нагреть до температуры, превышающей на несколько градусов температуру полного плавления смеси, чтобы исследуемая система находилась в виде расплава. Для этого модуль «Термический анализ» имеет специальный элемент, предназначенный для одновременного нагревания нескольких ампул.
Далее необходимо провести постепенное охлаждение каждой ампулы с фиксированием значения температуры через определенные интервалы времени. Оно происходит в специальном измерительном блоке модуля. Для равномерного охлаждения ампулы обдуваются потоком воздуха.
Наиболее ответственным этапом выполнения работы является анализ полученных кривых охлаждения. Кривые охлаждения часто бывают довольно сложными, перегибы и температурные остановки на них могут иметь маловыраженный характер.
Если до охлаждения система находилась в полностью расплавленном состоянии, то первый перегиб указывает на температуру начала кристаллизации системы (этот перегиб в нашем случае виден наиболее отчетливо). Наличие последующих перегибов или температурных остановок будет указывать на появление в системе новых фаз. Для построения диаграммы состояния изучаемой системы на нее переносятся все выявленные на кривых охлаждения точки.
Диаграмму строят в координатах температура – состав и для каждой изученной смеси откладывают температуры фазовых переходов (начала и конца кристаллизации), которые были определены в результате анализа кривых охлаждения. Таким образом, ордината каждой точки соответствует температуре начала выявленного фазового перехода для определенной смеси, а абсцисса – составу этой смеси (например, массовому или мольному проценту одного из компонентов). На основании полученных точек проводят линии диаграммы.
Порядок выполнения работы
Модуль «Термический анализ» имеет три группы гнезд для размещения ампул. Первая группа, предназначенная для нагревания ампул, имеет четыре гнезда и снабжена нагревательным элементом. Вторая группа (расположенная по середине) имеет шесть гнезд и предназначена для хранения ампул, не задействованных в текущем опыте. Третья группа – измерительный блок – имеет четыре гнезда, предназначенных для охлаждения предварительно нагретых ампул с фиксированием температуры в каждой ампуле в ходе охлаждения. Блок снабжен вентилятором для обдува ампул воздухом. Центральный контроллер позволяет управлять включением и выключением нагревательного элемента и вентилятора модуля.
Для подготовки модуля к работе необходимо при выключенном контроллере подключить шнур модуля к разъему контроллера и подключить контроллер и модуль к электрической сети (220 В). Каждая ампула на крышке имеет цифровую маркировку. Номер ампулы, умноженный на 10, соответствует содержанию одного из компонентов, выраженному в массовых процентах.
Включают нагревательный элемент и вентилятор модуля. Ампулы, выбранные для текущего эксперимента, размещают в нагревательном блоке и нагревают выше температуры плавления смесей. Следят за показаниями термодатчиков на измерительных каналах.
После достаточного нагрева ампулы перемещают в измерительный блок для проведения охлаждения. Начинают охлаждение ампул с фиксированием значений температуры в каждой ампуле через равные промежутки времени (10 сек.). Измерения проводят до температуры 25 – 26 °С.
По окончании всего цикла измерений (работы со всеми ампулами) начинают просмотр экспериментальных данных. Результаты измерений хранятся в энергонезависимой памяти контроллера.
Строят кривые охлаждения – графики зависимости температуры в ампуле от времени охлаждения.
Проводят анализ кривых охлаждения: выявляют перегибы и температурные остановки на графиках.
По графикам определяют температуры начала (Tнк) и конца кристаллизации (Tкк).
С целью определения координат точки эвтектики строят треугольник Таммана в координатах время – состав.
На основании полученных данных строят фазовую диаграмму системы нафталин – фенол.
С помощью уравнения Шрёдера рассчитывают энтальпии плавления и криоскопические константы нафталина и фенола.
Рекомендуемый вид таблицы
-
№ п/п
Состав
Температура, °С
мас. %
мольн. %
начала
кристаллизации, Tнк
конца
кристаллизации, Tкк
