
- •Оглавление
- •Глава 4. Результаты и обсуждение 2
- •Глава 4. Результаты и обсуждение
- •4.1. Изучение влияния лигноцеллюлозных субстратов на синтез основного фермента-биокатализатора деструкции
- •4.2. Изучение эффективности способов иммобилизации мицелия штамма-деструктора на носителях разных типов
- •4.2.1 Иммобилизация мицелия гриба в колбах на круговой качалке
- •4.2.1.2 Засев носителя поверхностной культурой
- •4.2.2. Иммобилизация мицелия гриба в стационарном состоянии
- •4.3 Изучение динамики оксидазной активности в культуральной жидкостиTrametes hirsuta 56, иммобилизованного на различных носителях
- •4.4 Изучение динамики оксидазной активности культуральной жидкости базидиального грибаTrameteshirsuta56, иммобилизованного с использованием различных способов засева носителя
- •4.5. Выбор модельного соединения для проведения экспериментов по биодеградации
- •4.6. Изучение влияния различных параметров на проведение процесса биодеградации модельного соединения
- •4.6.1. Изучение влияния концентрации модельного соединения на жизнеспособность продуцента
- •4.6.2. Изучение влияния активности лакказы на процесс биодеградации модельного соединения
- •4.6.3. Изучение влияния значения рН на процесс биодеградации модельного соединения
- •4.6.4.Изучение влияния температуры на процесс биодеградации модельного соединения
- •4.7. Изучение процесса биодеградации модельного соединения
- •4.7.1. Изучение процесса биодеградации модельного соединения в колбах
- •4.7.2.Разработка, монтаж и испытания экспериментальной установки
- •Список литературы
4.7.2.Разработка, монтаж и испытания экспериментальной установки
Полученные в экспериментах данные были использованы при разработке экспериментальной установки для биодеградации токсических веществ, содержащихся в промышленных стоках.

Рисунок – 22. Экспериментальная установка для биодеградации токсических веществ, содержащихся в промышленных стоках
Основным элементом установки (рисунок 22) является биореактор насадочного типа рабочим объемом 1 л, в который помещена насадка с иммобилизованным мицелием продуцента лакказы. Очищаемая жидкость из загрузочной емкости подается в биореактор при помощи перистальтического насоса и равномерно распределяется по поверхности насадки оросительным устройством.
Воздух в реактор подается компрессором. Прошедшая через насадку жидкость самотеком возвращается в загрузочную емкость. Расход жидкости в установке - 30 л/час, расход воздуха – до 5 л/мин.
В качестве носителя для иммобилизации мицелия гриба в данном эксперименте были использованы сосновые стружки. Иммобилизацию осуществляли стационарным способом в течение 14 суток. В качестве очищаемой жидкости был использован водный раствор красителя Methyl Orange с исходной концентрацией соединения 0, 15 мг/мл. pH раствора был доведен до значения 4,5 титрованием. Объем насадки составил 1000 см3, объем очищаемой жидкости – 2,5л. Эксперимент осуществляли в течение 12 часов при температуре 32ºС.
Результат эксперимента представлен на рисунке 23.
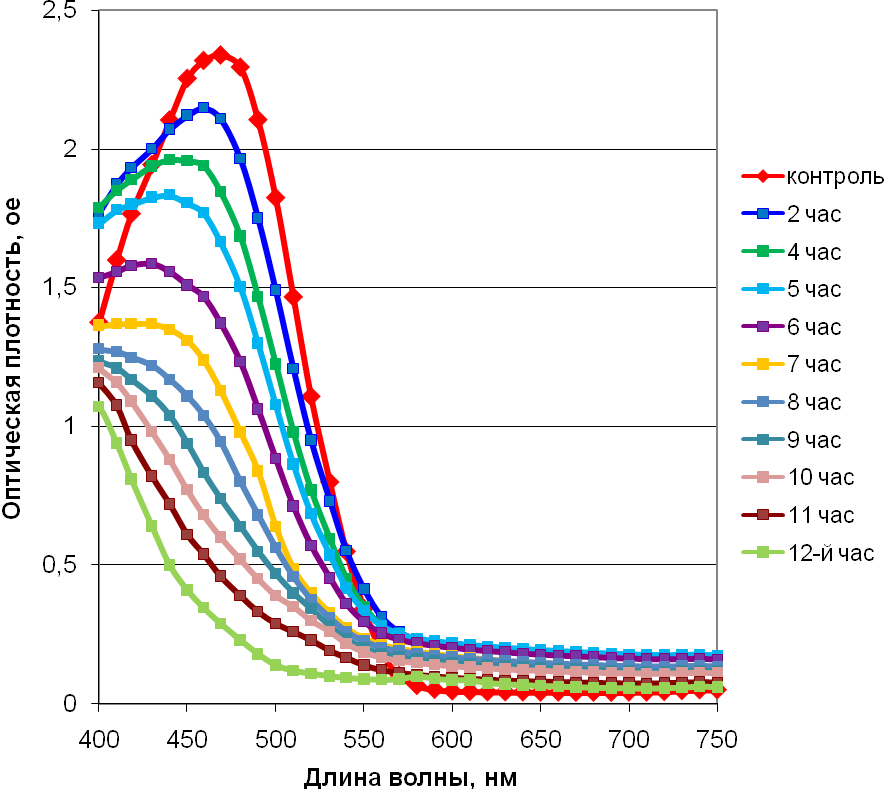
Рисунок – 23. Изменение спектра красителяMethylOrangeпод воздействием лакказы иммобилизованного на сосновых стружках мицелия через 12 часов эксперимента
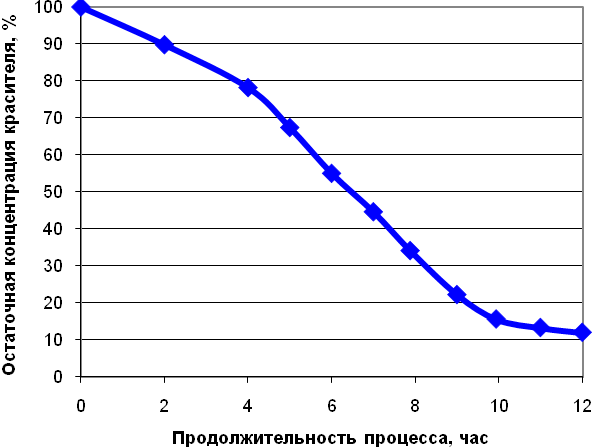
Рисунок – 24. Изменение концентрации красителяMethylOrangeпод воздействием лакказы иммобилизованного на сосновых стружках мицелия через 12 часов эксперимента
В результате проведения эксперимента установлено, что степень деградации красителя MethylOrangeсоставила 88% за 12 часов протекания процесса (рисунок 24). При этом сорбции красителя мицелием гриба не наблюдалось, о чем свидетельствуют данные микроскопического анализа (рисунок 25).

Рисунок – 25. Иммобилизованный на сосновых стружках мицелий штамма-продуцента лакказы после 12 часов проведения эксперимента по биодеградации модельного соединения
Основные результаты и выводы
Показано, что из числа отобранных по литературным данным носителей для иммобилизации гриба мицелий штамма-деструктора наиболее эффективно иммобилизуется и обладает наибольшей синтетической активностью на носителях с воздухопроницаемой структурой, в частности, стальных губках
Установлено, что лигноцеллюлозные отходы существенно (в 1,3-1,8 раза) увеличивают синтез фермента-биокатализатора (лакказы), что повышает эффективность биодеградации ксенобиотиков
Показано, что наиболее перспективным носителем для иммобилизации штамма-деструктора являются древесные стружки, которые легко утилизируются после использования, что исключает образование новых слабо деградируемых отходов отработанного носителя.
Отобраны модельные соединения для проведения экспериментов по биодеградации сточных вод текстильного поизводства – красители MethylOrangeиMethylGreen. Показано, что предельная концентрация токсического вещества в растворе модельного соединения, при котором происходит девитализация клетов гриба составляет 0,5 мг/мл. Концентрации ниже 0,1 мг/мл не влияют на жизнеспособность штамма-продуцента лакказы.
Разработана методика иммобилизации мицелия штамма-деструктора на древесных струдках с использованием глубиного посевного материала.
Показано, что для осуществления деградации без снижения скорости достаточно в реакционной смеси активности лакказы – 1 ое/мл.
Выявлен наиболее благоприятный диапазон рН для проведения биодеградации 4,5–5,0.
Экспериментально подтверждена эффективность биодеградации ксенобиотиков с помощью иммобилизованного мицелия базидиального гриба Trametes hirsuta, которая дляMethylOrangeдостигает 88% в течение 12 часов, а дляMethylGreen92% при исходной концентрации модельного соединения 0,015%.
На основании полученных экспериментально исходных данных разработана экспериментальная установка для биодеградации токсических веществ в сточных водах с использованием иммобилизованного мицелия ксилотрофа.
Предложено в дальнейшем продолжать работу в направлении уточнения параметров и интенсификации процесса биодеградации.
