
- •1. Введение
- •1. Допастеровская эра (до 1865 г.).
- •2. Послепастеровская эра (1866 – 1940 гг.).
- •3. Эра антибиотиков (1941-1960 гг.).
- •4. Эра управляемого биосинтеза (1961 – 1975 гг.).
- •5. Эра новой биотехнологии (после 1975 г.).
- •Вопросы для самоконтроля
- •2. Живая клетка – основа биологических систем
- •Эндоплазматический ретикулум (эр)
- •Аппарат Гольджи
- •Цитоплазматический матрикс
- •Клеточные органеллы
- •Хлоропласты
- •Клеточная стенка
- •3. Общая характеристика организмов – объектов биотехнологии
- •Эукариоты. Водоросли
- •Принципы подбора биотехнологических объектов
- •Вопросы для самоконтроля
- •4. Основы генетики микроорганизмов
- •Репликация
- •Синтез белка
- •Регуляция генной активности
- •Изменчивость
- •Генетическая рекомбинация
- •Плазмиды
- •Вопросы для самоконтроля
- •5. Метаболизм и принципы его регуляции
- •Анаболизм и катаболизм
- •Углеводы как источник энергии
- •Анаэробное дыхание
- •Брожение
- •Молочнокислое брожение
- •Спиртовое брожение
- •Маслянокислое брожение
- •Аминокислоты как источник энергии
- •Липиды как источники энергии
- •Двууглеродные соединения как источники энергии
- •Рост микроорганизмов на углеводных средах, спиртах, органических кислотах, углеводородах, с1-соединениях
- •Вопросы для самоконтроля
- •6. Ассимиляция у автотрофных и гетеротрофных организмов
- •Биосинтез углеводов
- •Поглощение света и возбуждение пигментов.
- •Биосинтез нуклеиновых кислот
- •Синтез пуриновых нуклеотидов:
- •Регуляция метаболизма
- •Первичные метаболиты
- •Производство аминокислот.
- •Производство органических кислот.
- •Производство спиртов.
- •Производство витаминов.
- •Вторичные метаболиты
- •Антибиотики.
- •Вопросы для самоконтроля
- •7. Питание микроорганизмов
- •Механизм поступления веществ в клетку
- •1) Пассивная диффузия.
- •4) Перенос (транслокация) групп.
- •1.Фотолитотрофия.
- •2. Фотоорганотрофия.
- •3. Хемолитотрофия.
- •4. Хемоорганотрофия.
- •Потребности микроорганизмов в дополнительных питательных веществах
- •Минеральные элементы.
- •Ростовые вещества.
- •Вопросы для самоконтроля
- •8. Рост, размножение и культивирование микроорганизмов
- •Рост бактериальной клетки
- •Размножение бактерий
- •Размножение бактериальной популяции
- •Непрерывные культуры
- •Синхронные культуры
- •Вопросы для самоконтроля
- •9. Подготовка биологических объектов для биотехнологического процесса
- •Гибридизация микроорганизмов
- •1. Получение генов.
- •2. Введение гена в вектор.
- •3. Перенос генов в клетки организма-реципиента.
- •4. Идентификация клеток-реципиентов, которые приобрели желаемый ген (гены).
- •Генетическая инженерия и конструирование новых организмов
- •Улучшение продуцентов, используемых в производстве, методами генетической инженерии
- •Клеточная инженерия
- •Получение гибридных клеток
- •Возможности клеточной инженерии
- •Культуры тканей и клеток высших растений
- •Культуры клеток животных и человека
- •Трансплантация эмбрионов
- •Гибридомная технология
- •Вопросы для самоконтроля
- •10. Культивирование биологических объектов
- •Принципы действия и конструкции биореакторов
- •Системы перемешивания и аэрации
- •1. Аппараты с механическим перемешиванием.
- •2. Аппараты с пневматическим перемешиванием.
- •3. Аппараты с циркуляционным перемешиванием.
- •Лабораторные, пилотные и промышленные биореакторы: проблемы масштабирования
- •Биотехнологические процессы и аппараты периодического и непрерывного действия
- •Периодические процессы.
- •Специализированные типы биотехнологических процессов и аппаратов Анаэробные процессы.
- •Твердофазные и газофазные процессы.
- •Поверхностные процессы.
- •Вопросы для самоконтроля
- •11. Словарь терминов
- •12.Список использованной литературы
Антибиотики.
Антибиотики – самый большой класс фармацевтических соединений, синтез которых осуществляется микробными клетками. К этому классу относятся противогрибковые агенты, противоопухолевые лекарства и алкалоиды. Открытие антибиотиков произвело переворот в лечении инфекционных заболеваний. Несмотря на то, что некоторые вопросы о физиологических функциях антибиотиков, их месте в метаболизме и процессах эволюции окончательно не решены, можно сказать, что они появились в борьбе за существование почвенных биоценозов, поэтому многие из них служат средствами защиты и нападения в клетке. Кроме того, антибиотики могут участвовать в процессах детоксикации вредных метаболитов, контролировать некоторые стороны обмена веществ, служить запасными питательными веществами.
Количество открываемых антибиотиков постоянно растет. Если в 1940 г. было известно всего 6 антибиотиков, то в настоящее время описано более 12000 аналогичных соединений, из которых в медицинской практике применяют около 200 препаратов. 97 % известных антибиотиков токсичны, поэтому в практике не используются.
Вначале антибиотики классифицировали по их продуцентам – грибам, эубактериям, актиномицетам. В настоящее время в зависимости от химической природы и ряда других свойств антибиотики делят на ряд классов:
1) ß-Лактамные (пенициллин, цефалоспорин);
2) тетрациклины;
3) макролиды (эритромицин, олеандомицин);
4) аминогликозиды (гентамицин);
5) гликопептиды (ванкомицин);
6) амфениколы (левомицетин);
7) линкосамиды (линкомицин);
8) противогрибковые (нистатин, леворин);
9) противоопухолевые (блеомицин).
Большой вклад в установление структуры ряда антибиотиков внесли М.М. Шемякин, Ю.А. Овчинников, В.Т. Иванов, А.С. Хохлов, Г.Б. Локшин, М.Н. Колосов и др.
Начиная с середины 1960-х гг. в связи с возросшей сложностью выделения эффективных антибиотиков и распространением устойчивости к наиболее широко применяемым соединениям у большого числа патогенных бактерий исследователи перешли от поиска новых антибиотиков к модификации структуры уже имеющихся. Устойчивость к пенициллинам и цефалоспоринам связана с наличием ферментов ß-лактамаз у бактерий, актиномицетов, цианобактерий и дрожжей. Фермент гидролизует амидную связь ß-лактамного цикла в молекуле антибиотика с образованием пенициллиновой кислоты, которая лишена антимикробной активности. Исследователями был открыт новый класс ß-лактамных антибиотиков – тиенамицины, чрезвычайно эффективный против грампозитивных и грамнегативных бактерий, а также способный ингибировать ß-лактамазы. К природным ингибиторам ß-лактамаз относятся клавулановая и оливановая кислоты.
Антибиотики вырабатываются в результате совместного действия продуктов 10-30 генов, поэтому практически невозможно обнаружить отдельные спонтанные мутации, приводящие к повышению выхода антибиотика. В настоящее время большинство высокопродуктивных штаммов продуцентов антибиотиков получено в результате последовательных циклов мутагенеза и селекции. Например, 21 цикл мутагенеза и селекции, продолжавшийся более двадцати лет, позволил четырем группам исследователей увеличить выход пенициллина в 55 раз. В настоящее время промышленный выход пенициллина в 10000 раз превышает выход, полученный в 1941 г. Флори и Чейном.
Биосинтез антибиотиков возрастает в конце тропофазы и достигает максимума в идиофазе. Исследователи считают, что в конце тропофазы изменяется энзиматический статус клеток, появляются индукторы вторичного метаболизма. Поэтому любые механизмы, тормозящие активный рост клеток, стрессовые ситуации, активируют образование антибиотиков.
Процесс культивирования идиолитов проходит две фазы. На первой фазе происходит накопление достаточного количества биомассы, которая выращивается в среде для роста микроорганизмов. Эта фаза должна быть быстрой, а среда дешевой. На второй фазе осуществляются запуск и активный синтез антибиотика. Ферментацию ведут на продуктивной среде, т.к. образование антибиотика регулируется условиями культивирования.
Многие антибиотики происходят от промежуточных соединений обмена первичных метаболитов, поэтому их биосинтез регулируется путем ретроингибирования. Например, биосинтез пенициллина культурой гриба Penicillium chrysogenumконтролируется по принципу обратной связи лизином (рис. 41). Этот эффект объясняется тем, что биосинтез как пенициллина, так и лизина осуществляется через общий предшественник – α-аминоадипиновую кислоту. Ингибирование лизином фермента гомоцитратсинтетазы приводит к недостатку α-аминоадипиновой кислоты, что снижает выход антибиотика. Добавление в питательную среду α-аминоадипиновой кислоты предотвращает ингибирующий эффект лизина и активирует биосинтез пенициллина.
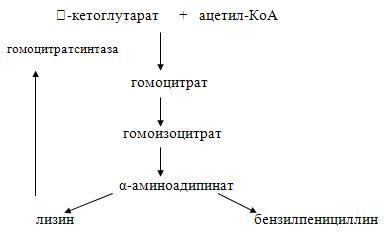
Рис.41. Ингибирование лизином биосинтеза бензилпенициллина
Таким образом, регуляция метаболизма имеет большое значение при получении как первичных, так и вторичных метаболитов. Это необходимо учитывать при реализации биотехнологического процесса.
