
n1
.pdfМетаболізм вуглеводів
Метаболізм вуглеводів являє собою одну з найважливіших складових частин обміну речовин як єдиного цілого. Обмін вугле- водів у людини охоплює весь складний процес їх перетворення: від надходження до організму з їжею, перетравлювання і всмок- тування в шлунково-кишковому тракті до утворення кінцевих продуктів – CO2 и H2O.
Серед вуглеводів їжі найбільшу біологічну цінність, тобто здат- ність засвоюватися організмом людини, мають полісахариди – кро- хмаль (амілоза й амілопектин), глікоген; дисахариди – сахароза, лак- тоза, мальтоза. Лише невелика частка вуглеводів їжі припадає на моносахариди (глюкоза, фруктоза, пентози).
Добовапотреба дорослої людиниу вуглеводах становить 400–500 г.
Через відсутність відповідних ферментів, як зазначалося вище, вуглеводи, що мають -глікозидні зв'язки – целюлоза, ксилоза, пекти-
ни та інші не можуть розщеплюватися до своїх мономерів ні в шлун- ково-кишковому тракті, ні в клітинах. Але вони відіграють допоміжну роль у травленні, активуючи механічну діяльність кишечника.
Перетравлювання вуглеводів їжі
Перетравлювання – це сукупність процесів ферментативного гі- дролізу великих молекул полісахаридів, білків, ліпідів, нуклеїнових кислот їжі до більш дрібних компонентів, головним чином, до своїх мономерів, які можуть всмоктуватися і потім зазнавати метаболіч- них перетворень. Дуже важливо, що в процесі перетравлювання їжі її
компоненти – білки, вуглеводи, ліпіди, нуклеїнові кислоти – втрача- ють свою видову і тканинну специфічність. Це, по-перше, створює можливість досить швидкого їх використання організмом і, по- друге, захищає цей організм від несприятливого впливу на імунні ре- акції і стан генетичного апарата.
Процес перетравлювання вуглеводів починається вже в ротовій порожнині під впливом ферментів слини – -амілази і -глюкозидази
(мальтази). -Амілаза слини являє собою суміш близьких ізофермен- тів, які електрофоретично розділяються. Кожен із них є одноланцюго-
вим поліпептидом (М.м. 56 000), до якого приєднується олігосахарид. Амілаза розщеплює крохмаль і глікоген, а -глюкозидаза – мальтозу.
-Амілаза слини є ендоамілазою і розриває внутрішні зв'язки в моле-
кулах рослинного крохмалю і глікогену з утворенням уламків поліса- харидів різної величини, так званих декстринів, і мальтози. Якщо сли- ну інкубувати з крохмалем і через певні інтервали часу проводити йо- дну пробу суміші, то вихідне синє забарвлення поступово змінює колір до пурпурового, потім червоно-коричневого внаслідок утворення так званих еритродекстринів. Пізніше проба з йодом дає жовте забарв-
лення з дрібнішими ахродекстринами, і, нарешті, перестає давати за- барвлення після того, як -амілаза слини розщеплює всі молекули
крохмалю. Оскільки в ротовій порожнині їжа знаходиться менше од- нієї хвилини, мальтози і глюкози утворюється небагато.
241
У шлунковому соку відсутні амілолітичні ферменти. Пере-
творення крохмалю в шлунку пов'язане лише з можливою залиш- ковою активністю слинної -амілази. Остання виявляє каталітич-
ну дію при нейтральній або слабколужній реакції. У шлунку ж реа- кція кисла (pH = 1,5–2,5), тому розщеплення вуглеводів у ньому триває близько 20–40 хв, поки харчова маса не стане остаточно кислою під впливом соляної кислоти.
Розщеплення вуглеводів відбувається переважно в дванадцяти- палій кишці та інших відділах тонкого кишечника під впливом фер- ментів підшлункової залози і кишкового соку.
Панкреатична -амілаза ( -1,4-глюкан-4-глюканогідролаза) за деякими властивостями нагадує -амілазу слини і має оптимум pH 7,1. Оптимальне значення pH у тонкому кишечнику досягається внаслідок змішування кислого шлункового вмісту з лужними панкре- атичними і жовчними секретами. Дія панкреатичної -амілази на крохмаль і глікоген призводить до утворення мальтози.
Перетравлювання дисахаридів їжі і дисахаридів, що утворилися внаслідок дії -амілази, закінчується в тонкому кишечнику.
Гідроліз дисахаридів відбувається, головним чином, у клітинах слизової оболонки, в яких присутні мальтаза, сахараза і лактаза. Ці ферменти знаходяться в щітковій каймі епітелію слизової оболонки в кількостях, достатніх для нормального засвоєння вуглеводів їжі.
Такий тип перетравлювання називається контактним, або пристінковим. Як результат мальтоза розщеплюється на дві мо- лекули глюкози, сахароза – на глюкозу і фруктозу, і лактоза – на глюкозу і галактозу.
Лактоза зустрічається тільки як компонент молока; її концент- рація в жіночому молоці удвічі вища, ніж у коров'ячому. Активність же лактази обмежена навіть у період годування дитини і може зник- нути зовсім після його припинення. Недостатня активність лактази може становити серйозну проблему для дітей.
При тривалому годуванні немовлят материнським молоком, надходження лактози може досягати 30–40 г/доб і перевищувати ла- ктазну потужність. Неперетравлена лактоза не засвоюється організ- мом дитини і може замість цього підтримувати небажаний розвиток кишкової флори. Перехід до коров'ячого молока або до «суміші», яка включає сахарозу, сприяє подоланню такого явища.
Клітковина, яка міститься у харчових продуктах, не атакується жодним із ферментів шлунково-кишкового тракту і лише в товстій кишці під впливом ферментів мікроорганізмів – бактеріальних це- люлаз ( -глюкозидаз) – вона частково розщеплюється до дисахариду целобіози і глюкози. Останні далі розкладаються з утворенням оц- тової та інших органічних кислот (масляної, молочної, пропіонової), що всмоктуються в кров, а також деяких летких продуктів (вуглекис- лого газу, водню, метану), що виводяться назовні. Органічні кисло- ти, які утворилися з клітковини, стимулюють перистальтику, тому рослинні полісахариди іноді вживаються як м'які послаблюючі. Але
242
вживання великої кількості клітковини без кулінарно-технічної об- робки спричиняє посилення процесів бродіння в кишечнику і накопи- чення газу (метеоризм).
Мікроорганізми товстого кишечника використовують також клітковину для біосинтезу деяких вітамінів, наприклад, вітамінів К, В12 та фолієвої кислоти.
Всмоктування вуглеводів у кишечнику
Всмоктування вуглеводів у тонкому кишечнику – складний біо- хімічний процес. Глюкоза, галактоза і фруктоза всмоктуються із по- рожнини кишечника з високою ефективністю, але з різною швидкіс- тю, а саме (за зменшенням швидкості всмоктування): галактоза > глюкоза > фруктоза > маноза > ксилоза > арабіноза.
Через мембрани клітин тонкої кишки прості сахари за градієн- том концентрації шляхом простої дифузії можуть надходити в кров і лімфу. Але зараз доведено, що прості сахари всмоктуються шляхом вторинного активного транспорту за допомогою іонів Na+.
Вважають, що білки-переносники на зовнішній поверхні мем- бран клітин тонкої кишки сполучаються з певним моносахаридом (глюкозою або галактозою) та іонами Na+, утворюючи рухомий комплекс Na+–переносник–моносахарид. Процес транспорту потре- бує витрат енергії і за своєю сутністю є ферментативною реакцією. Сказане підтверджується тим, що всмоктування поліпшується у разі підвищення активності ферменту аденозинтрифосфатази, яка роз- щеплює АТФ з утворенням АДФ та фосфату, що супроводжується звільненням енергії для активації транспортного механізму.
Про ферментативну сутність процесу транспорту вуглеводів сві- дчить також спряженість перетравлювання вуглеводів (зокрема при- стінкового) до моносахаридів з їх всмоктуванням. Припускають (О.М.Уголєв), що в мембрані мікроворсинок існує єдина каталітична система, яка об'єднує функції ферменту і переносника і забезпечує передачу моносахариду на переносник. Завдяки такій системі найко- ротшим шляхом і швидко здійснюється всмоктування.
Важливою ланкою механізму усмоктування вуглеводів є транс- мембранний перенос іонів Na+ і K+. Зокрема, іони Na+ необхідні для транспорту моносахариду проти градієнта концентрації. До різних контактних ділянок білка-переносника приєднуються іон Na+ і моно- сахарид, і у вигляді такого комплексу вони проходять через мембра- ну в цитоплазму клітини тонкої кишки. У цитоплазмі комплекс роз- падається, моносахарид використовується в клітині або транспорту- ється у кров, а іон Na+ «відкачується» із клітин Na+, K+-АТФазою – складною енергозалежною ферментною системою. При цьому іони K надходять («накачуються») у клітину.
Таким чином, всмоктування вуглеводів спряжене з певними лан- ками обміну електролітів – іонів Na+ і K+.
Перетворення вуглеводів після всмоктування
Моносахариди всмоктуються з тонкого кишечника в кров і сис- темою ворітної вени потрапляють у печінку і далі в інші органи і
243
тканини. У печінці близько 5% глюкози витрачається на синтез глі- когену; 30–35% глюкози перетворюється на жири, а основна маса – 60–65% окислюється до СО2 і Н2О зі звільненням енергії. При зни- женій м'язовій активності і багатій вуглеводовмісній дієті на біоси- нтез глікогену може витрачатися до 10–12% глюкози, а на біосин- тез жирів – до 40%.
Невелика кількість глюкози завжди циркулює в крові і є необхід- ною умовою нормального обміну речовин в організмі. У дорослих людей вміст глюкози коливається у вузьких, так званих гомеостатич- них, межах, складаючи в середньому 0,8–1,2 г/л або 3,33–5,55 ммоль/л. Це забезпечується регулюючим впливом нейрогуморальної системи.
Підвищення вмісту глюкози в крові вище зазначеного рівня на- зивається гіперглікемією (hyper – через, над; glykys – солодкий; haima – кров, грецьк.). У разі зростання вмісту глюкози в крові вище так званого ниркового порогу (понад 1,8 г/л) гіперглікемія вже супро- воджується виділенням цукру із сечею – глюкозурією (glykys – солод- кий, uron – сеча, грецьк.). Гіперглікемія може бути фізіологічною і патологічною. Перша трапляється за умов вживання великої кілько- сті вуглеводів і називається аліментарною або харчовою гіперглікемі- єю. Патологічна ж гіперглікемія і глюкозурія спостерігаються при захворюванні цукровим діабетом. Захворювання пов'язане з нестачею гормону підшлункової залози – інсуліну. Докладніше питання буде розглядатися далі в главі «Гормони».
При підвищених фізичних навантаженнях, тривалих нервово- психічних напруженнях, у випадках передозування інсуліну під час лі- кування цукрового діабету вміст цукру в крові може зменшитися, на- стає гіпоглікемія (hypo – зменшення, грецьк.). Це також спостеріга- ється при деяких захворюваннях, наприклад, пухлинах мозку, пухли- нах у підшлунковій залозі (інсулінома), тяжких ураженнях паренхіми печінки та інших порушеннях.
Збільшення в крові вмісту глюкози відбувається переважно за ра- хунок двох чинників: розщеплення глікогену в печінці і всмоктування із кишечника простих сахарів, в основному глюкози. Розщеплення глі- когену в печінці здійснюється переважно шляхом фосфоролізу під впливом -глікогенфосфорилази з утворенням глюкозо-1-монофос- фату, який під впливом ферменту фосфоглюкомутази перетворюєть- ся на глюкозо-6-монофосфат. Останній під впливом ферменту глюко- зо-6-фосфатази розщеплюється на глюкозу і фосфорну кислоту.
У печінці відбувається також гідролітичне розщеплення глікоге- ну з утворенням вільної глюкози. Але цей процес має обмежене зна- чення. Глюкоза, що утворилася, потрапляє у кров та інші тканини. Окрім глюкози в крові міститься в невеликих кількостях фруктоза, галактоза і пентози.
Надходження глюкози в клітини
Концентрація вільної глюкози в цитозолі більшості клітин дуже низька, тоді як концентрація її в плазмі крові підтримується близь-
244
кою до 5,0 ммоль/л. Тому надходження глюкози в клітини здійсню- ється в напрямку падіння градієнта концентрацій.
Але воно відбувається не як проста дифузія крізь безладно роз- міщені пори мембрани, а як полегшений процес із недостатньо ви- вченим механізмом. Він не пов'язаний з використанням АТФ або іо- ну Na+, але, можливо, включає мембранний переносник, діючий спе- цифічно в різних клітинах: еритроцитах, м'язах, мозку. Очевидно, відповідний білок-переносник вбудований у мембрану так, що гліко- зилюється на зовнішній стороні мембрани за допомогою сульфгід- рильних груп. Підраховано, що на одну клітину припадає 2 105 таких центрів, кожен з яких переносить понад 500 молекул глюкози в секу- нду. Надходження глюкози в клітини печінки здійснюється шляхом простої дифузії.
Взаємоперетворення простих сахарів
У тонкому кишечнику, як вже зазначалося, всмоктуються перева- жно глюкоза і в невеликих кількостях фруктоза і галактоза. Оборот- ний процес переходу глюкози в галактозу, фруктозу і навпаки відбува- ється в процесі обміну в багатьох реакціях, зокрема, під час біосинтезу глікогену, коли галактоза перетворюється на глюкозу, особливо в ор- ганізмі дитини, яка харчується молоком і молочними продуктами. Не менше біологічне значення має і протилежний процес, тобто пере- творення глюкози на галактозу, що особливо важливо в період лакта- ції в жінок. У дієті матері домінують вуглеводи, котрі містять глюко- зу, а для синтезу молочного цукру необхідна і галактоза.
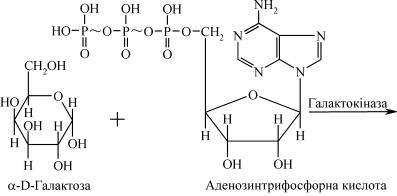
Процес перетворення галактози на глюкозу відбувається в печінці шляхом фосфорилювання за рахунок АТФ під впливом ферменту галактокінази, внаслідок чого утворюється галактозо-1- монофосфат і АДФ. Галактозо-1-монофосфат потім під впливом ферменту гексозо-1-монофосфат-уридилтрансферази вступає в реакцію з уридиндифосфоглюкозою (УДФ-глюкозою). Як резуль- тат утворюється уридиндифосфогалактоза (УДФ-галактоза) і глю- козо-1-монофосфат.
245
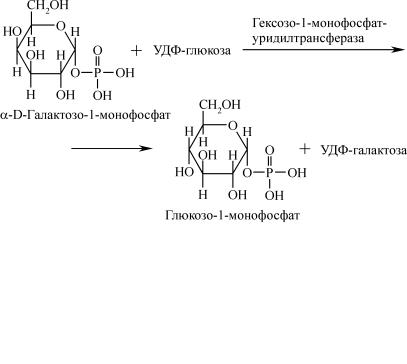
УДФ-галактоза використовується для біосинтезу лактози, тобто молочного цукру, а глюкозо-1-монофосфат – для біосинтезу глікогену.
Анаеробний шлях обміну вуглеводів
Утворення енергії в клітинах відбувається не тільки в процесі окислювального фосфорилювання (аеробним шляхом), але і в про- цесі розпаду поживних речовин без участі молекулярного кисню (анаеробним шляхом).
При провідній ролі тканинного дихання в людини і вищих тва- рин реакції анаеробного обміну вуглеводів відіграють хоча й обме- жену, але важливу роль у забезпеченні організму енергією.
Майже універсальним процесом генерування метаболічної ене- ргії в біологічних системах є гліколіз. Термін гліколіз походить від грецьких слів glykys – цукор (солодкий) и lysis – розчинення.
Гліколіз– це послідовність реакцій, які призводять до перетворен- ня глюкози в молочну кислоту(лактат) з одночаснимутворенням АТФ.
У людини й інших аеробних організмів гліколіз передує циклу трикарбонових кислот і ланцюга переносу електронів, у процесі яких вилучається велика частина енергії, що міститься в глюкозі.
В аеробних умовах метаболіт гліколізу – піруват проникає в мі- тохондрії, де він повністю окислюється до CO2 и H2O.
246
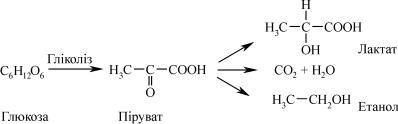
У разі недостатнього вмісту кисню, як це може мати місце, на- приклад, у м'язах, що активно скорочуються, піруват перетворюється у лактат. В анаеробних організмах, таких, як дріжджі, піруват пере- творюється не в лактат, а в етанол. Утворення етанолу із глюкози – це приклад спиртового бродіння.
Вивчення гліколізу має багату історію і відбувалося разом із роз- витком біохімії. Основне відкриття зробили цілком випадково Ганс і Едуард Бюхнери в 1897 р. Вони працювали над одержанням безклі- тинних екстрактів дріжджів з метою їх лікувального застосування. Ці екстракти потрібно було зберігати без добавлення антисептиків, та- ких, як фенол, і вони вирішили випробувати сахарозу, яка звичайно за- стосовується для зберігання продуктів у харчовій хімії. Результат був несподіваний: під дією дріжджового соку сахароза швидко зброджува- лась, утворюючи спирт. Це відкриття мало велике значення, бо впер- ше було доведено, що бродіння може відбуватися поза живими кліти- нами. До цього вважалося, згідно з твердженням Луї Пастера, вислов- леним у 1860 р., що бродіння нерозривно пов'язане з живими клітина- ми. Відкриття Бюхнерів, яке заперечувало цю віталістичну догму, від- крило двері новій біохімії. Метаболізм став хімією.
Повністю гліколітичний шлях був установлений в 40-х рр. голо- вним чином завдяки працям Густава Ембдена, Отто Мейергофа, Карла Нойберга, ЯковаПарнаса, ОттоВарбурга, ГертіКорі йКарлаКорі.
Основні молекулярні механізми гліколізу і глікогенолізу
Якщо процес починається з глікогену, його називають глікогено- лізом. Окремі стадії цих процесів каталізуються відповідно 10 і 11 основними ферментами. Вони утворюють ланцюг функціонально зв'язаних ферментів (поліферментна функціональна система), у якому продукт реакції попереднього ферменту є субстратом для на- ступного. Ферменти гліколізу лабільно сполучені з мембранами ен- доплазматичної сітки.
Першою фазою глікогенолізу і гліколізу є утворення глюкозо- фосфорних ефірів. Якщо процес починається з глікогену, то внаслі- док дії ферменту глікогенфосфорилази від нього відщеплюється глюкозо-1-монофосфат (I продукт), який внаслідок дії ферменту фо- сфоглюкомутази за участю глюкозо-1,6-дифосфату перетворюється на глюкозо-6-монофосфат (II продукт).
247
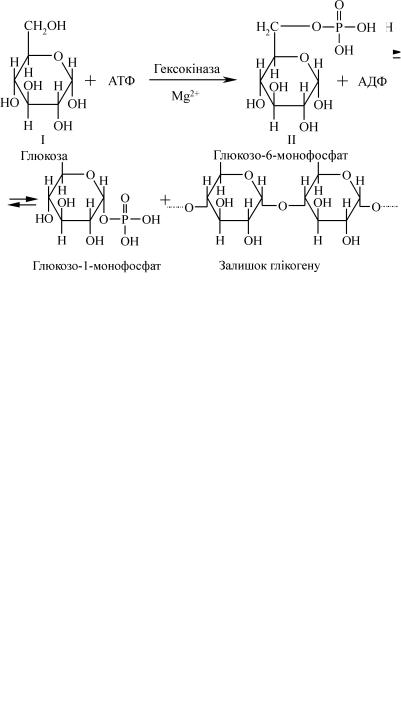
Якщо процес починається з глюкози, то глюкозо-6-моно- фосфат під впливом гексокінази утворюється за рахунок переносу залишку фосфорної кислоти з АТФ на глюкозу, при цьому АТФ перетворюється в АДФ.
Доля глюкози всередині клітини однозначна: вона фосфори- люється за участю АТФ з утворенням глюкозо-6-фосфату. Перенос фосфатної групи з АТФ на гідроксильну групу біля С-6 глюкози ка-
талізується гексокіназою:
248
Гексокіназа– це фермент, здатний переносити фосфатну групу від АТФ до різних шестивуглецевих сахарів (гексоз). Гексокіназа, подібно до всіх інших кіназ, потребує для прояву своєї активності іон Мg2+ (або інший двовалентний іон металу), які утворюють комплекс зАТФ.
Гексокіназна реакція практично необоротна у фізіологічних умовах. Гексокіназа присутня в клітинах організму у вигляді чоти- рьох типів ізоферментів (I, II, III і IV). Найбільшою специфічністю до глюкози відзначається гексокіназа IV – глюкокіназа. Вона не пе- ретворює інші гексози і діє тільки в печінці при високому вмісті глю- кози. Інші гексокінази фосфорилюють не лише глюкозу, але й інші гексози при звичайних їх концентраціях у клітинах. Гексокіназа I осо- бливо активна в нирках, печінці; гексокіназа II – у м'язовій і жировій тканинах; гексокіназа III – у печінці й селезінці. Гексокінази II і IV змінюють свою активність під впливом гормонів, у першу чергу – ін- суліну. Найбільші можливості у «виловлюванні» глюкози має печін- ка, яка містить весь набір ізоферментів гексокінази.
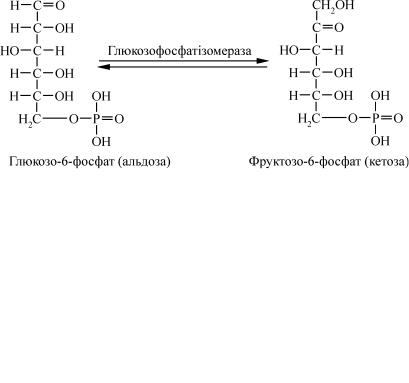
Наступний етап гліколізу – це ізомеризація глюкозо-6-фосфату (продукту II) у фруктозо-6-фосфат (продукт III). Шестичленне піра- нозне кільце глюкозо-6-фосфату перетворюється на п’ятичленне фу- ранозне кільце фруктозо-6-фосфату. Ця оборотна реакція каталізу-
ється ферментом глюкозофосфатізомеразою.
Сутність даної реакції стане зрозумілою, якщо підставити в це рівняння форми моносахаридів з відкритим ланцюгом:
249
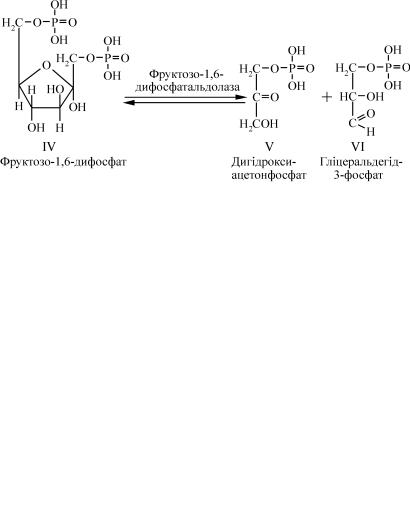
За стадією ізомеризації відбувається друга реакція фосфорилю- вання. Фруктозо-6-фосфат фосфорилюється за рахунок АТФ з утво- ренням фруктозо-1,6-дифосфату (продукт IV).
Реакція каталізується алостеричним (регуляторним) ферментом фосфофруктокіназою. У цій реакції відбувається значна втрата віль- ної енергії, тому вона практично необоротна. Фосфофруктокіназа (М.м. 360 000) має складну четвертинну структуру і є «ключовим» ферментом гліколізу, який лімітує швидкість усього процесу. Ката- літична активність фосфофруктокінази перебуває під алостеричним контролем з боку АТФ і деяких інших метаболітів. Тому АТФ споча- тку використовується як субстрат, а потім зв'язується з алостерич- ним центром і припиняє фосфофруктокіназну реакцію.
Фруктозо-1,6-дифосфат є вже типовим субстратом гліколізу. Цей субстрат (продукт IV) під дією ферменту альдолази (фруктозо-1,6-ди- фосфатальдолази) розщеплюється на дві тріози: дигідроксиацетонфо- сфат (ДОФ, продукт V) і гліцеральдегід-3-фосфат (продукт VI).
У подальших реакціях гліколізу беруть участь тривуглецеві, а не шестивуглецеві сполуки. Назва ферменту «альдолаза» відображає природу оборотної реакції, що являє собою альдольну конденсацію. Такий розподіл молекули гексози на дві молекули тріози називається дихотомією (dicho – поділ на двоє и tome – різання, грецьк.). Тому глі- коліз ще називають дихотомічним циклом обміну вуглеводів.
Найважливішим продуктом гліколізу є гліцеральдегід-3-фосфат (продукт VI). Це не стосується дигідроксиацетонфосфату, оскільки
250
