
- •Часть I
- •Тема 3. Химическая термодинамика и кинетика.
- •Основные понятия и определения.
- •Первый закон термодинамики
- •Изменение энтальпии в различных химических и физико-химических процессах.
- •Второй закон термодинамики.
- •Абсолютная энтропия идеального кристалла при ок равна нулю.
- •Энергия Гиббса.
- •Анализ уравнения Гиббса.
- •Основные понятия.
- •Закон действия масс
- •Зависимость скорости от температуры.
- •2.3 Обратимые и необратимые реакции. Химическое равновесие. Константа равновесия. Принцип Ле-Шателье. Фазовые равновесия. Правило фаз. Химическое равновесие.
- •Химическая кинетика. Химическое равновесие. Правило Ле Шателье-Брауна.
- •Фазовые равновесия.
- •Правило фаз.
- •Катализ Общие понятия.
- •Фотохимические реакции.
- •Тема 4. Растворы
- •Классификация дисперсных систем.
- •Общие свойства растворов.
- •Растворимость
- •Энергетика процесса растворения.
- •4.2Два вида электролитов: сильные и слабые электролиты. Электролитическая диссоциация в водных растворах. Ионное произведение воды. Водородный показатель. Электролиты и неэлектролиты.
- •Водородный показатель, или pH раствора.
- •Тема 5. Окислительно-восстановительные и электрохимические процессы.
- •5.1.Электрохимические процессы. Равновесие на границе металл-раствор. Электродный потенциал. Уравнение Нернста. Водородный электрод. Ряд напряжений. Гальванический элемент. Электродвижущая сила.
- •Электроны от перешли к ионам восстановили их в свободный металл и в растворе остались ионы железа.
- •Термодинамика гальванического элемента
- •Уравнение Нернста для определения потенциала при любых условиях
- •5.2. Электрохимические источники тока.
- •Химические цепи.
- •Свинцовый аккумулятор
- •Щелочной аккумулятор:
- •Топливные элементы.
- •Тема 2. Строение вещества
- •Валентность.
- •Тема 6. Химическая идентификация и анализ вещества.
- •6.1 Химическая идентификация вещества. Идентификация катионов и анионов. Количественный анализ: гравиметрический, титриметрический анализ.
- •Химическая идентификация вещества
- •Количественный анализ.
- •6.2 Инструментальные методы анализа.
- •Тема 7.Свойства металлов и их соединений
- •7.1. Физические и химические свойства металлов. Получение металлов. Металлические сплавы и композиты.
- •Тема 8 Полимерные материалы и их применение
- •8.1 Методы получения полимеров: полимеризация, поликонденсация. Свойства полимеров. Применение полимеров и олигомеров.
- •Тема 9. Заключительная лекция.
- •9.1. Экологические проблемы общества. Охрана воздушного и водного бассейна. Предельно допустимые нормы содержания вредных веществ в биосфере. Очистка сточных вод.
- •Классификация сточных вод и примесей в них.
- •Методы и оборудование для очистки сточных вод.
- •Биологическая очистка сточных вод.
- •Проверка воды на содержание газов. Дегазация.
- •Умягчение воды.
- •Методы опреснения воды
- •Электродиализ
- •Метод обратного осмоса
- •Опреснение воды вымораживанием
- •Метод опреснения воды основанный на явлении гидратации
- •Метод солнечной дистилляции
- •Список литературы
Изменение энтальпии в различных химических и физико-химических процессах.
Обычно энтальпии образования имеют абсолютные значения от (±) сотен до нескольких тысяч кДж/моль. Стандартные значения энтальпий сгорания органических веществ имеют отрицательные значения. Фазовые переходы, при которых простое или сложное вещество переходит из одной твердой модификации в другую, обычно сопровождаются энергетическими эффектами порядка десятых долей единиц или нескольких десятков кДж/моль.
![]() ;
;
![]() кДж/моль
кДж/моль
Любой человеческий организм является открытой термодинамической
системой. Основным источником энергии для него является химическая энергия, заключенная в пищевых продуктах, часть которой расходуется на:
1. совершение работы внутри организма, связанной с дыханием,
кровообращением;
2. нагревание вдыхаемого воздуха, потребляемой воды, пищи;
3. совершение внешней работы, связанной со всеми перемещениями человека и его трудовой деятельностью (при нормальной трудовой деятельности энергетические затраты человека покрываются за счет углеводов на 56 - 60 %, жиров на 20- 25 %, белков 15-20 %).
В процессе пищеварения углеводы разлагаются на глюкозу, которая растворяется в крови и реагирует с кислородом в несколько стадий.
![]()
![]() кДж
кДж
В связи с тем, что
топливо и пища обычно представляют
собой смеси, их теплотворная способность
указывается в расчете не на 1 моль, а на
1 кг. Средняя калорийность углеводов
![]() кДж/ кг, а жиров
кДж/ кг, а жиров![]() кДж/кг.
кДж/кг.
Суточная потребность человека в энергии составляет в среднем при умеренной и напряженной работе (лаборанты, врачи, учащиеся, студенты) 12500 -15100 кДж.
Направление самопроизвольно протекающих процессов. Движущие силы химического процесса. Понятие об энтропии.
Первое начало термодинамики утверждает, что все виды энергии взаимно превращаются в строго эквивалентных количествах. Но не даёт ответа на вопросы, почему процесс протекает именно в этом направлении, а не в обратном; настолько полно осуществляется превращение энергии из одного вида в другой.
Решение этих вопросов невозможно на основе первого начала, поэтому
используют иные термодинамические критерии.
В 1867 году Бертло сформулировал критерий возможности осуществления химических реакций:
1. Самопроизвольно могут протекать такие химические реакции,
которые сопровождаются выделением тепла.
Например:
![]()
![]()
![]()
![]()
Но существуют самопроизвольные процессы, которые сопровождаются поглощением тепла. Это эндотермические реакции типа:

Очевидно, не одно только стремление системы свести к минимуму свой запас внутренней энергии, выделить избыток этой энергии в окружающую среду является движущей силой для самопроизвольного протекания химических и физико-химических процессов.
2. Стремление системы к максимальному беспорядку.
Например:имеются два газообразных баллона, соединенных трубкой с краном и заполненные не реагирующими друг с другом газами азотом и оксидом углерода СО, имеющими одинаковыеt, Р и молекулярные массы . После открытия крана начинается активный процесс смешения газов. Наблюдается стремление системы к беспорядку.
Самопроизвольный процесс смешения газов в этом примере будет протекать без изменения энтальпии. Но обратный процесс разделения газов самопроизвольно протекать не будет: его можно осуществить, только затрачивая работу из вне. В самопроизвольных процессах система переходит от менее вероятного состояния к более вероятному.
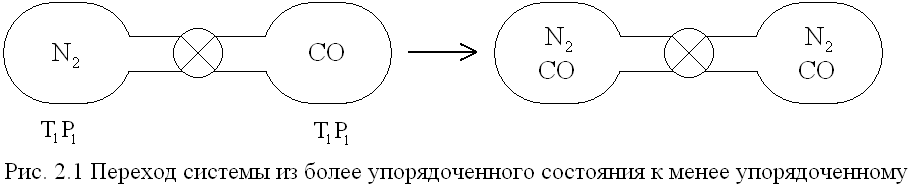
Мерой беспорядка системы служит энтропия S( Дж/моль·К);
