
- •Часть I
- •Тема 3. Химическая термодинамика и кинетика.
- •Основные понятия и определения.
- •Первый закон термодинамики
- •Изменение энтальпии в различных химических и физико-химических процессах.
- •Второй закон термодинамики.
- •Абсолютная энтропия идеального кристалла при ок равна нулю.
- •Энергия Гиббса.
- •Анализ уравнения Гиббса.
- •Основные понятия.
- •Закон действия масс
- •Зависимость скорости от температуры.
- •2.3 Обратимые и необратимые реакции. Химическое равновесие. Константа равновесия. Принцип Ле-Шателье. Фазовые равновесия. Правило фаз. Химическое равновесие.
- •Химическая кинетика. Химическое равновесие. Правило Ле Шателье-Брауна.
- •Фазовые равновесия.
- •Правило фаз.
- •Катализ Общие понятия.
- •Фотохимические реакции.
- •Тема 4. Растворы
- •Классификация дисперсных систем.
- •Общие свойства растворов.
- •Растворимость
- •Энергетика процесса растворения.
- •4.2Два вида электролитов: сильные и слабые электролиты. Электролитическая диссоциация в водных растворах. Ионное произведение воды. Водородный показатель. Электролиты и неэлектролиты.
- •Водородный показатель, или pH раствора.
- •Тема 5. Окислительно-восстановительные и электрохимические процессы.
- •5.1.Электрохимические процессы. Равновесие на границе металл-раствор. Электродный потенциал. Уравнение Нернста. Водородный электрод. Ряд напряжений. Гальванический элемент. Электродвижущая сила.
- •Электроны от перешли к ионам восстановили их в свободный металл и в растворе остались ионы железа.
- •Термодинамика гальванического элемента
- •Уравнение Нернста для определения потенциала при любых условиях
- •5.2. Электрохимические источники тока.
- •Химические цепи.
- •Свинцовый аккумулятор
- •Щелочной аккумулятор:
- •Топливные элементы.
- •Тема 2. Строение вещества
- •Валентность.
- •Тема 6. Химическая идентификация и анализ вещества.
- •6.1 Химическая идентификация вещества. Идентификация катионов и анионов. Количественный анализ: гравиметрический, титриметрический анализ.
- •Химическая идентификация вещества
- •Количественный анализ.
- •6.2 Инструментальные методы анализа.
- •Тема 7.Свойства металлов и их соединений
- •7.1. Физические и химические свойства металлов. Получение металлов. Металлические сплавы и композиты.
- •Тема 8 Полимерные материалы и их применение
- •8.1 Методы получения полимеров: полимеризация, поликонденсация. Свойства полимеров. Применение полимеров и олигомеров.
- •Тема 9. Заключительная лекция.
- •9.1. Экологические проблемы общества. Охрана воздушного и водного бассейна. Предельно допустимые нормы содержания вредных веществ в биосфере. Очистка сточных вод.
- •Классификация сточных вод и примесей в них.
- •Методы и оборудование для очистки сточных вод.
- •Биологическая очистка сточных вод.
- •Проверка воды на содержание газов. Дегазация.
- •Умягчение воды.
- •Методы опреснения воды
- •Электродиализ
- •Метод обратного осмоса
- •Опреснение воды вымораживанием
- •Метод опреснения воды основанный на явлении гидратации
- •Метод солнечной дистилляции
- •Список литературы
Электродиализ
Процесс удаления
из растворов поляризованных веществ
путем переноса их через мембрану в поле
постоянного электрического тока, В
такой системе возникает направленное
движение ионов растворенных солей, а
также ионов
![]() и
и![]() ,
причем катионы движутся к катоду, анионы
- к аноду.
,
причем катионы движутся к катоду, анионы
- к аноду.
На катоде:
![]()
![]()
Анодные реакции:
![]()
![]()
Для предотвращения
переноса ионов
![]() и
и![]() образующихся по реакциям, электродиализатор
разделяют на отсеки с помощью специальных
мембран, проницаемых только для катионов
или только для анионов (рис.1.1).
образующихся по реакциям, электродиализатор
разделяют на отсеки с помощью специальных
мембран, проницаемых только для катионов
или только для анионов (рис.1.1).
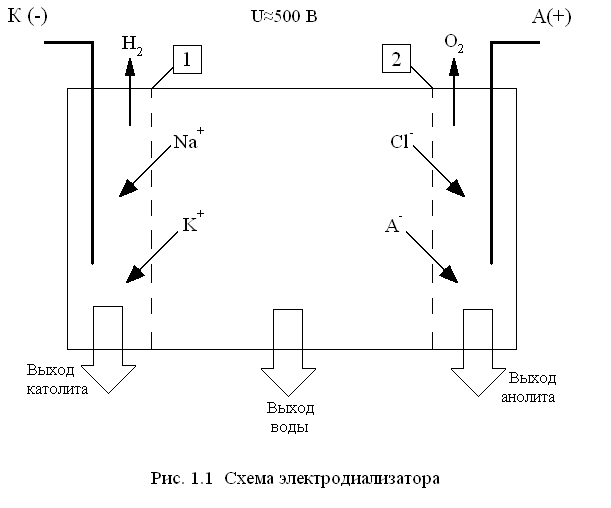
1 – катионитовая мембрана; 2 – анионитовая мембрана;
Расход электроэнергии
на 1
![]() водыQ=96500
водыQ=96500![]()
Метод обратного осмоса
Осмос - это самопроизвольная диффузия растворителя из менее концентрированного раствора в более концентрированный раствор через полупроницаемую перегородку. Если чистую воду отделить такой перегородкой от соленой воды, то молекулы воды проникнут в раствор, разбавляя его. Уровень раствора повысится (рис.1.2).
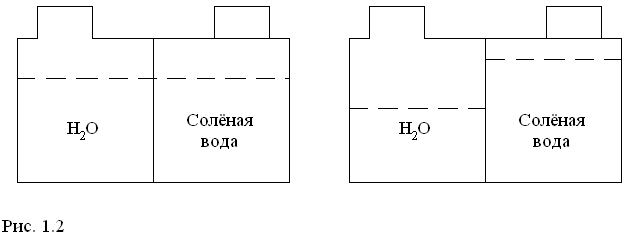
Схема самопроизвольной диффузии
Разница уровней в момент равновесия будет характеризоваться осмотическим давлением раствора. Зависит Росм от концентрации раствора. Если к раствору приложить давление большее, чем Росм, то будет наблюдаться явление обратного осмоса: вода из раствора будет переходить в направлении, обратном естественной диффузии (рис.1.3).

Схема опреснения воды методом обратного осмоса
Вода проходит через отверстия в 3,5 А, а молекулы солей через поры
более 5 А.В качестве
полупроницаемых мембран применяются
пористый фарфор, пропитанный ферроцианидом
меди (II)
![]() .Стоимость
получения пресной воды этим методом
составляет 1 доллар за 16000 л.
.Стоимость
получения пресной воды этим методом
составляет 1 доллар за 16000 л.
Опреснение воды вымораживанием
Известно, что лед, образовавшийся при замерзании морской воды, почти не содержит солей.
Морская вода представляет собой раствор солей, и при замерзании воды и соли образуют различные кристаллографические структуры.
Если чистая вода
замерзает при 0°, то морская вода с
солесодержанием 35 г/л при t=
- 1,85°. Этим по видимому обусловлен тот
факт, что при замерзании морской воды
в первую очередь образуются кристаллы
пресного льда, а затем замерзает рассол,
который в виде тонких оболочек покрывает
эти кристаллы. При медленном замерзании
получают более крупные кристаллы льда
со значительно меньшими кристаллами
рассола. Процесс таяния идет в обратной
последовательности - сначала из морского
льда стекает охлажденный рассол![]() ,
а затем чистая вода.
,
а затем чистая вода.
Опреснение воды вымораживанием состоит из трех основных операций; образования кристаллов льда, отделение их от рассола и плавление льда.
Такие установки разработали в Японии (1969). У нас спроектирована такая установка в Туркмении, производит 30 кг/час.
Метод опреснения воды основанный на явлении гидратации
В соленый раствор
вводят под давлением
![]() - хладоагент, способный обрабатывать
кристаллогидраты
- хладоагент, способный обрабатывать
кристаллогидраты![]() и
и![]() ).
Газгидраты представляют собой льдоподобные
кристаллы, состоящие из молекул воды и
неполярных молекул газов. На каждую
молекулу гидратообразующего газа
приходится 7-18 молекул воды.
).
Газгидраты представляют собой льдоподобные
кристаллы, состоящие из молекул воды и
неполярных молекул газов. На каждую
молекулу гидратообразующего газа
приходится 7-18 молекул воды.
