
- •Часть I
- •Тема 3. Химическая термодинамика и кинетика.
- •Основные понятия и определения.
- •Первый закон термодинамики
- •Изменение энтальпии в различных химических и физико-химических процессах.
- •Второй закон термодинамики.
- •Абсолютная энтропия идеального кристалла при ок равна нулю.
- •Энергия Гиббса.
- •Анализ уравнения Гиббса.
- •Основные понятия.
- •Закон действия масс
- •Зависимость скорости от температуры.
- •2.3 Обратимые и необратимые реакции. Химическое равновесие. Константа равновесия. Принцип Ле-Шателье. Фазовые равновесия. Правило фаз. Химическое равновесие.
- •Химическая кинетика. Химическое равновесие. Правило Ле Шателье-Брауна.
- •Фазовые равновесия.
- •Правило фаз.
- •Катализ Общие понятия.
- •Фотохимические реакции.
- •Тема 4. Растворы
- •Классификация дисперсных систем.
- •Общие свойства растворов.
- •Растворимость
- •Энергетика процесса растворения.
- •4.2Два вида электролитов: сильные и слабые электролиты. Электролитическая диссоциация в водных растворах. Ионное произведение воды. Водородный показатель. Электролиты и неэлектролиты.
- •Водородный показатель, или pH раствора.
- •Тема 5. Окислительно-восстановительные и электрохимические процессы.
- •5.1.Электрохимические процессы. Равновесие на границе металл-раствор. Электродный потенциал. Уравнение Нернста. Водородный электрод. Ряд напряжений. Гальванический элемент. Электродвижущая сила.
- •Электроны от перешли к ионам восстановили их в свободный металл и в растворе остались ионы железа.
- •Термодинамика гальванического элемента
- •Уравнение Нернста для определения потенциала при любых условиях
- •5.2. Электрохимические источники тока.
- •Химические цепи.
- •Свинцовый аккумулятор
- •Щелочной аккумулятор:
- •Топливные элементы.
- •Тема 2. Строение вещества
- •Валентность.
- •Тема 6. Химическая идентификация и анализ вещества.
- •6.1 Химическая идентификация вещества. Идентификация катионов и анионов. Количественный анализ: гравиметрический, титриметрический анализ.
- •Химическая идентификация вещества
- •Количественный анализ.
- •6.2 Инструментальные методы анализа.
- •Тема 7.Свойства металлов и их соединений
- •7.1. Физические и химические свойства металлов. Получение металлов. Металлические сплавы и композиты.
- •Тема 8 Полимерные материалы и их применение
- •8.1 Методы получения полимеров: полимеризация, поликонденсация. Свойства полимеров. Применение полимеров и олигомеров.
- •Тема 9. Заключительная лекция.
- •9.1. Экологические проблемы общества. Охрана воздушного и водного бассейна. Предельно допустимые нормы содержания вредных веществ в биосфере. Очистка сточных вод.
- •Классификация сточных вод и примесей в них.
- •Методы и оборудование для очистки сточных вод.
- •Биологическая очистка сточных вод.
- •Проверка воды на содержание газов. Дегазация.
- •Умягчение воды.
- •Методы опреснения воды
- •Электродиализ
- •Метод обратного осмоса
- •Опреснение воды вымораживанием
- •Метод опреснения воды основанный на явлении гидратации
- •Метод солнечной дистилляции
- •Список литературы
Тема 8 Полимерные материалы и их применение
8.1 Методы получения полимеров: полимеризация, поликонденсация. Свойства полимеров. Применение полимеров и олигомеров.
Полимеры, или высокомолекулярные соединения (ВМС), получили свое название из-за большой молекулярной массы, отличающей их от низкомолекулярных веществ, молекулярная масса которых лишь сравнительно редко достигает нескольких сотен. В настоящее время принято относить к ВМС вещества с молекулярной массой более 5000.
Молекулу полимерного вещества называют макромолекулой, а процесс соединения многих молекул в макромолекулу - полимеризацией или поликонденсацией, в зависимости от типа реакции, лежащей в основе процесса. Молекулу низкомолекулярного соединения, вступающего в полимеризацию, называют мономером. Вещества, которые по молекулярной массе и свойствам занимают промежуточное положение между полимерами и мономерами, называют олигомерами. Молекулярная масса олигомеров примерно от 500 до 5000. Как правило, они не обладают свойствами ВМС, но и не могут быть отнесены к низкомолекулярным соединениям. Олигомеры представляют собой молекулярно однородные вещества, они являются гомологами полимеров и по физическим свойствам настолько отличаются друг от друга, что могут быть разделены на индивидуальные химические соединения.
Олигомеры с более высокой молекулярной массой по свойствам приближаются к полимерам и не могут быть разделены на индивидуальные соединения.
Макромолекулы большинства ВМС построены из одинаковых, многократно повторяющихся групп атомов - элементарных звеньев, например, элементарным звеном макромолекулы натурального каучука является участок цепи строения
![]()
элементарное звено
Поэтому для каучука принимают суммарную формулу (С5Н8)Л. Индекс n в таких формулах обозначает число элементарных звеньев, входящих в состав макромолекулы, характеризует степень полимеризации ВМС. Степень полимеризации Р связана с молекулярной массой полимера М уравнением Р=М/т, где т - молекулярная масса элементарного звена. При изучении строения макромолекулы полимера наряду с определением химического строения элементарных звеньев, порядка их чередования и пространственного расположения большое значение приобретает определение формы макромолекулы. По форме макромолекул ВМС разделяются на линейные, разветвленные, сетчатые, пространственные и др. (рис. 16).
Макромолекулы линейных полимеров представляют собой длинные цепи с очень высокой степенью асимметрии (их поперечный размер в вытянутом состоянии соответствует поперечному размеру молекулы мономера, а длина в сотни и тысячи раз превышает этот размер). К линейным полимерам относятся природные высокомолекулярные соединения (целлюлоза, белки), натуральный каучук и очень большое число синтетических полимеров.
Макромолекулы разветвленного полимера представляют собой цепи с боковыми ответвлениями. Число боковых ответвлений, а также отношение длины основной цепи к длине боковых цепей могут быть различными.
Все высокомолекулярные соединения в зависимости от происхождения подразделяют на природные, выделенные из природных материалов (часть из которых мы уже рассмотрели выше), искусственные, полученные путем химической модификации природных полимеров, и синтетические, полученные путем синтеза из низкомолекулярных соединений.
По строению основной цепи высокомолекулярные соединения делятся на три большие класса.
1. Высокомолекулярные соединения, основная цепь которых построена из одинаковых атомов, образуют гомоцепные полимеры, например, если цепь построена из атомов углерода, то это карбоцепные полимеры.
Из природных органических полимеров к карбоцепным относится натуральный каучук, а из неорганических - все модификации элементарного углерода (аморфный углерод, графит, алмаз). К синтетическим карбоцепным полимерам относятся все высокомолекулярные предельные, непредельные и ароматические углеводороды:
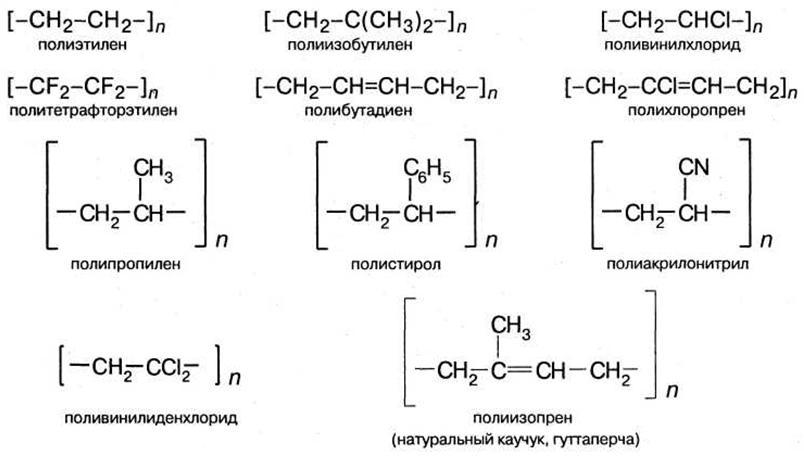
2. Высокомолекулярные соединения, основная цепь которых построена из двух или большего числа разных элементов (углерода и кислорода, углерода и азота, углерода и серы, и т. п.), образуют гетероцепные полимеры.
Гетероцепные полимеры могут быть органические и элементорганические. К органическим гетероцепным полимерам относятся важнейшие природные высокомолекулярные соединения (например, белки, полисахариды и др.), полиамиды:
H-[-NH-(CH2)x-CO-]-OH
полиамиды
Элементорганические полимеры содержат неорганическую главную цепь с органическими боковыми группами:
R




S









 i
O Al O
i
O Al O
R


 n R n
n R n
полисилоксаны полиалюмоксаны
3. Высокомолекулярные соединения с системой сопряженных связей, например:








[
 -CH=CR
- ] n
-CH=CR
- ] n
полиацителениы
n
полифенилениы
Названия карбоцепных полимеров складываются обычно из названия исходного мономера, входящего в качестве элементарного звена в состав макромолекулы полимера, и приставки поли-. Так, полимер, полученный из винилхлорида СН2=СНС1, называется поливинилхлоридом.
